Clear Sky Science · pt
Análise personalizada de vias de sinalização de tumores gastrointestinais para estratificação de pacientes e avaliação de alvos medicamentosos usando biópsias centrais derivadas clinicamente
Por que esta pesquisa importa para os pacientes
Os oncologistas estão cada vez mais tentando combinar tratamentos com a biologia única do tumor de cada pessoa. Para cânceres do sistema digestivo — como pâncreas, cólon, fígado ou ductos biliares — isso é especialmente urgente, pois são frequentes, muitas vezes diagnosticados tardiamente e de difícil tratamento. Este estudo explora um novo método laboratorial que pode ler a atividade de muitas proteínas relacionadas ao câncer a partir de pequenas amostras de biópsia, com o objetivo de ajudar médicos a escolher terapias mais precisas para pacientes individualmente.
De listas de DNA a sinais viventes
Hoje, a maior parte do cuidado “personalizado” contra o câncer baseia‑se na leitura de alterações no DNA do tumor. Embora poderoso, o DNA sozinho não mostra quais sinais dentro da célula estão realmente ativados e impulsionando o crescimento. Esses sinais são transportados por proteínas, muitas das quais podem ser alvo direto de medicamentos. Os pesquisadores usaram uma técnica de alto rendimento chamada DigiWest, uma versão moderna do clássico Western blot, para medir cerca de 130–200 proteínas e suas formas ativadas de uma só vez. Importante: esse método precisa apenas de material equivalente ao de uma única biópsia por agulha, tornando‑o adequado para uso clínico real.
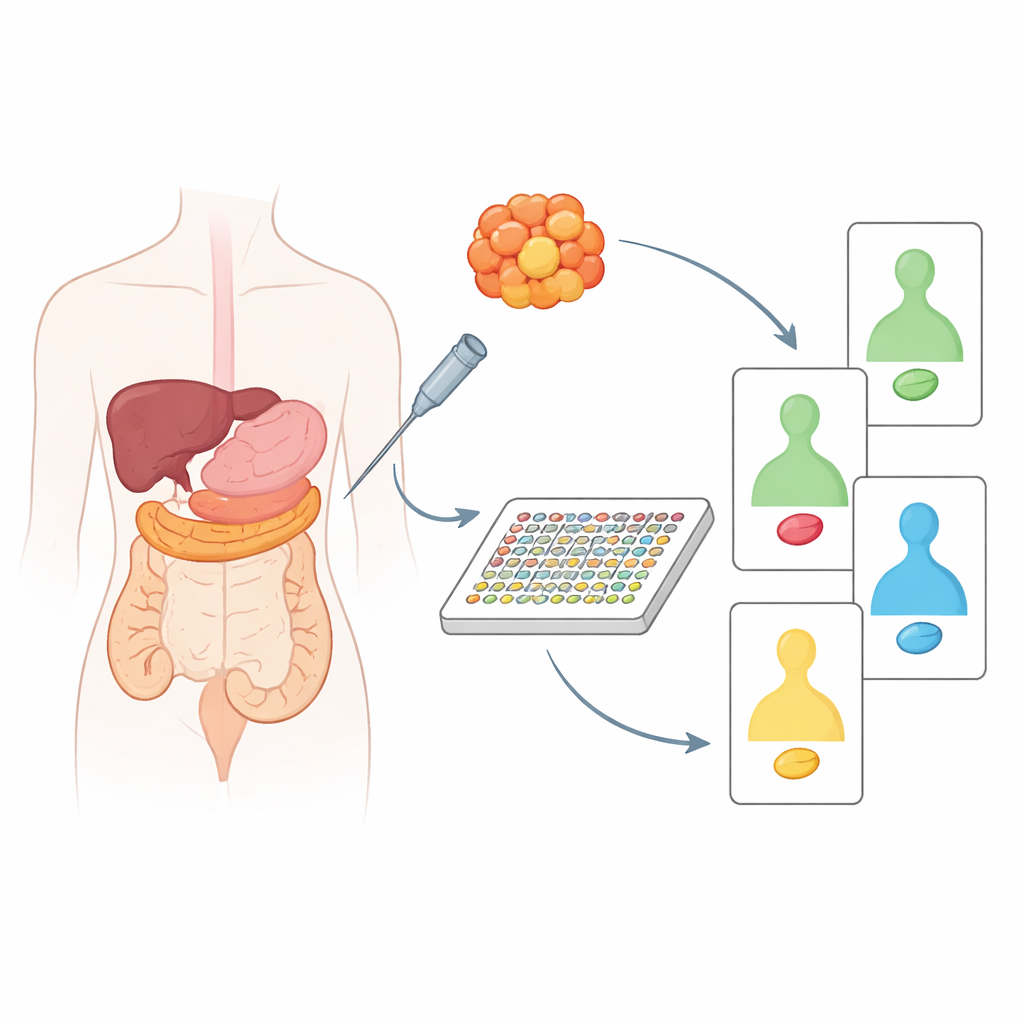
Comparando tecido tumoral com seu vizinho saudável
A equipe primeiro analisou tecido armazenado de 20 pacientes com câncer de pâncreas ou colorretal, sempre pareado com tecido não canceroso próximo da mesma pessoa. Ao comparar tumores com seus próprios contrapartes saudáveis, puderam ver quais proteínas foram realmente alteradas pelo câncer em vez de apenas refletirem diferenças normais entre órgãos. Isso revelou contrastes claros no comportamento de guardiões e motores do câncer bem conhecidos, como p53, Ras, PTEN e outros. Tumores pancreáticos, por exemplo, tenderam a mostrar sinais de promoção de crescimento intensificados e perda de proteínas protetoras, enquanto tumores de cólon apresentaram seu próprio padrão distinto de vias perturbadas. Quando os pesquisadores agruparam as amostras com base nessas alterações proteicas, conseguiram dividir os cânceres pancreáticos em dois grupos biologicamente diferentes e detectar diferenças significativas entre cânceres colorretais relacionadas à idade do paciente e à localização do tumor no intestino.
“Códigos de barras” individuais de atividade de sinalização
Indo além das médias de grupo, os cientistas construíram um perfil proteico detalhado para cada tumor. Esses perfis destacaram quais rotas de sinalização — como as envolvendo mTOR, MAPK/Erk, Wnt ou fatores relacionados ao sistema imune — estavam especialmente ativas ou desligadas. Muitas das proteínas medidas são alvos diretos de medicamentos existentes, ou atuam logo a jusante desses alvos, permitindo à equipe inferir quais fármacos poderiam interferir nos principais motores de crescimento do tumor. Em três quartos dos casos retrospectivos, conseguiram apontar uma ou mais vias que provavelmente impulsionaram a progressão tumoral. Também identificaram tumores repletos de marcadores de células imunes, sugerindo cânceres “quentes” que poderiam responder à imunoterapia, e casos incomuns com assinaturas marcadamente únicas.
Colocando o método em prática em pacientes reais
Para testar sua utilidade à beira do leito, os pesquisadores então aplicaram o DigiWest em biópsias por agulha frescas de 14 pacientes com vários cânceres gastrointestinais cujos casos eram avaliados por um Conselho Molecular de Tumores. Esses pacientes tinham trajetórias clínicas complexas e, frequentemente, tratamentos prévios. Como tecido saudável correspondente não estava disponível, os níveis proteicos de cada tumor foram comparados à mediana do grupo para definir o que seria considerado anormalmente alto ou baixo. Mesmo com essa configuração mais restrita, 12 dos 14 tumores exibiram padrões claros de atividade de vias relevantes para tratamento. Em dois exemplos detalhados, os dados proteicos confirmaram uma amplificação ao nível do DNA do gene FGFR2 em um câncer de cólon e perda de um freio do mTOR em um câncer de fígado, apoiando fortemente a consideração, pelo Conselho, de fármacos bloqueadores de FGFR ou de mTOR. De modo geral, as descobertas do DigiWest concordaram com motores genéticos chave e sugeriram alvos medicamentosos na maioria dos casos avaliáveis.
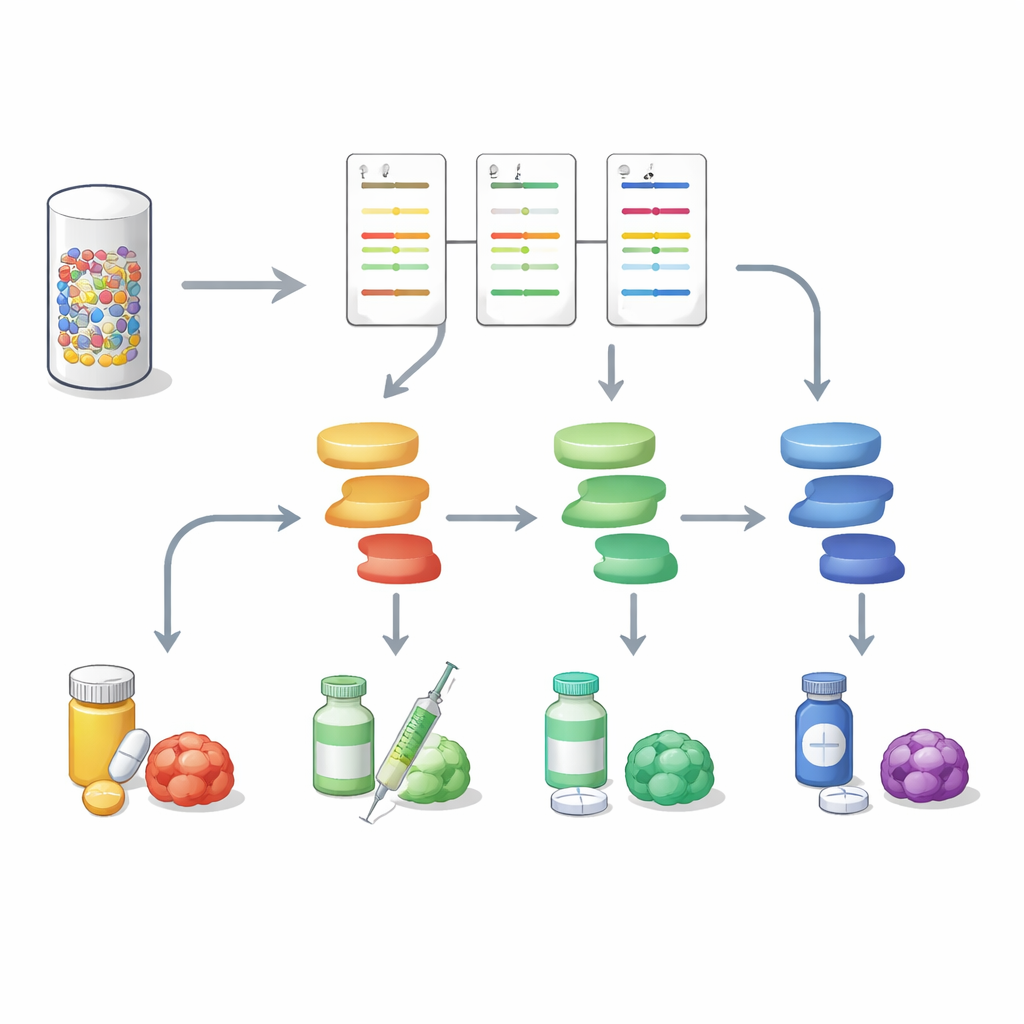
Rumo a retratos tumorais mais completos
Este trabalho mostra que analisar a sinalização proteica em paralelo com o sequenciamento de DNA pode fornecer um quadro mais rico e acionável dos tumores gastrointestinais. Ao transformar uma pequena biópsia em um mapa de atividade multi‑via, o DigiWest ajuda a distinguir quais interruptores moleculares estão realmente ligados em um câncer e quais medicamentos podem atingi‑los melhor, além de possivelmente sinalizar rotas emergentes de resistência. Embora estudos maiores ainda sejam necessários, a abordagem oferece uma forma prática de incorporar o perfil proteico de alto conteúdo na oncologia de precisão cotidiana e avançar rumo a planos de tratamento adaptados ao tumor vivo de cada paciente, e não apenas à sua impressão genética.»
Citação: Stahl, A., Büringer, K., Missios, P. et al. Personalized signaling pathway analysis of gastrointestinal tumors for patient stratification and drug target evaluation using clinically derived core biopsies. npj Precis. Onc. 10, 124 (2026). https://doi.org/10.1038/s41698-026-01304-5
Palavras-chave: oncologia de precisão, câncer gastrointestinal, proteômica, perfilagem de biópsia, terapia direcionada