Clear Sky Science · pt
Retenção de splicing e divergência de enhancers governam o destino evolutivo de ohnólogos após duplicação genômica completa em truta-arco-íris
Por que cópias extras de genes importam nos peixes
A truta-arco-íris, como muitos outros peixes, carrega um legado incomum em seu DNA: em algum ponto de sua história, todo o genoma foi duplicado. Isso significa que muitos de seus genes existem em pares, levantando uma questão básica sobre evolução: o que acontece com todas essas cópias extras ao longo de milhões de anos? Este estudo examina como esses genes duplicados são usados, reduzidos e reaproveitados nas trutas, com foco em como são ativados e desativados e como suas mensagens são cortadas e rearranjadas antes de produzir proteínas. As respostas ajudam a explicar como genomas vertebrados complexos podem inovar sem desmoronar sob sua própria complexidade.
De um genoma para dois
Há cerca de 80–100 milhões de anos, os ancestrais de salmões e trutas passaram por uma duplicação completa do genoma. Em vez de ter apenas uma cópia de cada gene, eles de repente tinham duas, chamadas “ohnólogos”. Cópias extras criam oportunidades: uma pode manter a função original enquanto a outra experimenta novos papéis. Mas também geram riscos, porque a célula precisa manter o equilíbrio geral da atividade gênica sob controle. Usando um genoma de alta qualidade da truta-arco-íris, dados de expressão gênica de seis órgãos e comparações com um peixe estreitamente relacionado (o lúcio-do-norte) que não passou pela mesma duplicação, os autores acompanharam quase dez mil pares de genes duplicados para ver como eles evoluíram ao longo do tempo profundo.
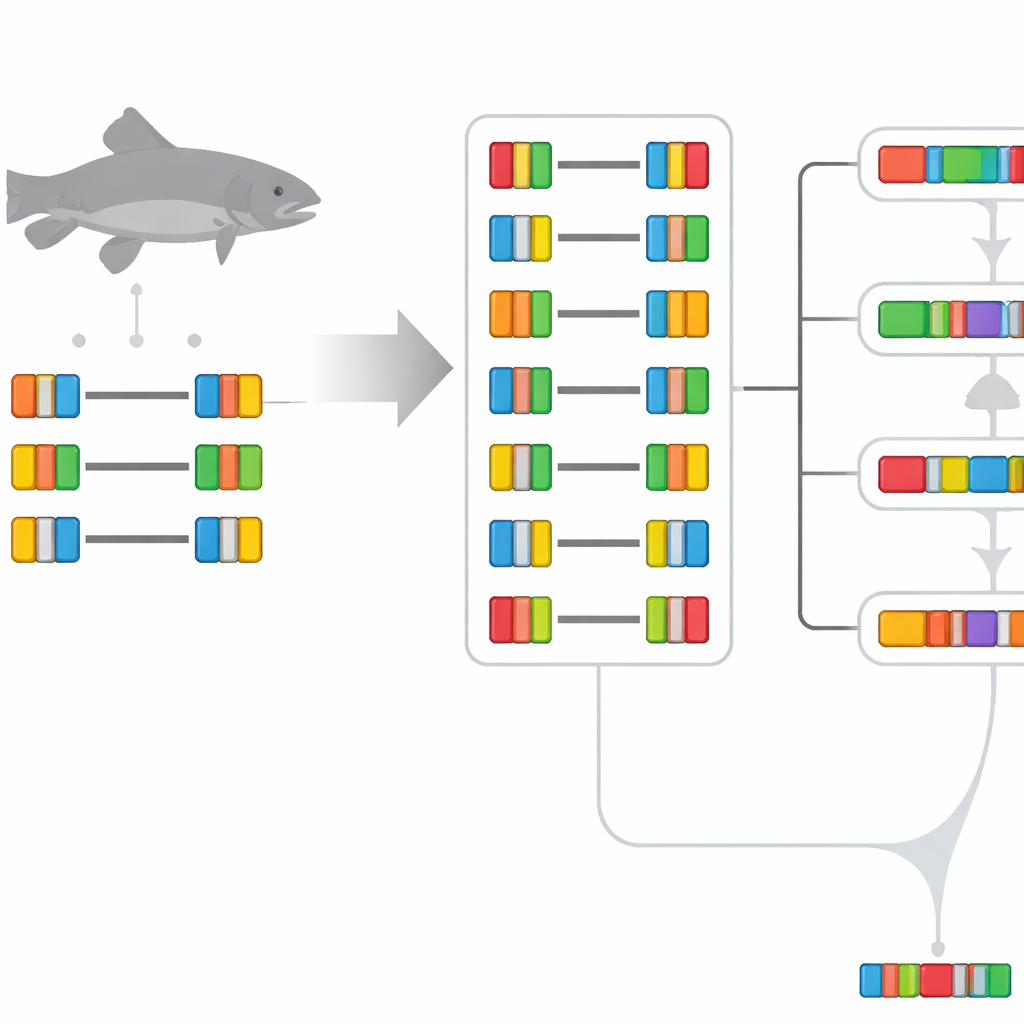
Manter, ajustar ou reinventar funções gênicas
A equipe descobriu que o destino mais comum dos genes duplicados na truta é surpreendentemente conservador. Mais de 70% dos pares de genes ainda apresentam padrões de expressão semelhantes ao gene ancestral inferido, o que significa que ambas as cópias mantiveram, em grande parte, o mesmo papel e atividade entre tecidos. Uma fração menor de pares mostra que um membro divergiu para assumir um novo padrão de expressão (neofuncionalização) ou que ambos os membros deslocaram-se juntos para padrões distintos (especialização). A divisão clássica da função original de forma equilibrada entre as duas cópias (subfuncionalização) revelou-se rara. Quando os pesquisadores estenderam a comparação para outros peixes que passaram por eventos de duplicação mais antigos, observaram que, com o passar do tempo, mais pares de genes tendem a derivar para novos papéis, especialmente em espécies com genomas menores e mais enxutos.
Como as mensagens são recortadas e coladas
Os genes não apenas são ligados ou desligados; suas mensagens de RNA podem ser editadas de diferentes maneiras por meio de um processo chamado splicing alternativo, que mistura e combina trechos da mensagem para produzir múltiplas variantes de proteína. Na truta, mais de quatro em cada cinco genes sofrem splicing alternativo, com uma média de cerca de sete formas distintas de mensagem por gene. Contrariando ideias anteriores de que cópias extras rapidamente perdem essas formas adicionais, a duplicação gênica na truta costuma vir acompanhada de um ganho na complexidade do splicing. Genes duplicados gerados pela duplicação genômica completa tendem a ter mais variantes de splicing do que genes de cópia única, e eles perdem essas variantes apenas de forma gradual ao longo do tempo evolutivo. Os autores mostram que a relação entre tamanho da família gênica e splicing não é simplesmente “mais cópias, menos variantes”, mas segue um padrão em forma de corcova: famílias gênicas de tamanho moderado tendem a ser as mais ricamente spliceadas.
Caminhos diferentes para a evolução do splicing
Para entender como o próprio splicing evolui após a duplicação, os pesquisadores compararam pares de genes da truta com seus correspondentes ancestrais de cópia única no lúcio. Agruparam os pares em três cenários. No modelo “acelerado”, os duplicados juntos apresentam mais variantes de mensagem do que o ancestral; no modelo “compartilhamento de função”, as duas cópias dividem entre si as variantes do ancestral; e no modelo “independente”, o splicing total permanece semelhante ao do ancestral. Na truta e no salmão do Atlântico, os três padrões ocorrem, mas um insight-chave é que o splicing acelerado parece comum logo após a duplicação, enquanto o modelo independente predomina a longo prazo. Com o tempo, ohnólogos perdem variantes de splicing de forma lenta, enquanto outros tipos de genes duplicados, gerados um a um e não por um evento genômico completo, tendem a ganhar variantes à medida que envelhecem.
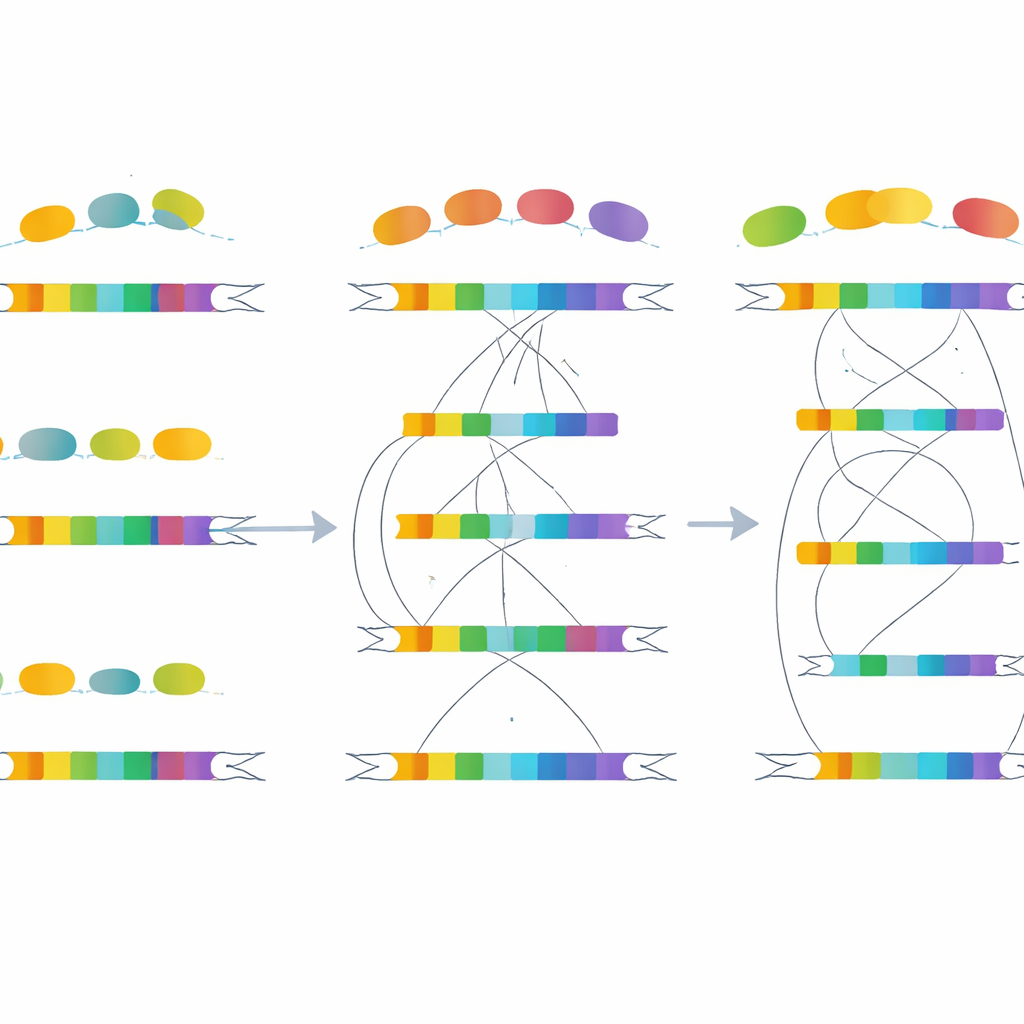
Interruptores epigenéticos e “reconfiguração” de enhancers
A história não termina nas sequências de DNA. A equipe sobrepôs mapas de marcas químicas nas proteínas que embrulham o DNA—histonas—que funcionam como sinais para regiões ativas ou silenciosas do genoma. Eles descobriram que genes duplicados geralmente exibem fortes sinais de elementos de controle ativos, especialmente em regiões que atuam como enhancers, potenciando a atividade gênica à distância. Pares de genes com padrões de splicing em rápida evolução mostram níveis particularmente altos de marcas associadas a enhancers e níveis mais baixos de marcas repressivas. Por sua vez, pares conservados exibem padrões de histonas mais semelhantes entre suas duas cópias. Isso sugere que alterações em elementos regulatórios, em vez de mudanças apenas nos corpos gênicos, ajudam a direcionar diferenças de expressão e de splicing entre os duplicados.
O que isso significa para a evolução
Em termos cotidianos, este trabalho mostra que quando todo um genoma é duplicado, a evolução frequentemente primeiro preserva ambas as cópias e permite que elas experimentem formas extras de cortar e usar suas mensagens. Somente lentamente essas opções são aparadas. Muitos genes mantêm suas funções originais por dezenas de milhões de anos, enquanto um subconjunto ramifica-se em novas funções ou padrões de expressão. De modo crucial, o estudo derruba a ideia simples de que a diversidade de splicing deve colapsar rapidamente após a duplicação e destaca um papel importante para a manutenção independente e de longo prazo dos níveis de splicing. Ao vincular esses padrões a alterações na atividade de enhancers e em marcas de cromatina, os autores fornecem um retrato mecanístico de como o “hardware” genético extra pode ser estabilizado, reaproveitado e ajustado, ajudando peixes—e, por extensão, outros vertebrados—a expandir seu repertório biológico.
Citação: Ali, A., Al-Tobasei, R., Zhou, H. et al. Splicing retention and enhancer divergence govern the evolutionary fate of ohnologues following whole-genome duplication in rainbow trout. Sci Rep 16, 13265 (2026). https://doi.org/10.1038/s41598-026-44703-1
Palavras-chave: duplicação completa do genoma, splicing alternativo, truta-arco-íris, regulação gênica, epigenética