Clear Sky Science · pt
Cinetics de reparo de DSB de DNA retardados e maior sensibilidade à radiação em pacientes com síndrome de Wiskott‑Aldrich
Por que pequenas quebras no DNA importam
Para pessoas nascidas com a síndrome de Wiskott–Aldrich, infecções e hematomas cotidianos podem ser potencialmente fatais. Esses pacientes já convivem com sistemas imunológicos frágeis e maior probabilidade de desenvolver câncer. Este estudo investiga uma pergunta crucial para o manejo clínico: quando o DNA deles é danificado por radiação médica ou certos medicamentos, as células conseguem reparar esse dano com a mesma rapidez e precisão que em outras pessoas? A resposta é não, e esse atraso pode ajudar a explicar tanto o risco aumentado de câncer quanto como os médicos devem ajustar tratamentos.
Uma doença rara com riscos ocultos
A síndrome de Wiskott–Aldrich é uma condição hereditária rara que quase sempre afeta meninos. Causa plaquetas baixas (levando a sangramentos e hematomas), eczema e fragilidade imunológica grave. O problema subjacente é uma proteína defeituosa chamada WASp, presente nas células formadoras de sangue. A WASp ajuda a organizar o esqueleto interno das células e sustenta várias funções imunes. São conhecidas mais de 440 alterações diferentes no gene da WASp, que variam de alterações severas a modificações mais brandas. Crianças com essas mutações enfrentam risco muito maior de linfoma e leucemia, o que sugere que seu DNA é mais suscetível a danos ou que os danos não são reparados adequadamente.
Observando o dano ao DNA em tempo real
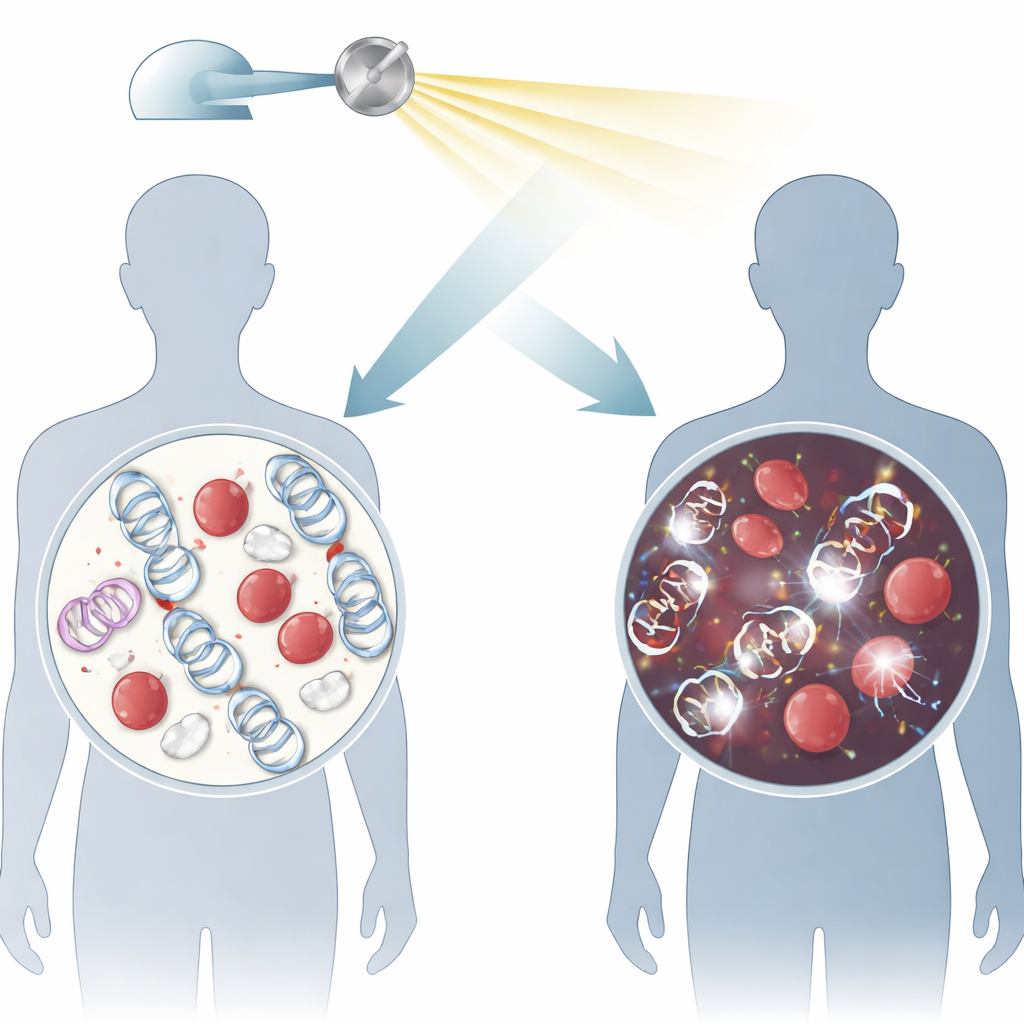
Para ver como o dano ao DNA é tratado na síndrome de Wiskott–Aldrich, os pesquisadores coletaram sangue de quatro meninos com diferentes mutações no gene WAS, de suas mães não afetadas e de quatro voluntários saudáveis. Eles se concentraram em um dos tipos mais perigosos de lesão no DNA: quebras de dupla fita, em que ambas as fitas da hélice de DNA se rompem. Essas quebras podem ser causadas por radiação ionizante, como raios gama médicos, e por alguns quimioterápicos. No laboratório, isolaram glóbulos brancos chamados linfócitos e os expuseram a uma dose padrão de radiação similar à usada em contextos clínicos.
Em vez de observar diretamente o DNA rompido, a equipe rastreou duas proteínas “sinalizadoras”, γH2AX e 53BP1, que se acumulam rapidamente nos locais de quebra e aparecem como pontos brilhantes, ou focos, sob um microscópio confocal. Contando esses focos ao longo de 24 horas e ajustando os dados com curvas matemáticas, puderam medir quão rápido as quebras surgiam e eram reparadas, e quantas permaneciam muito tempo após a exposição. Essa abordagem permitiu comparar a velocidade e a eficiência do reparo entre pacientes, mães e controles saudáveis.

Mais dano em repouso, reparo mais lento após radiação
Mesmo antes de qualquer radiação, os linfócitos de pacientes com Wiskott–Aldrich exibiam de 16 a 25 vezes mais focos de dano ao DNA do que as células de pessoas saudáveis, um sinal claro de instabilidade genômica em curso. As mães portadoras, contudo, apresentaram aparência essencialmente normal. Após a irradiação, todos os grupos mostraram aumento rápido de focos em minutos, seguido por um pico em cerca de uma a duas horas. Depois, o número de focos declinou gradualmente à medida que as células tentavam reparar. Mas nos linfócitos de Wiskott–Aldrich essa queda foi nitidamente mais lenta. Em média, o tempo necessário para que metade dos focos induzidos pela radiação desaparecesse foi cerca de 1,6 vezes maior do que em controles saudáveis. Vinte e quatro horas depois, as células dos pacientes ainda retinham aproximadamente o dobro de focos residuais em comparação com células normais, indicando que muitas quebras permaneceram não reparadas ou foram reparadas apenas muito lentamente. O grau exato do atraso variou entre os pacientes e pareceu acompanhar o quão disruptiva era a mutação específica de cada um.
Por que as mães são poupadas
As mães dos meninos afetados carregam uma cópia normal e uma cópia defeituosa do gene WAS. Neste estudo, os linfócitos delas apresentaram níveis basais de dano e velocidades de reparo quase idênticos aos de homens saudáveis não relacionados. Tanto o acúmulo quanto a redução dos focos de γH2AX e 53BP1 seguiram os mesmos padrões, e as meias‑vidas estimadas de reparo foram indistinguíveis. Isso sugere que, nessas mulheres, a cópia normal do gene é suficientemente ativa nas células sanguíneas para fornecer capacidade completa de reparo, poupando‑as da maior sensibilidade à radiação observada em seus filhos.
O que isso significa para cuidados e tratamentos
Para famílias e clínicos que lidam com a síndrome de Wiskott–Aldrich, essas descobertas têm implicações imediatas. Crianças com essa condição frequentemente passam por transplante de medula óssea, muitas vezes após irradiação corporal total ou outro condicionamento genotóxico. Saber que as células deles começam com mais dano ao DNA e eliminam novas quebras mais lentamente aponta para a necessidade de adequar com cuidado procedimentos baseados em radiação e terapias contra o câncer. O estudo fornece o primeiro mapa detalhado de como quebras de dupla fita no DNA são tratadas ao longo do tempo em linfócitos de Wiskott–Aldrich, reforçando a ideia de que esses pacientes são incomumente radiossensíveis. Em termos práticos, tratamentos mais seguros podem significar ajustar doses de radiação, escolher esquemas menos danosos ao DNA quando possível e monitorar de perto o risco de câncer a longo prazo.
Citação: Pathak, R.S., Chaurasia, R.K., Sapra, B.K. et al. Retarded DNA DSB repair kinetics and augmented radiation sensitivity in Wiskott Aldrich syndrome patients. Sci Rep 16, 13142 (2026). https://doi.org/10.1038/s41598-026-37262-y
Palavras-chave: Síndrome de Wiskott–Aldrich, Reparo de DNA, Sensibilidade à radiação, Instabilidade genômica, Transplante de medula óssea