Clear Sky Science · pt
Ensaio aprimorado de triagem multicâncer por meio de análise multimodal de DNA livre circulante baseada em sequenciamento de metilação do genoma inteiro
Por que um exame de sangue simples para vários cânceres importa
O câncer costuma ser mais curável quando detectado precocemente, mas muitos cânceres perigosos ainda não têm exame de rastreamento de rotina. Em vez de exames distintos ou endoscopias para cada órgão, este estudo investiga um único exame de sangue que poderia sinalizar vários cânceres comuns ao mesmo tempo, mesmo em estágios iniciais. Ao ler padrões químicos e estruturais sutis em fragmentos de DNA livres na circulação sanguínea, os pesquisadores mostram que uma análise cuidadosamente projetada e conduzida por computador pode identificar câncer com alta precisão e até sugerir onde no corpo ele teve início. 
Transformando uma amostra de sangue em uma janela para o corpo
O nosso sangue carrega minúsculos fragmentos de DNA liberados pelas células quando morrem e se fragmentam. Em pessoas com câncer, parte desse “DNA livre” provém dos tumores. A equipe por trás deste artigo desenvolveu um teste melhorado de detecção precoce multicâncer que examina esses fragmentos de várias maneiras ao mesmo tempo. Eles analisaram 1.415 amostras de sangue, incluindo 1.034 de pacientes com oito tipos de câncer — cólon, estômago, fígado, pâncreas, pulmão, mama, ovário e próstata — e 381 de pessoas sem câncer. O objetivo não era apenas detectar câncer, mas fazê‑lo de forma confiável em estágios iniciais, quando o DNA tumoral é escasso e facilmente ofuscado pelo DNA de células saudáveis.
Quatro pistas escondidas nos fragmentos de DNA tumoral
Os pesquisadores se concentraram em quatro características distintas do DNA livre circulante. Primeiro, mediram a metilação, um padrão químico de marcação no DNA que muda de maneiras características nos cânceres e difere entre órgãos. Em segundo lugar, procuraram alterações no número de cópias — trechos de DNA que os tumores perderam ou ganharam. Em terceiro lugar, examinaram a proporção entre fragmentos curtos e longos, já que o DNA tumoral tende a ser fragmentado em peças mais curtas. Por fim, analisaram a distribuição geral dos tamanhos dos fragmentos. Cada uma dessas características sozinha fornecia informações úteis, porém incompletas, e suas forças variavam conforme o tipo e o estágio do câncer.
Deixando o aprendizado de máquina ponderar as evidências
Para combinar esses sinais, a equipe treinou modelos de computador separados para cada característica e então construiu um modelo "ensemble" que aprendeu quanta confiança dar a cada um. Usando apenas amostras de pessoas com 50 anos ou mais — o grupo etário típico para rastreamento — ajustaram o sistema para manter baixas as falsos‑positivos, visando 95% de especificidade. Em um conjunto de teste independente, o modelo combinado detectou câncer em 93,2% dos pacientes no geral, mantendo essa especificidade de 95%. Importante, o desempenho em doenças precoces foi forte: a sensibilidade foi de cerca de 92% tanto para cânceres em estágio I quanto em estágio II, o que significa que aproximadamente nove em cada dez cânceres iniciais foram sinalizados pelo exame de sangue. 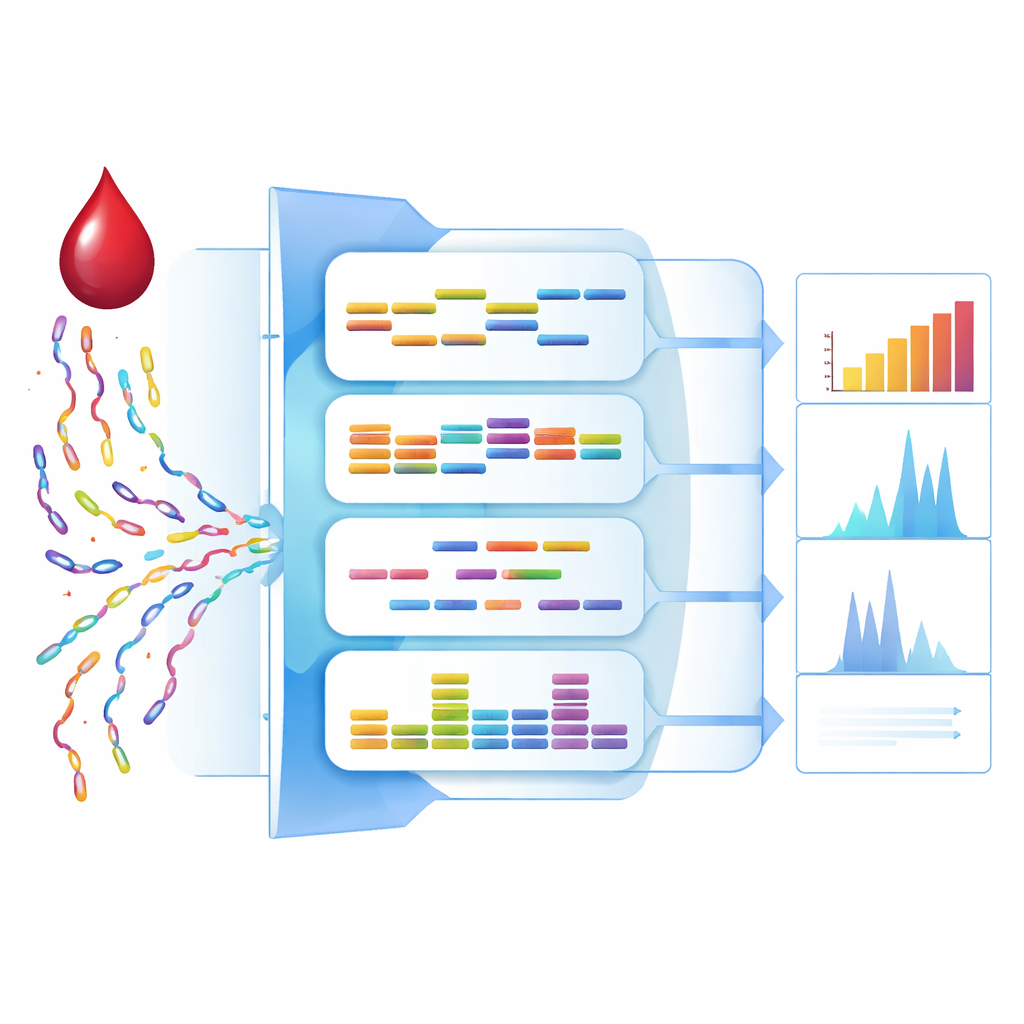
Encontrando onde o câncer começou
Além de indicar “câncer” ou “sem câncer”, o teste também tenta estimar o tecido de origem — onde no corpo o tumor provavelmente se originou. Usando as mesmas quatro características do DNA, o modelo escolheu um tipo de câncer mais provável e um segundo candidato. A primeira escolha esteve correta cerca de 73% das vezes; se os médicos considerarem tanto a primeira quanto a segunda sugestão, a precisão subiu para quase 86%. Cânceres de cólon, estômago e próstata foram identificados particularmente bem, e os cânceres de mama, quando previstos, raramente foram atribuídos incorretamente. Essas informações podem orientar exames ou procedimentos de seguimento para o órgão certo e poupar pacientes de testes sem foco.
O que isso pode significar para check‑ups futuros
Para um público não especializado, a conclusão é que uma única coleta de sangue, interpretada por meio de uma combinação sofisticada de química do DNA e algoritmos de reconhecimento de padrão, pode detectar uma ampla gama de cânceres com alta precisão, incluindo muitos em um estágio precoce e mais tratável. O estudo ainda precisa ser confirmado em grandes ensaios prospectivos de rastreamento e em populações mais diversas, e o desempenho para alguns cânceres difíceis de detectar precisa ser aprimorado. Mas o trabalho mostra que misturar vários sinais complementares do DNA em uma única decisão pode mover o rastreamento sanguíneo multicâncer do conceito para a prática no mundo real, potencialmente remodelando como procuramos câncer muito antes de os sintomas aparecerem.
Citação: Jeong, S., Go, D., Jeon, Y. et al. Enhanced multicancer screening assay through whole-genome methylation sequencing-based multimodal cell-free DNA analysis. Exp Mol Med 58, 1311–1324 (2026). https://doi.org/10.1038/s12276-026-01674-7
Palavras-chave: detecção precoce de múltiplos cânceres, biópsia líquida, DNA livre circulante, metilação do DNA, triagem de câncer