Clear Sky Science · pl
Spersonalizowana analiza szlaków sygnałowych nowotworów przewodu pokarmowego w celu stratyfikacji pacjentów i oceny celów lekowych przy użyciu klinicznie pobranych wycinków rdzeniowych
Dlaczego to badanie ma znaczenie dla pacjentów
Lekarze zajmujący się rakiem coraz częściej starają się dopasowywać terapie do unikalnej biologii guza każdego pacjenta. W przypadku nowotworów układu pokarmowego — takich jak trzustki, jelita grubego, wątroby czy dróg żółciowych — jest to szczególnie pilne, ponieważ są one częste, często rozpoznawane późno i trudne w leczeniu. W badaniu przedstawiono nową metodę laboratoryjną, która potrafi odczytać aktywność wielu białek związanych z rakiem z maleńkich próbek biopsyjnych, z zamiarem pomocy lekarzom w wyborze bardziej precyzyjnych terapii dla poszczególnych pacjentów.
Od list DNA do żywych sygnałów
Obecnie większość „spersonalizowanej” opieki onkologicznej opiera się na wykrywaniu zmian w DNA guza. Choć to potężne narzędzie, sam DNA nie pokazuje, które sygnały wewnątrz komórki są faktycznie włączone i napędzają wzrost. Te sygnały są przenoszone przez białka, z których wiele może być bezpośrednio celem leków. Naukowcy zastosowali technikę wysokoprzepustową nazwaną DigiWest, nowoczesną odmianę klasycznego Western blot, aby jednocześnie zmierzyć około 130–200 białek i ich aktywowane formy. Co ważne, metoda ta wymaga tylko tyle materiału, ile zawiera pojedyncza biopsja igłowa, dzięki czemu nadaje się do realnego zastosowania klinicznego.
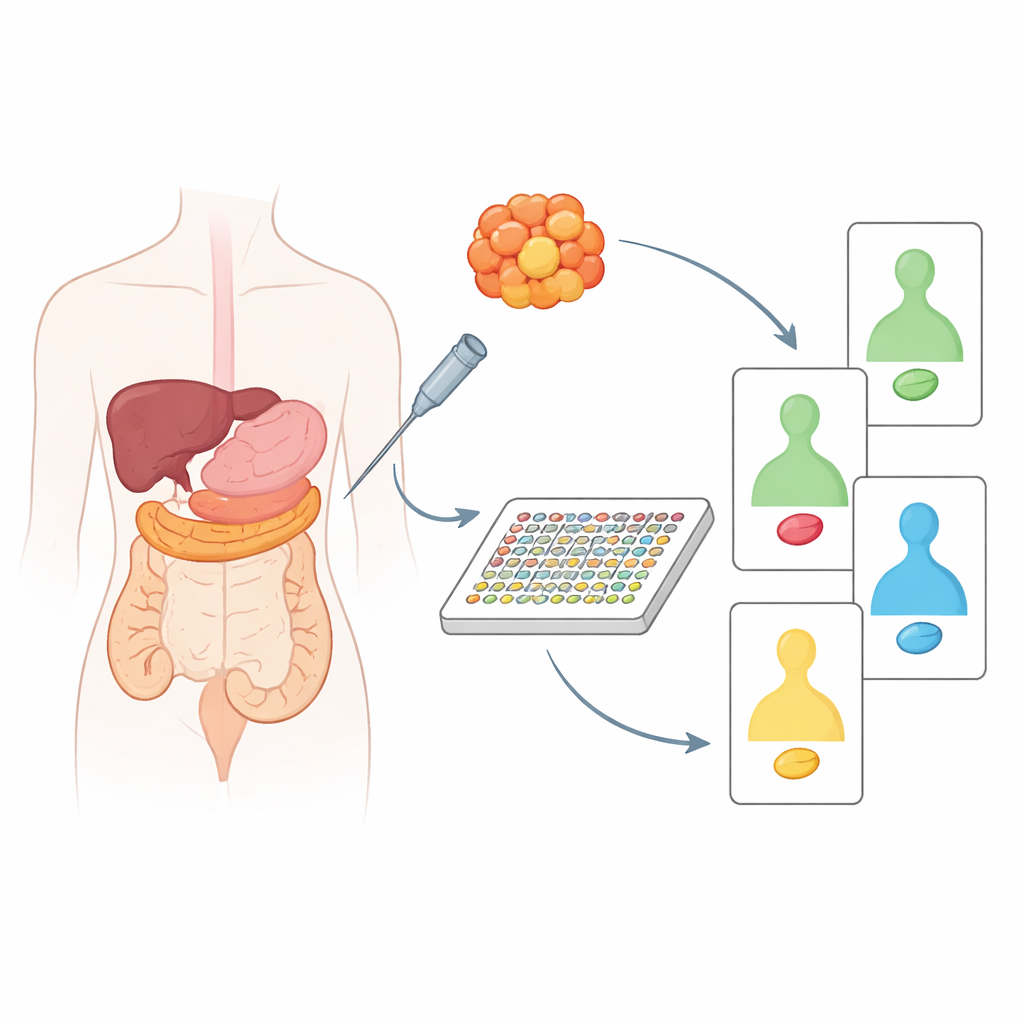
Porównanie tkanki nowotworowej z jej zdrowym sąsiadem
Zespół najpierw przeanalizował przechowywane próbki od 20 pacjentów z rakiem trzustki lub jelita grubego, zawsze sparowane z pobliską tkanką nie‑nowotworową tego samego pacjenta. Poprzez porównanie guzów z ich własnymi zdrowymi odpowiednikami mogli określić, które białka były rzeczywiście zmienione przez raka, a nie jedynie odzwierciedlały normalne różnice między narządami. Wyłoniły się wyraźne kontrasty w zachowaniu dobrze znanych strażników i czynników napędzających raka, takich jak p53, Ras, PTEN i inne. Guzy trzustki na przykład wykazywały zwykle wzmocnione sygnały sprzyjające wzrostowi i utratę białek ochronnych, podczas gdy guzy jelita grubego miały swój własny, odrębny wzorzec zaburzonych szlaków. Gdy badacze grupowali próbki na podstawie tych zmian białkowych, udało się podzielić raki trzustki na dwie biologicznie różne grupy oraz wykryć istotne różnice wśród raków jelita grubego związane z wiekiem pacjenta i lokalizacją guza w jelicie.
Indywidualne „kody kreskowe” aktywności sygnałowej guza
Wykraczając poza uśrednione wyniki grupowe, naukowcy zbudowali szczegółowy profil białkowy każdego guza. Profile te uwydatniały, które szlaki sygnałowe — takie jak obejmujące mTOR, MAPK/Erk, Wnt czy czynniki związane z odpornością — były szczególnie aktywne lub wyciszone. Wiele mierzonych białek jest bezpośrednimi celami istniejących leków albo znajduje się tuż poniżej takich celów, co pozwoliło zespołowi wnioskować, które leki mogłyby zakłócić główne „silniki” wzrostu guza. W trzech czwartych retrospektywnych przypadków potrafili wskazać jeden lub więcej szlaków, które prawdopodobnie napędzały progresję guza. Wyróżnili też guzy bogate w markery komórek odpornościowych, sugerujące „gorące” nowotwory mogące odpowiadać na immunoterapię, oraz nietypowe przypadki o wyraźnie unikalnych sygnaturach.
Wdrożenie metody u rzeczywistych pacjentów
Aby sprawdzić użyteczność przy łóżku pacjenta, badacze zastosowali następnie DigiWest do świeżych biopsji igłowych od 14 pacjentów z różnymi nowotworami przewodu pokarmowego, których przypadki były oceniane przez Molekularną Komisję Onkologiczną. Pacjenci mieli złożone historie choroby i często wcześniejsze terapie. Ponieważ nie dysponowano dopasowaną zdrową tkanką, poziomy białek w każdym guzie porównywano z medianą w całej grupie, aby określić, co uznać za nieprawidłowo wysokie lub niskie. Nawet w tym ostrzejszym układzie 12 z 14 guzów wykazało wyraźne, istotne klinicznie wzorce aktywności szlaków. W dwóch szczegółowych przykładach dane białkowe potwierdziły na poziomie DNA amplifikację genu FGFR2 w raku jelita grubego oraz utratę hamulca mTOR w raku wątroby, silnie wspierając rozważenie przez Komisję leków blokujących FGFR lub hamujących mTOR. Ogólnie wyniki DigiWest zgadzały się z kluczowymi czynnikami genetycznymi i sugerowały cele lekowe w większości ocenianych przypadków.
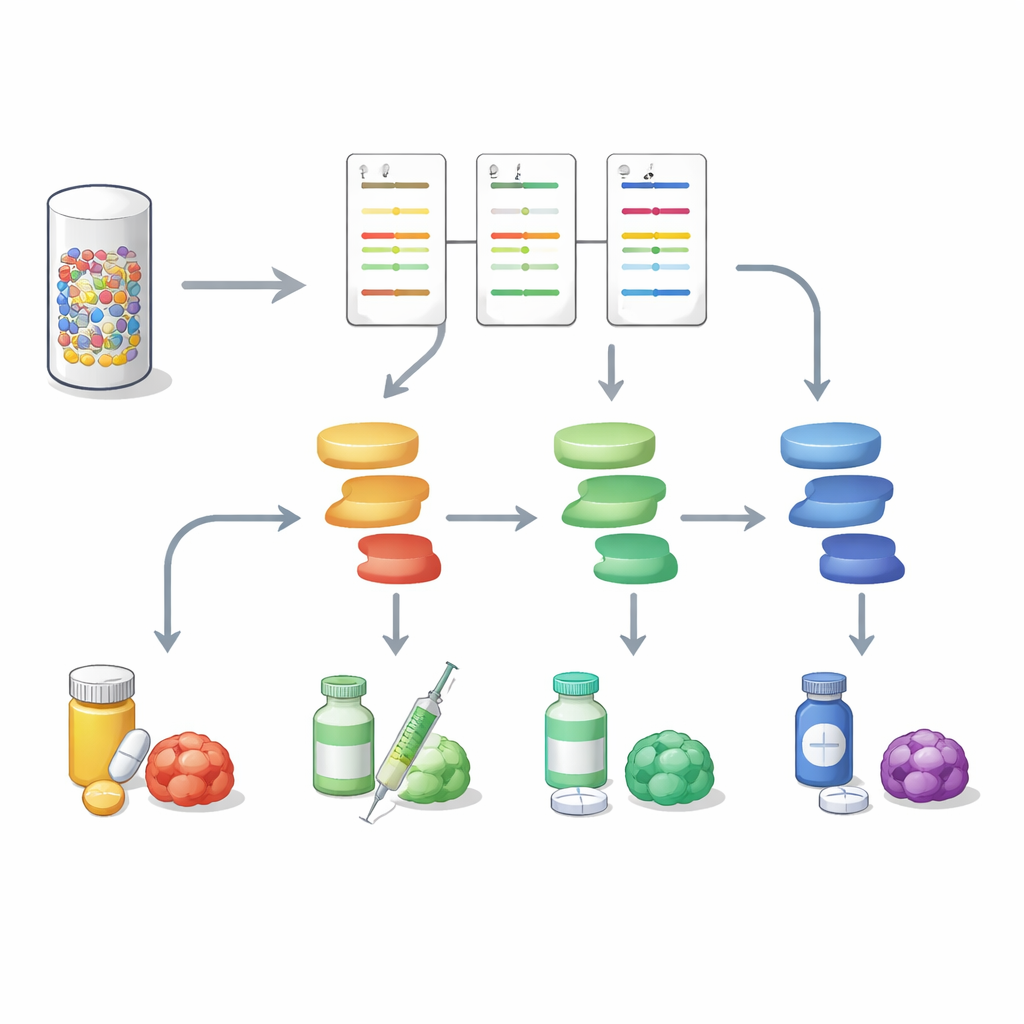
W stronę pełniejszych portretów nowotworów
Praca ta pokazuje, że analizowanie sygnalizacji białkowej równolegle do sekwencjonowania DNA może dostarczyć bogatszego i bardziej użytecznego obrazu nowotworów przewodu pokarmowego. Przekształcając maleńką biopsję w mapę aktywności wielu szlaków, DigiWest pomaga rozróżnić, które molekularne przełączniki są rzeczywiście włączone w danym raku i które leki mogą je najlepiej trafić, a także może sygnalizować pojawiające się drogi oporności. Choć potrzebne są większe badania, podejście to oferuje praktyczny sposób wprowadzenia wysokozawartościowego profilowania białek do codziennej onkologii precyzyjnej i przybliża do planów leczenia dostosowanych do żywego guza każdego pacjenta, a nie tylko jego genetycznego planu działania.
Cytowanie: Stahl, A., Büringer, K., Missios, P. et al. Personalized signaling pathway analysis of gastrointestinal tumors for patient stratification and drug target evaluation using clinically derived core biopsies. npj Precis. Onc. 10, 124 (2026). https://doi.org/10.1038/s41698-026-01304-5
Słowa kluczowe: onkologia precyzyjna, rak przewodu pokarmowego, proteomika, profilowanie biopsji, terapia celowana