Clear Sky Science · pl
Optymalizacja ogniwa elektrolitycznego typu mokrego dla wydajnej produkcji gazu oxywodorowego (HHO): krok w stronę zrównoważonych zielonych rozwiązań energetycznych
Przekształcanie wody w czystsze paliwo
W miarę jak świat szuka sposobów na redukcję zanieczyszczeń bez rezygnacji z wygody silników, jednym z ciekawych pomysłów jest wytwarzanie czystego, dostępnego na żądanie paliwa bezpośrednio z wody. Badanie to analizuje kompaktowe urządzenie, które robi dokładnie to: rozdziela wodę na palną mieszaninę wodoru i tlenu przy użyciu elektryczności. Badacze postawili sobie za cel przeprojektowanie tego typu generatora tak, by marnował znacznie mniej energii na ciepło i produkował więcej użytecznego gazu z każdej jednostki energii elektrycznej. Ich wyniki wskazują praktyczną drogę do bardziej zielonych wzmacniaczy paliwa dla pojazdów i systemów energetycznych na małą skalę.
Dlaczego rozdzielanie wody ma znaczenie
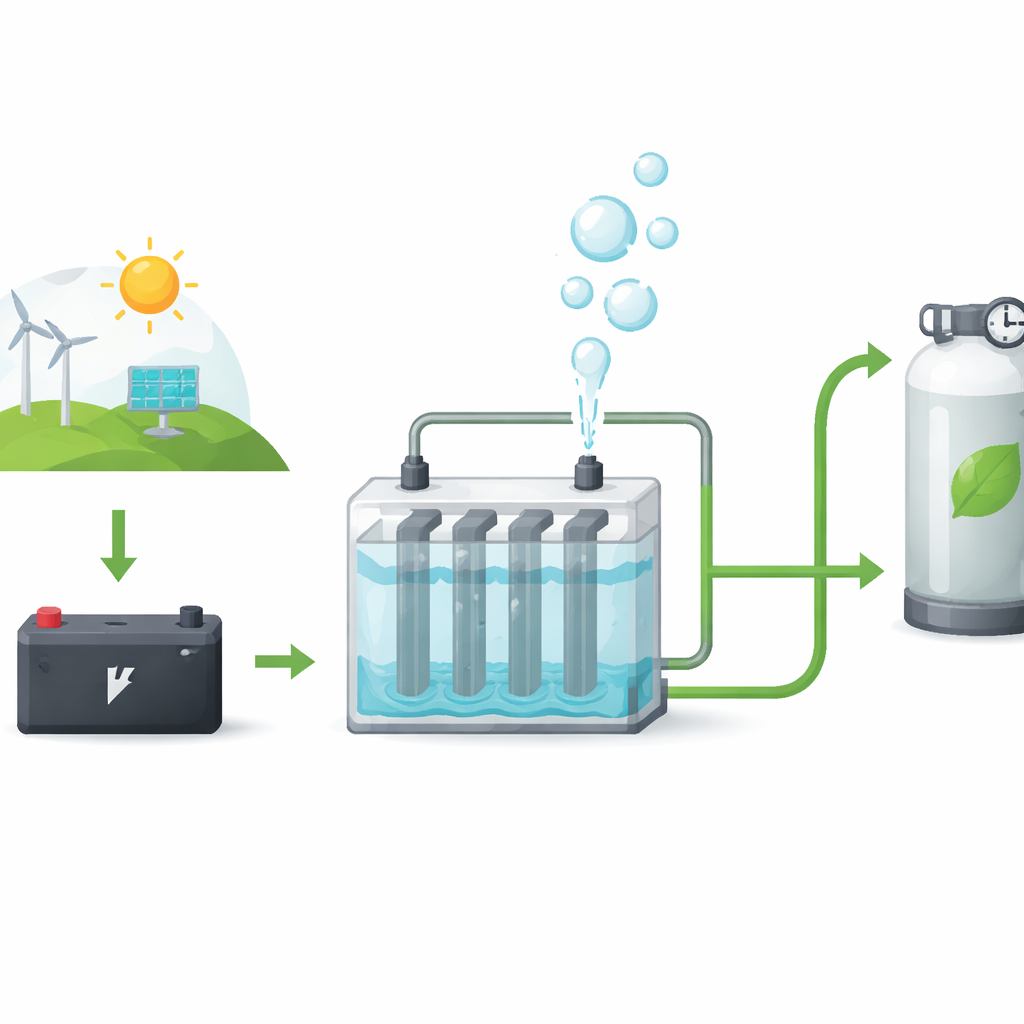
Woda składa się z wodoru i tlenu, a wodór pali się czysto, tworząc z powrotem wodę zamiast sadzistego dymu. Jednak wodór rzadko występuje sam w naturze, więc trzeba go wydzielić przy użyciu energii. Jednym ze sposobów jest elektroliza: przepuszczenie prądu elektrycznego przez wodę, co powoduje jej rozkład na gazy. Gdy gazy utrzymywane są razem w idealnym stosunku dwa do jednego, mieszanka nazywana jest oxywodorem lub HHO. Jest bezbarwna, łatwopalna i może być podawana do silników, by poprawić spalanie. Problemem jest efektywność. Jeśli większość energii elektrycznej zamienia się w niepożądane ciepło zamiast w gaz, proces staje się zbyt kosztowny i marnotrawny. Niniejsze badanie zajmuje się tym problemem poprzez staranne ukształtowanie i ułożenie metalowych płyt, na których zachodzi reakcja, oraz dostrojenie cieczy przewodzącej prąd.
Budowa czterech wersji tego samego pomysłu
Zespół zbudował cztery niemal identyczne urządzenia rozdzielające wodę, nazwane Alpha, Beta, Gamma i Delta. Wszystkie używały stalowych płyt ułożonych w zbiorniku wypełnionym wodą zawierającą niewielką ilość wodorotlenku potasu, soli ułatwiającej przewodzenie prądu przez ciecz. Płyty były okablowane tak, że niektóre pełniły rolę elektrod dodatnich i ujemnych, podczas gdy inne znajdowały się między nimi jako powierzchnie „neutralne”, które również wspomagały reakcję. Badacze zmieniali trzy elementy: wielkość każdej płyty, liczbę płyt dodatnich i ujemnych oraz czy ciecz zawierała niższe czy wyższe stężenie rozpuszczonej soli. Następnie zasili przygotowane urządzenia z akumulatora 12‑woltowego i mierzyłili wydajność gazu, pobór mocy, temperaturę i ogólną efektywność w czasie.
Co wyróżniało najlepszy projekt
Jeden projekt, Delta, wyraźnie przewyższał pozostałe. Wykorzystywał większe płyty (o dwa razy większym boku niż mniejsze wersje), większą liczbę płyt pod napięciem i obszerną objętość elektrolitu. To połączenie rozłożyło prąd elektryczny na szerszej powierzchni, co złagodziło mikroskopijne bariery zwykle spowalniające reakcję i zmniejszyło lokalne gorące punkty. Większy zbiornik cieczy działał też jak bufor termiczny, pochłaniając ciepło i zapobiegając gwałtownemu wzrostowi temperatury. W efekcie Delta produkowała około 3,4 litra gazu HHO na minutę, osiągając ogólną sprawność bliską 60%, co oznacza, że duża część dostarczonej energii elektrycznej pozostawała w wiązaniach chemicznych wodoru zamiast jako stratne ciepło. Mniejsze konstrukcje, zwłaszcza Beta, pracowały goręcej i marnowały znaczną część zasilania na podgrzewanie cieczy zamiast na produkcję gazu.

Równoważenie mocy, ciepła i wydajności gazu
Innym istotnym pokrętłem była siła roztworu soli. Podwojenie stężenia wodorotlenku potasu ułatwiło przemieszczanie ładunków elektrycznych przez wodę, więc każda konstrukcja pobierała więcej prądu i produkowała więcej gazu. Jednak pojawił się kompromis: większy prąd oznaczał także więcej nagrzewania. Tylko konstrukcje z większymi płytami, Gamma i szczególnie Delta, potrafiły przekuć wyższy prąd w lepszą ogólną efektywność zamiast nadmiaru ciepła. Osiągnęły to dzięki połączeniu niskiego oporu elektrycznego, dużej aktywnej powierzchni, na której pęcherzyki mogły formować się i odrywać, oraz wystarczającej objętości cieczy do odprowadzania ciepła. W tych przypadkach, wraz ze wzrostem prądu, ilość energii potrzebnej na jednostkę objętości gazu faktycznie malała — znak, że urządzenie pracowało w optymalnym punkcie, gdzie konstrukcja i warunki pracy wzajemnie się wzmacniały.
Od urządzenia laboratoryjnego do pomocnika w świecie rzeczywistym
Badacze porównali swój najlepszy projekt z wcześniejszymi generatorami HHO oraz z komercyjnymi systemami wodorowymi. Układ Delta dorównywał lub przewyższał wiele wcześniej opisywanych urządzeń, pozostając przy tym prosty i stosunkowo niedrogi, z częściami kosztującymi nieco ponad dwieście dolarów. W przeciwieństwie do przemysłowych zakładów produkujących wodór, wytwarza on gotową do spalania mieszankę wodoru i tlenu przy niskim ciśnieniu, co czyni go odpowiednim do bezpośredniego użycia jako wzmacniacz spalania w silnikach lub jako sposób lokalnego magazynowania nadmiaru energii słonecznej. Badanie pokazuje, że uważne dobranie wielkości płyt, ich ułożenia i chemii cieczy może przekształcić podstawowe ogniwo rozdzielające wodę w znacznie wydajniejsze narzędzie. Dla laika kluczowe przesłanie jest takie, że przemyślana geometria i dobra kontrola termiczna mogą zamienić codzienną substancję — wodę — w praktyczniejszego, czystszego partnera przyszłych systemów energetycznych.
Cytowanie: Fayez, N.H.A., Qenawy, M., Mustafa, H.M.M. et al. Optimization of a wet-cell electrolyzer for efficient oxyhydrogen (HHO) gas production: a step towards sustainable green energy solutions. Sci Rep 16, 12374 (2026). https://doi.org/10.1038/s41598-026-45418-z
Słowa kluczowe: oxywodór, ogniwo elektrolityczne typu mokrego, zielony wodór, elektroliza wody, wzmacniacz paliwa silnikowego