Clear Sky Science · pl
Naturalna pektyna o niskim stopniu metoksylacji wyekstrahowana z koszy słonecznika jako wydajny biosorbent do usuwania ołowiu
Przekształcanie odpadów rolniczych w środek oczyszczający wodę
Zanieczyszczenie wody pitnej ołowiem stanowi poważne zagrożenie na całym świecie, a usuwanie śladowych ilości rozpuszczonego ołowiu jest technicznie trudne i kosztowne. W tym badaniu badacze proponują niespodziewanego sojusznika w walce z ołowiem: rodzaj naturalnego cukru żelującego, zwanego pektyną, wyekstrahowanego nie z owocowych skórek, jak zwykle, lecz z odrzuconych koszy słonecznika. Poprzez staranne dostrojenie procesu ekstrakcji pokazują, że ta pektyna może działać jak potężna gąbka na ołów w wodzie, wskazując drogę do przekształcenia odpadów rolniczych w niskokosztowy, zrównoważony materiał do oczyszczania wody.
Dlaczego ołów w wodzie trudno usunąć
Jony ołowiu w wodzie są niebezpieczne nawet przy bardzo niskich stężeniach, ponieważ kumulują się w organizmie i są trudne do usunięcia. Standardowe metody uzdatniania—takie jak strącanie chemiczne, filtracja membranowa czy wymiana jonowa—często wymagają skomplikowanego sprzętu, dużego zużycia energii lub generują wtórne odpady. Adsorpcja, czyli proces, w którym materiał stały wychwytuje zanieczyszczenia z wody i utrzymuje je na swojej powierzchni, jest znacznie prostsza i może być bardzo skuteczna. Wyzwanie polega na znalezieniu tanich, odnawialnych materiałów, które mocno i w dużych ilościach wiążą ołów, bez konieczności stosowania intensywnej obróbki chemicznej.
Nowe życie koszy słonecznika
Kosze słonecznika, zwykle pozostawiane na polu lub wyrzucane po usunięciu nasion, zawierają duże ilości pektyny. Cząsteczki pektyny są bogate w specyficzne grupy chemiczne zdolne do wiązania jonów metali. Zespół porównał trzy pektyny: jedną wyekstrahowaną z koszy słonecznika w stosunkowo łagodnej temperaturze (LHP), jedną wyekstrahowaną w wyższej temperaturze przez dłuższy czas (AHP) oraz typową komercyjną pektynę cytrusową (CP). Silniejsze podgrzewanie koszy słonecznika pozwoliło uzyskać AHP o krótszych, bardziej elastycznych łańcuchach i wielu odsłoniętych miejscach wiążących metale. W przeciwieństwie do tego, komercyjna pektyna cytrusowa miała więcej swoich miejsc wiążących zablokowanych małymi „czapkami” chemicznymi, co zmniejszało jej zdolność do utrzymywania ołowiu.

Jak struktura kontroluje zdolność chwytania ołowiu
Choć pektyny ze słonecznika i pektyna cytrusowa miały w przybliżeniu podobne podstawowe jednostki budulcowe, różniły się w dwóch kluczowych aspektach, które decydują o skuteczności pochłaniania ołowiu: liczbą dostępnych aktywnych miejsc oraz łatwością dostępu do tych miejsc. Obie pektyny ze słonecznika naturalnie wykazywały niski poziom chemicznego „blokowania”, pozostawiając wiele ujemnie naładowanych miejsc otwartych na wiązanie ołowiu. Jednak AHP miała znacznie krótsze łańcuchy niż LHP, co zmniejszało splątywanie się między cząsteczkami i otwierało strukturę. Eksperymenty wykazały, że AHP może zatrzymać prawie 296 miligramów ołowiu na gram pektyny—około jedną czwartą więcej niż LHP i trzy czwarte więcej niż pektyna cytrusowa. Badania zależności od pH, temperatury i początkowego stężenia ołowiu potwierdziły, że AHP konsekwentnie przewyższała pozostałe dwa materiały.
Obserwowanie wiązania ołowiu i przemiany sieci
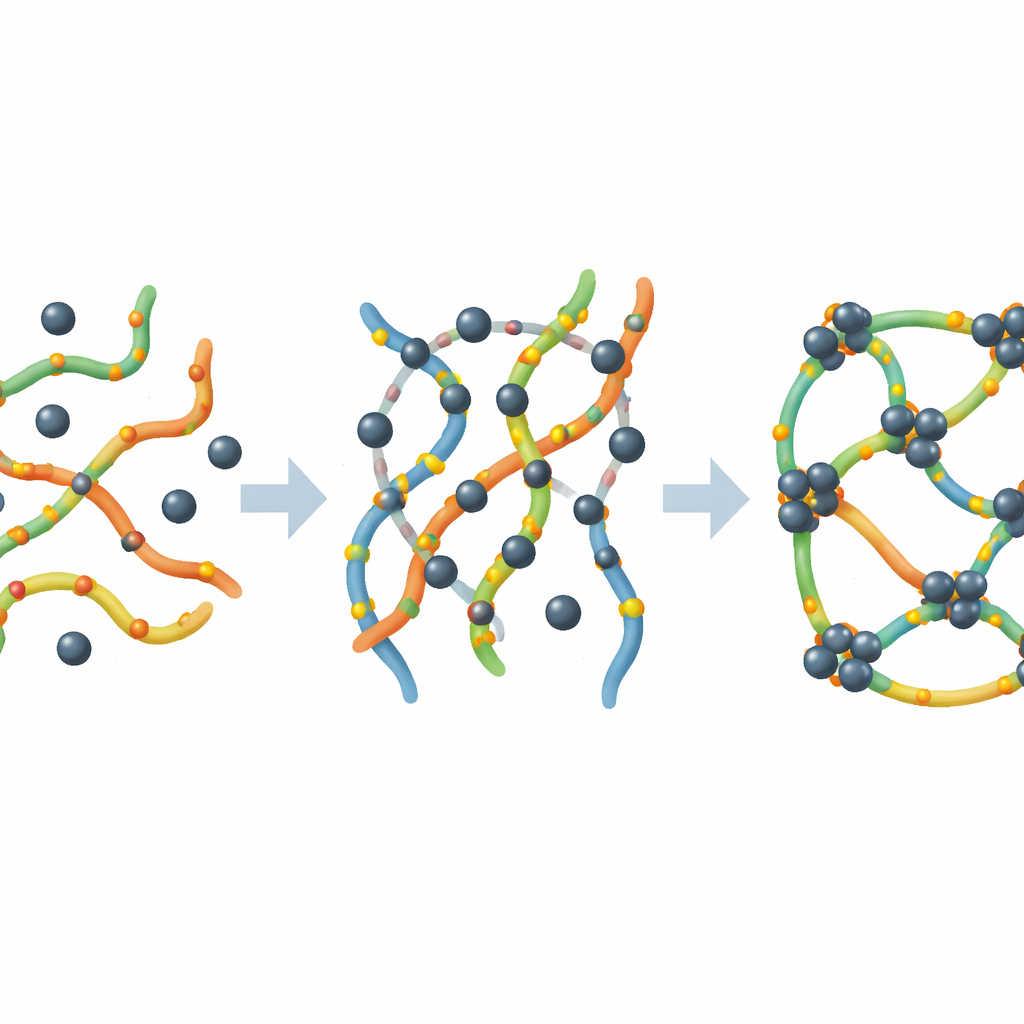
Aby zrozumieć, co dzieje się na poziomie mikroskopowym, badacze śledzili interakcję ołowiu z pektyną przy użyciu kilku zaawansowanych technik. Spektroskopia i analiza powierzchni wykazały, że ołów przyłącza się bezpośrednio do grup zawierających tlen na łańcuchach pektyny, tworząc silne wiązania chemiczne, a nie tylko słabe oddziaływania. Obrazy mikroskopowe ujawniły, że w miarę wiązania ołowiu łańcuchy pektyny reorganizują się, tworząc gęstszą, bardziej połączoną sieć, podobną do miękkiego żelu. Pomiary powierzchni i struktury porów potwierdziły, że ta sieć faktycznie staje się bardziej wewnętrznie teksturowana w trakcie zatrzymywania ołowiu, tworząc dodatkowe wewnętrzne powierzchnie i drobne pory, które pomagają utrzymać jeszcze większe ilości metalu.
Od mechanizmu w laboratorium do potencjału w praktyce
Badanie przetestowało również, jak inne powszechne jony w wodzie, takie jak wapń i glin, konkurują z ołowiem o miejsca wiążące na pektynie. Jony wielowartościowe zakłócały wiązanie najbardziej, co pokazuje, że warunki rzeczywistych ścieków będą miały znaczenie dla wydajności. Mimo to pektyna ze słonecznika wypadła korzystnie w porównaniu z wieloma chemicznie modyfikowanymi lub kompozytowymi pektynami opisywanymi we wcześniejszych pracach, mimo że została otrzymana stosunkowo prostą ekstrakcją. Autorzy sugerują, że kolejnym krokiem jest osadzenie tej zoptymalizowanej pektyny w stałych granulkach, żelach lub cząstkach magnetycznych, które można łatwo oddzielać i ponownie wykorzystywać w systemach uzdatniania.
Co to oznacza dla bezpieczniejszej wody
Mówiąc prosto, badacze odkryli, że sposób obróbki cieplnej koszy słonecznika podczas ekstrakcji pektyny może przekształcić produkt uboczny rolniczy w szczególnie skuteczną gąbkę na ołów. Podgrzewanie w wyższej temperaturze przez dłużej skraca łańcuchy pektyny na tyle, by je rozplątać i odsłonić więcej „łapek” do chwytania ołowiu, bez niszczenia materiału. Ta starannie dobrana pektyna tworzy elastyczną, porowatą sieć, która unieruchamia ołów poprzez silne wiązania chemiczne. Pokazując, że same warunki ekstrakcji mogą optymalizować zarówno chemię, jak i fizyczną otwartość tej sieci, praca wskazuje praktyczną, bezodczynnikową strategię przekształcania odpadów roślinnych w skuteczne, bardziej ekologiczne narzędzia do usuwania metali ciężkich z wody.
Cytowanie: Peng, X., Gong, Q., Gao, R. et al. Natural low methoxyl pectin extracted from sunflower heads serves as an efficient biosorbent for lead removal. Sci Rep 16, 11557 (2026). https://doi.org/10.1038/s41598-026-40672-7
Słowa kluczowe: usuwanie ołowiu, pektyna ze słonecznika, biosorbent, oczyszczanie wody, ponowne wykorzystanie odpadów rolniczych