Clear Sky Science · pl
Wydajność podgrup komercyjnego modelu cyfrowej tomosyntezy piersi w wykrywaniu raka piersi
Dlaczego to ma znaczenie dla kobiet i rodzin
Skryning raka piersi ratuje życie, ale żaden test nie jest doskonały. Lekarze coraz częściej sięgają po sztuczną inteligencję (AI), aby pomóc w odczycie złożonych trójwymiarowych zdjęć rentgenowskich piersi. To badanie szczegółowo przeanalizowało, jak szeroko stosowany system AI radzi sobie w różnych grupach pacjentek i w odniesieniu do różnych zmian w piersiach, ujawniając miejsca, w których narzędzie działa dobrze, i te, w których ma trudności. 
Bliższe spojrzenie na nowy rodzaj mammografii
Tradycyjne mammogramy to płaskie, dwuwymiarowe zdjęcia rentgenowskie. W wielu placówkach stosuje się dziś cyfrową tomosyntezę piersi — skan przypominający 3D złożony z wielu cienkich warstw piersi. Może ona ujawnić nowotwory, które mogłyby być ukryte w nakładającej się tkance, szczególnie w gęstych piersiach, ale obrazy zajmują więcej czasu przy odczycie i wciąż mogą pominąć drobne ogniska wapnienia, które sygnalizują wczesną chorobę. Z tego powodu firmy opracowały narzędzia AI do oznaczania podejrzanych obszarów dla radiologów. Dotychczas większość ocen tych narzędzi koncentrowała się na ogólnej dokładności, a nie na tym, jak zachowują się wobec konkretnych pacjentek czy typów guzów.
Ogromny test w warunkach rzeczywistych narzędzia wspomagającego AI
Naukowcy z Emory University zbadali komercyjny system AI o nazwie INSIGHT DBT, stosowany na obrazach 3D piersi z ponad 167 000 badań przesiewowych u ponad 61 000 kobiet. Porównali oceny AI z rzeczywistymi wynikami, rozdzielając badania wyraźnie negatywne, biopsje łagodne i potwierdzone raki. Główne pytanie brzmiało, jak dobrze AI rozróżnia nowotwory wykryte podczas rutynowego skryningu od badań, które okazały się nie nowotworowe. W całej badanej populacji AI wykazała silną wydajność, trafnie klasyfikując badania nowotworowe i nienowotworowe w większości przypadków i potwierdzając wyniki z pierwotnej oceny regulacyjnej. Wyniki były podobne w różnych grupach wiekowych, rasowych i etnicznych, co jest istotnym odkryciem pod względem sprawiedliwości opieki.
Gdzie AI błyszczy, a gdzie zawodzi
Gdy zespół przeanalizował szczegóły, wyłoniły się kluczowe wzorce. AI najlepiej radziła sobie z wykrywaniem raków inwazyjnych, które tworzą zwarte masy lub powodują widoczne zniekształcenia tkanki piersi; większość takich przypadków została prawidłowo oznaczona. Była mniej niezawodna w przypadku nowotworów ograniczonych do przewodów mlecznych, znanych jako choroba in situ, oraz w przypadku nowotworów ujawniających się głównie jako drobne skupiska wapnieniowe. W tych wczesnych zmianach system przeoczył prawie połowę przypadków, a jego ogólna dokładność spadła. Gęsta tkanka piersi również nieco obniżała wydajność, prawdopodobnie dlatego, że gęsta tkanka może ukrywać subtelne objawy. 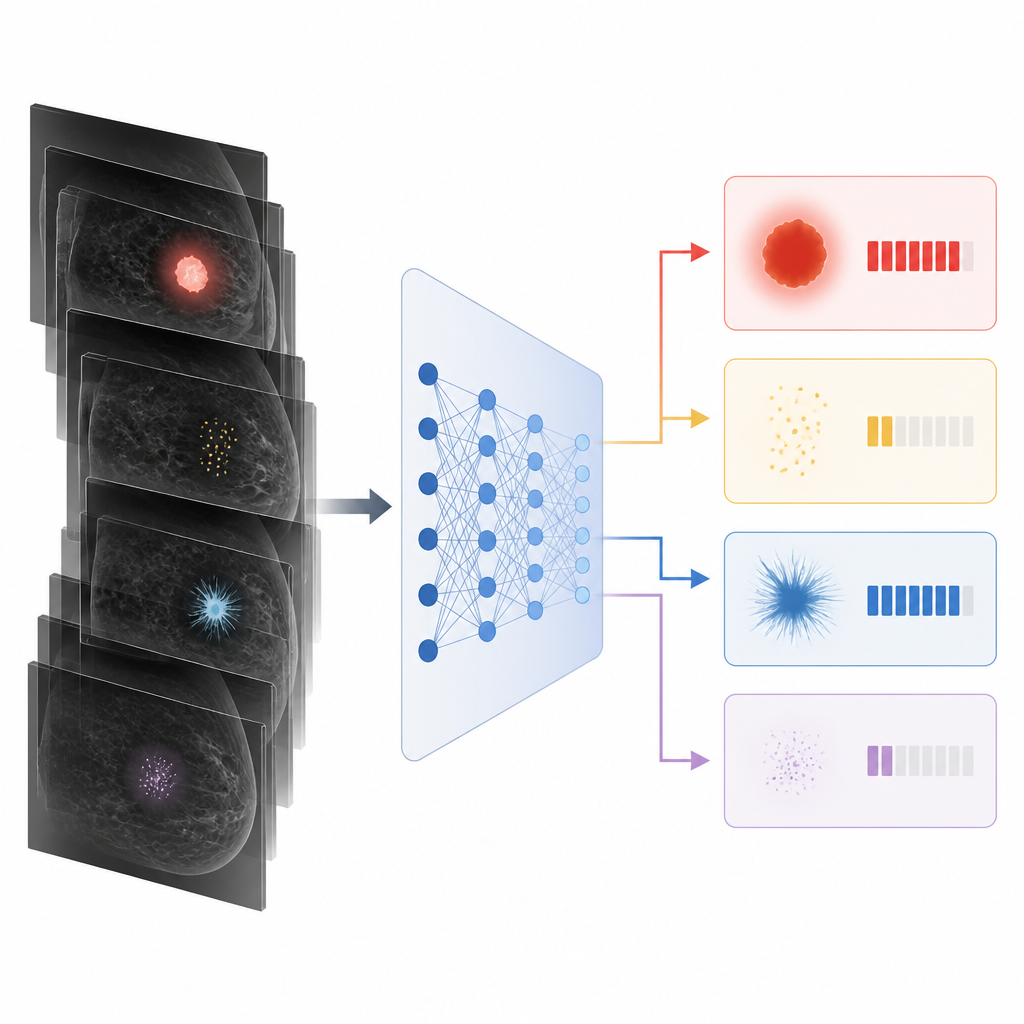
Co ujawniają wzorce ocen
Analizując pełen zakres ocen AI zamiast tylko decyzji „tak” lub „nie”, badacze zauważyli, że badania z bardziej niepokojącą patologią miały tendencję do otrzymywania wyższych ocen. Zmiany łagodne i niskiego ryzyka zwykle oceniano nisko, natomiast raki inwazyjne skupiały się na wysokim końcu skali. Jednak niektóre niezłośliwe zniekształcenia otrzymywały wysokie oceny, co prowadziło do fałszywych alarmów, a niektóre rzadkie podtypy raka inwazyjnego i zmiany in situ były niedoszacowane. System przypisał nawet wysokie oceny około jednej trzeciej raków, które pojawiły się między rutynowymi badaniami przesiewowymi, co sugeruje, że czasami dostrzega wskazówki, które umykają ludziom, choć rzeczywisty wpływ tego zjawiska w praktyce pozostaje niepewny.
Implikacje dla pacjentek i klinicystów
Dla czytelnika niebędącego specjalistą wniosek jest taki, że to narzędzie AI może istotnie wspomóc radiologów w odczycie złożonych obrazów 3D piersi, bez widocznych różnic między głównymi grupami demograficznymi. Nie jest jednak samodzielnym detektorem raka. Jest mniej godne zaufania w przypadku najwcześniejszych nowotworów opartych na wapnieniu i przy bardzo gęstych piersiach, i nadal może wywoływać niepotrzebne dalsze badania w niektórych przypadkach łagodnych. Autorzy argumentują, że zrozumienie tych mocnych stron i ślepych punktów jest niezbędne przed poleganiem na AI w codziennym skryningu, aby lekarze mogli używać jej jako ostrożnego partnera, a nie zastępstwa.
Cytowanie: Brown-Mulry, B., Isaac, R.S., Lee, S.H. et al. Subgroup performance of a commercial digital breast tomosynthesis model for breast cancer detection. Nat Commun 17, 4249 (2026). https://doi.org/10.1038/s41467-026-70637-3
Słowa kluczowe: skryning raka piersi, cyfrowa tomosynteza piersi, medyczne AI, mammografia, DCIS