Clear Sky Science · pl
Przestrzenna kartografia grasicy człowieka umożliwia geopozycjonowanie czynników transkrypcyjnych linii w rzadkich mimetycznych komórkach nabłonka grasicy
Dlaczego mapowanie małego narządu ma znaczenie
Grasica to mały organ schowany za mostkiem, a mimo to w subtelny sposób kształtuje układ odpornościowy, szkoląc nowo powstałe komórki T, by rozpoznawały zagrożenia, nie atakując własnych tkanek. W miarę jak ludzie żyją dłużej, a choroby związane z układem odpornościowym stają się częstsze, naukowcy muszą poznać to „miejsce szkolenia” w najdrobniejszych szczegółach. To badanie buduje szczegółową przestrzenną „mapę” grasicy ludzkiej płodów i małych dzieci, ujawniając, jak ułożone są różne sąsiedztwa komórkowe i jak rzadkie, wyspecjalizowane komórki pomagają zapobiegać autoimmunizacji.
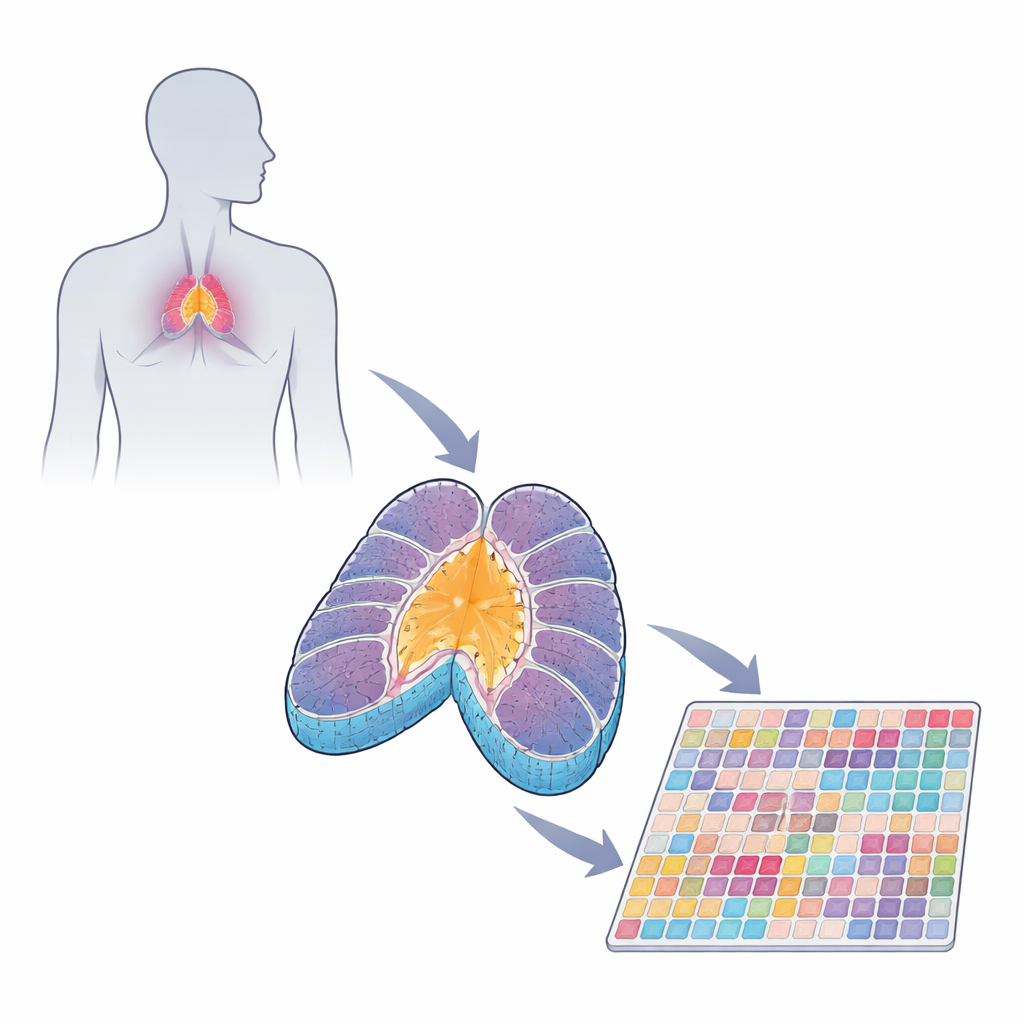
Grasica jako szkoła szkoląca układ odpornościowy
Komórki T zaczynają życie jako niedojrzałe rekruty przybywające z wątroby płodowej lub szpiku kostnego. W grasicy przechodzą uporządkowaną podróż. Zewnętrzny obszar, zwany korą, wypełniony jest rozwijającymi się komórkami T oraz komórkami nabłonka wspierającymi, które sprawdzają, czy każda komórka T potrafi rozpoznać molekularne znaki „ja”. Te, które przechodzą test, przechodzą do wewnętrznego obszaru, rdzenia, gdzie odbywa się kolejna runda selekcji usuwająca komórki reagujące zbyt silnie na własne antygeny. Ten proces, zwany tolerancją centralną, zapobiega temu, by zdrowy układ odpornościowy atakował normalne narządy, takie jak trzustka, skóra czy mózg.
Budowanie atlasa grasicy o wysokiej rozdzielczości
Poprzednie badania profilowały komórki grasicy, sekwencjonując je pojedynczo po wyizolowaniu z tkanki. To ujawniło głównych graczy, ale nie mówiło, gdzie się znajdują ani jak są zorganizowani. W niniejszej pracy autorzy zastosowali technikę zwaną transkryptomiką przestrzenną (Stereo‑seq), która odczytuje tysiące genów bezpośrednio z nieuszkodzonych przekrojów tkanki, wraz z wysoce multiplexowanym obrazowaniem białek. Zastosowali te narzędzia do ludzkich grasic płodów w wieku 13–18 tygodni ciąży oraz grasic pediatrycznych od 7 tygodnia do 6 lat. Łącząc dane genowe i białkowe, mogli wyznaczyć klasyczne regiony, takie jak kora, rdzeń i przegrody włókniste, a następnie podzielić je na mniejsze „niche” o odmiennych mieszankach komórek T, komórek nabłonkowych, fibroblastów i innych komórek układu odpornościowego.
Odkodowywanie sygnałów kształtujących los komórek T
Dzięki temu atlasowi zespół zbadał, jak komórki komunikują się za pomocą cząsteczek sygnałowych. W korze znaleźli szlaki wspierające utrzymanie fibroblastów i kierowanie niedojrzałymi komórkami T, w tym sygnały obejmujące białko CXCL12 i jego receptor na komórkach T. Te wskazówki pomagają młodym komórkom T przemieszczać się przez korę i przechodzić pierwsze etapy selekcji. W rdzeniu dominował inny zestaw sygnałów, takich jak chemokiny przyciągające dojrzałe komórki T do odpowiednich obszarów oraz czynniki związane z prezentacją antygenów i śmiercią komórkową. Razem te obwody zapewniają, że komórki T nie tylko uczą się, jak wygląda „ja”, lecz także są eliminowane, gdy reagują zbyt agresywnie.
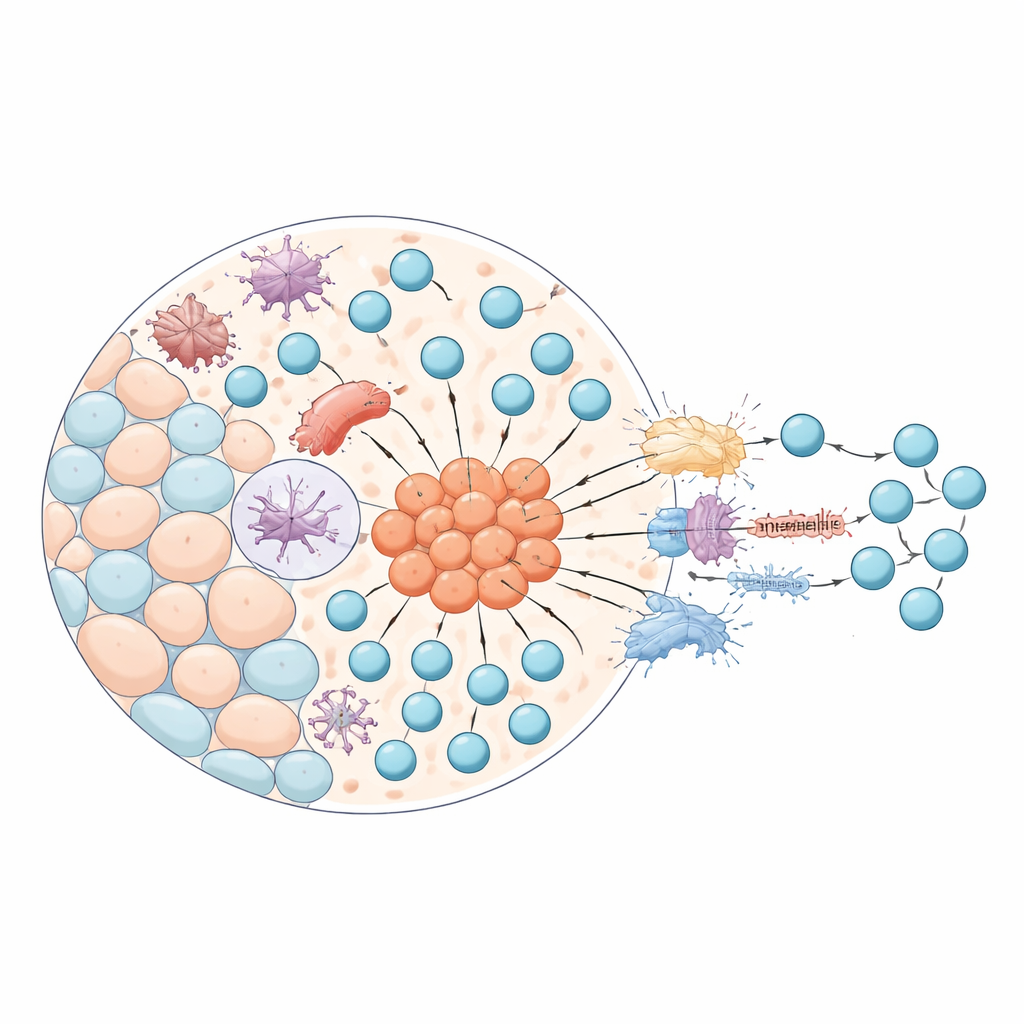
Rzadkie komórki mimetyczne i ich przełączniki kontrolne
Głównym punktem badania jest mało znana grupa komórek nabłonka grasicy, które zachowują się jak podróbki komórek pochodzących z innych narządów. Te „mimetyczne” komórki uruchamiają programy genowe zwykle używane przez komórki mięśniowe, nerwowe czy gruczołowe, pozwalając grasicy prezentować szeroki katalog własnych cząsteczek rozwijającym się komórkom T. Korzystając z mapy przestrzennej, badacze systematycznie szukali czynników transkrypcyjnych — przełączników kontrolujących geny — aktywnych w komórkach nabłonkowych zlokalizowanych w rdzeniu. Odkryli 70 takich czynników powiązanych z komórkami mimetycznymi, w tym znane regulatory jak AIRE i FEZF2, oraz dziesiątki wcześniej niedocenianych kandydatów. Te komórki są niezwykle rzadkie, stanowią mniej niż pół procenta tkanki, jednak skupiają się w wyspecjalizowanych ogniskach w pobliżu struktur zwanych ciałkami Hassalla.
Co ten atlas ujawnia o tolerancji immunologicznej
Nakładając ekspresję genów, wzorce białkowe i lokalizacje komórek, badanie pokazuje, że mimetyczne komórki nabłonkowe występują w ciasnych sąsiedztwach bogatych w komórki prezentujące antygeny i dojrzałe komórki T. Ich czynniki transkrypcyjne powiązane są z programami rozwojowymi wielu narządów — mózgu, mięśni, gruczołów dokrewnych i innych — co sugeruje, że każdy typ komórki mimetycznej wyspecjalizowany jest w reprezentowaniu innej części „biblioteki ja” organizmu. Praca wskazuje też na ograniczenia techniczne: obecne metody przestrzenne nie potrafią jeszcze odtworzyć granic każdej pojedynczej komórki w tak zatłoczonym narządzie, lecz autorzy zbliżają się do tego, używając chipów o wyższej rozdzielczości i zintegrowanych danych białkowych.
Jak to posuwa naprzód nasze rozumienie zdrowia i choroby
Dla laika kluczowy przekaz jest taki, że grasica to nie tylko prosty filtr, lecz precyzyjnie strefowany krajobraz, w którym rzadkie, wysoko wyspecjalizowane komórki pomagają uczyć komórki T tolerancji poprzez naśladowanie wielu innych tkanek. To badanie dostarcza szczegółowej mapy tego krajobrazu we wczesnym życiu człowieka, lokalizuje, gdzie żyją te komórki mimetyczne, i identyfikuje przełączniki genowe kształtujące ich tożsamość. Taka wiedza tworzy podstawę dla przyszłych badań nad tym, dlaczego tolerancja immunologiczna czasem zawodzi, przyczyniając się do chorób autoimmunologicznych, i może ostatecznie służyć do opracowania strategii odbudowy lub manipulacji grasicy w starzeniu, infekcji czy nowotworach.
Cytowanie: Kamaraj, U.S., Chen, Y., Lei, J. et al. Spatial cartography of human thymus enables the geopositioning of lineage transcription factors in rare mimetic thymic epithelial cells. Nat Commun 17, 3721 (2026). https://doi.org/10.1038/s41467-026-68596-w
Słowa kluczowe: grasica, rozwój komórek T, transkryptomika przestrzenna, tolerancja immunologiczna, komórki nabłonkowe grasicy