Clear Sky Science · pl
FBXO6 reguluje migrację i inwazję raka jelita grubego poprzez ubikwitynację ITGB1 i sygnalizację w dół szlaku
Dlaczego to badanie ma znaczenie
Rak jelita grubego jest jednym z najczęstszych i najbardziej śmiertelnych nowotworów na świecie, głównie dlatego, że bardzo często rozprzestrzenia się z jelita do odległych narządów. Gdy dochodzi do tego rozproszenia, czyli przerzutów, wskaźniki przeżycia gwałtownie spadają. To badanie odkrywa wbudowaną komórkową „hamulcową”, która pomaga powstrzymać komórki raka jelita przed odrywaniem się i inwazją nowych tkanek, oraz pokazuje, że wzmocnienie tego hamulca — albo jego naprawa, gdy zawodzi — mogłoby otworzyć nowe drogi leczenia i prognozowania.
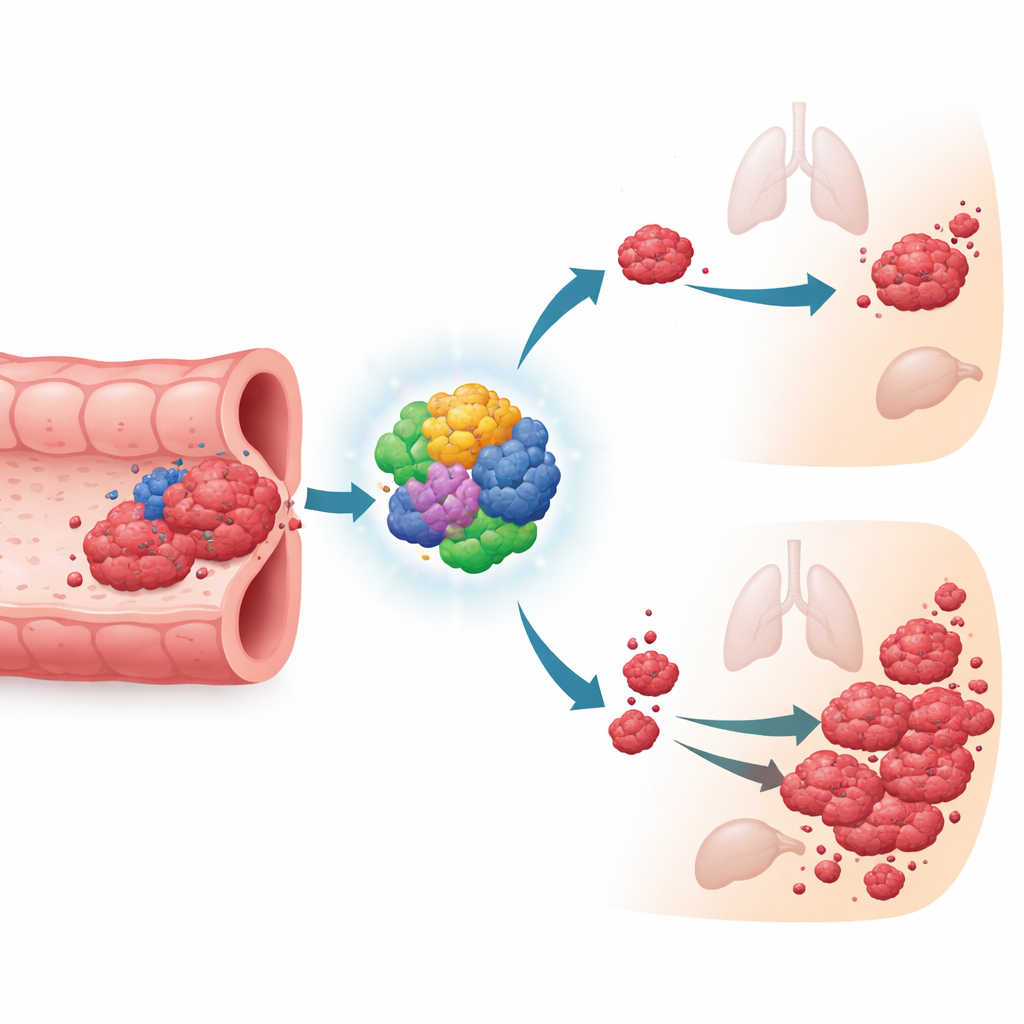
Wbudowany hamulec agresywności guza
Naukowcy skupili się na białku o nazwie FBXO6, będącym częścią komórkowego mechanizmu utylizacji odpadów, które znakuję niepożądane białka do zniszczenia. Przeszukując duże bazy danych pacjentów, stwierdzili, że osoby z rakami jelita grubego wykazujące wyższe poziomy FBXO6 miały tendencję do dłuższego przeżycia i rzadszych nawrotów. Co interesujące, ilość FBXO6 malała w bardziej zaawansowanych guzach, co sugeruje, że komórki nowotworowe mogą postępować częściowo poprzez wyciszanie tego ochronnego czynnika.
Obserwacja poruszających się komórek nowotworowych
Aby zrozumieć, co FBXO6 faktycznie robi, zespół manipulował jego poziomami w dwóch ludzkich liniach komórek raka jelita grubego. Gdy wymuszono u komórek większą produkcję FBXO6, tworzyły one mniej kolonii, poruszały się wolniej po płytce i miały trudności z przeciskaniem się przez żel imitujący otaczającą tkankę. Gdy zredukowano poziom FBXO6, następowało odwrotne zjawisko: komórki dzieliły się chętniej, migrowały szybciej i głębiej penetrowały. Te proste, lecz wymowne testy behawioralne wykazały, że FBXO6 działa jako silny inhibitor wzrostu, ruchu i inwazji komórek nowotworowych.
Odnalezienie kluczowego białkowego partnera
Następnie naukowcy postanowili odkryć, które białko jest celem FBXO6, żeby wywierać te efekty. Stosując podejście podobne do łowienia, gdzie FBXO6 służyło jako przynęta, w połączeniu z spektrometrią mas do identyfikacji „upolowanego” białka, wpadli na białko błonowe o nazwie ITGB1. Ta cząsteczka znajduje się na powierzchni komórki i pomaga komórkom nowotworowym chwytać i napinać otoczenie — umiejętność ściśle powiązaną z przerzutami. Dane kliniczne wykazały, że wysoki poziom ITGB1 w raku jelita grubego wiąże się z gorszymi wynikami dla pacjentów. W próbkach guzów od pacjentów ITGB1 był wyraźnie podwyższony w porównaniu z pobliską tkanką normalną, podczas gdy poziomy FBXO6 były stosunkowo niezmienione, co sugeruje, że w rzeczywistych guzach to ITGB1 pełni rolę dominującego sprawcy problemów.
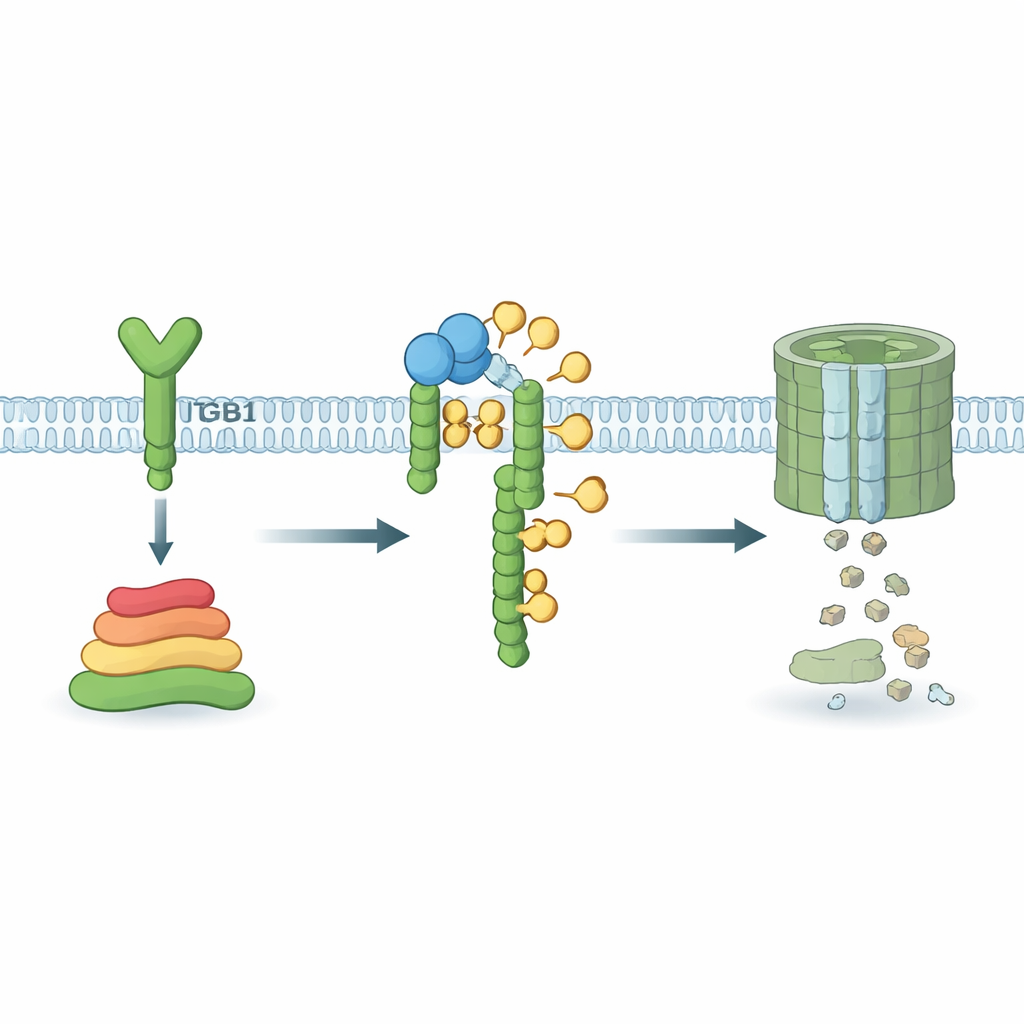
Jak hamulec zakłóca łańcuch sygnału wzrostu
Zagęszczając badania, zespół potwierdził, że FBXO6 fizycznie wiąże się z ITGB1 wewnątrz komórek. FBXO6 rozpoznaje części ITGB1 ozdobione cukrami i przyłącza małe molekularne „znaczki”, które oznaczają ITGB1 do rozdrobnienia przez mechanizm recyklingu białek w komórce. Gdy FBXO6 było obfite, poziomy ITGB1 spadały szybciej, a łańcuch sygnałów wzrostu i przetrwania — często podsumowywany jako szlak FAK–PI3K–AKT–ERK — był przytłumiony. Gdy FBXO6 usunięto lub zmieniono miejsce rozpoznawania cukrów, ITGB1 utrzymywał się dłużej, a ten łańcuch sygnałowy ulegał aktywacji. Dodanie dodatkowego ITGB1 mogło zneutralizować hamujące działanie FBXO6, przywracając silną sygnalizację i agresywne zachowanie, co potwierdza, że ITGB1 jest kluczowym celem.
Testowanie mechanizmu w żywych guzach
Naukowcy przeszli następnie od hodowli komórek do modeli mysich, wszczepiając komórki raka jelita grubego pod skórę. Guzy zaprojektowane do produkcji większej ilości FBXO6 rosły wolniej, wykazywały mniej komórek dzielących się oraz miały niższe poziomy ITGB1 i słabszą sygnalizację w dół szlaku. Guzy z obniżonym poziomem FBXO6 zachowywały się odwrotnie: rosły szybciej i wykazywały nasilone aktywności sygnalizacyjne. Dodatkowe eksperymenty modyfikujące poziomy ITGB1 w tym modelu pokazały, że zwiększenie FBXO6 może przeciwdziałać prozłośliwemu wpływowi ITGB1, wzmacniając ideę, że te dwa białka tworzą funkcjonalną wagę, która kontroluje, jak niebezpieczny staje się guz.
Co to oznacza dla pacjentów
W sumie praca przedstawia FBXO6 jako naturalnego obrońcę przed rozprzestrzenianiem się raka jelita grubego. Poprzez celowanie i usuwanie ITGB1, FBXO6 osłabia potężny łańcuch sygnałów, który normalnie pobudza komórki nowotworowe do wzrostu, migracji i inwazji. Gdy FBXO6 jest niski lub upośledzony, ITGB1 wymyka się tej kontroli, zwiększając prawdopodobieństwo przerzutów. To sugeruje, że poziomy FBXO6 mogłyby pomóc lekarzom w ocenie rokowania, a leki przywracające aktywność FBXO6 — lub bezpośrednio naśladujące jego atak na ITGB1 — mogłyby spowolnić lub zapobiec rozprzestrzenianiu się raka jelita grubego. Ponieważ ITGB1 wiąże się również z opornością na niektóre terapie, wyostrzenie tego komórkowego hamulca mogłoby w efekcie zwiększyć skuteczność istniejących leczeń.
Cytowanie: Ren, N., Cheng, L., Huang, Z. et al. FBXO6 regulates colon cancer migration and invasion via ITGB1 ubiquitination and downstream signaling. Cell Death Dis 17, 324 (2026). https://doi.org/10.1038/s41419-026-08554-y
Słowa kluczowe: rak jelita grubego, przerzuty, ubikwitynacja, integryna beta1, sygnalizacja komórkowa