Clear Sky Science · pl
Barwne sensytyzowane kaskadowe przekazywanie energii dla wzmocnionej luminescencji 1525 nm w silnie domieszkowanych nanopartikelach lantanowców
Bardziej wyraźne widoki wnętrza ciała
Wyraźne oglądanie struktur wewnątrz żywej tkanki bez otwierania jej to jedno z największych wyzwań współczesnej medycyny. Obrazowanie oparte na świetle jest atrakcyjne, ponieważ może być szybkie, łagodne i powtarzalne, ale nasze ciało rozprasza i pochłania światło, przez co głębsze struktury wyglądają na rozmyte i przygaszone. W tej pracy przedstawiono specjalnie zaprojektowane świecące nanocząstki, które jaśniej świecą w „słodkim punkcie” niewidocznej podczerwieni, umożliwiając mapowanie naczyń krwionośnych głęboko pod skórą z wysoką ostrością i kontrastem.
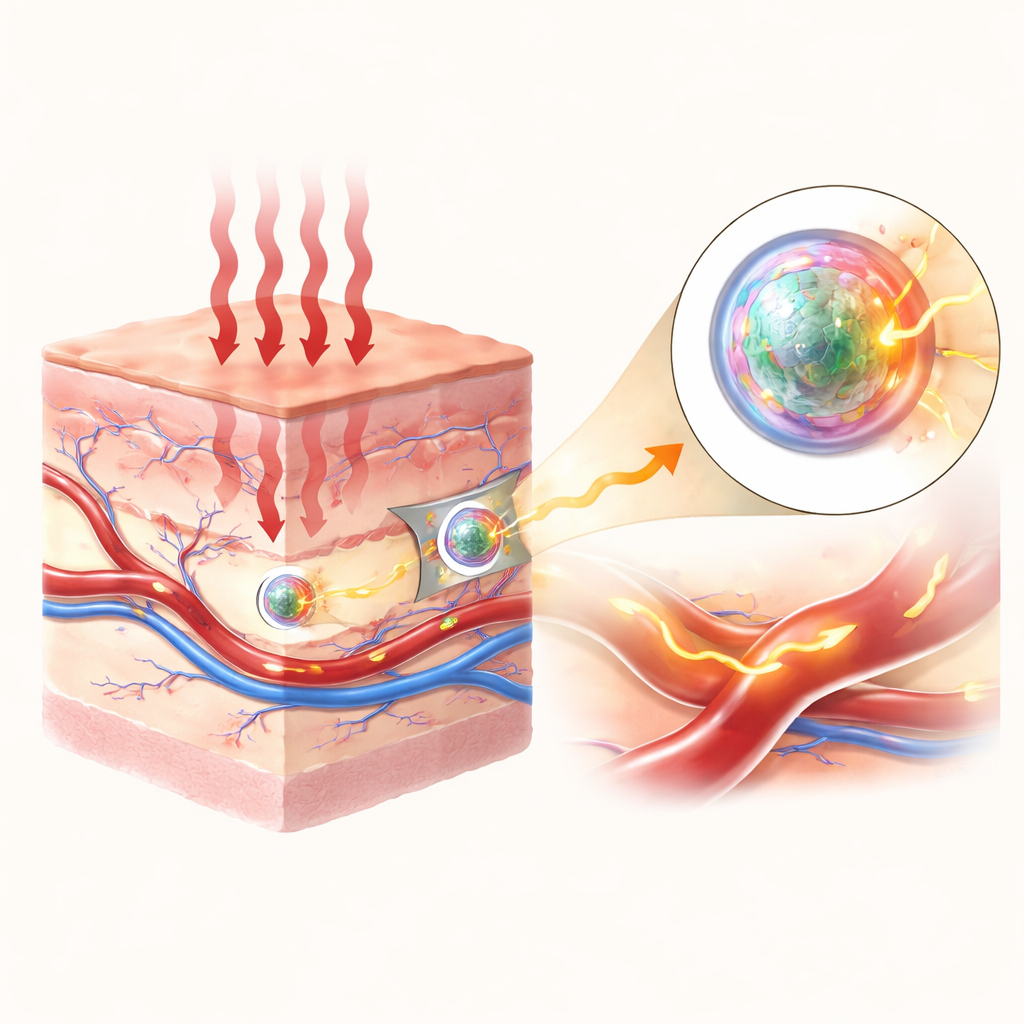
Dlaczego niewidzialne światło ma znaczenie
Większość medycznych kamer pracuje w świetle widzialnym lub bliskiej podczerwieni, ale w tych zakresach światło jest silnie rozpraszane, a same tkanki świecą, dodając niechciane tło. W nieco dłuższych długościach fal, w tzw. drugim oknie bliskiej podczerwieni, rozproszenie i naturalne tło są znacznie mniejsze, więc obrazy mogą być ostrzejsze i sięgać głębiej. Autorzy koncentrują się na wąskim paśmie w tym oknie, około 1525 nanometrów, które jest szczególnie korzystne do wizualizacji naczyń krwionośnych dzięki silnemu sygnałowi na ciemnym tle, gdy tkankę oświetla się powszechnym laserem 808 nm.
Budowanie jaśniejszej nanoskali latarni
W centrum pracy znajdują się maleńkie kryształowe cząstki z lantanowca zwanego erbem, który sam z siebie emituje światło około 1525 nm. Samodzielnie atomy erbu bardzo słabo absorbują padające światło laserowe, więc cząstki słabo świecą. Badacze rozwiązañ ten problem, tworząc warstwową nanocząstkę: rdzeń bogaty w erb otoczony cienką powłoką zawierającą inny lantanowiec, ytterb, o łącznej średnicy poniżej 20 nanometrów. Na powierzchnię przytwierdzili barwnik medyczny znany jako indocyjanina zielona (ICG), który jest wyjątkowo efektywny w absorpcji światła 808 nm.
Przekazywanie energii na skali nanometrowej
Gdy cząsteczki barwnika pochłaniają światło lasera, przekazują tę energię do cząstki zamiast emitować ją jako własne światło. Kluczową innowacją jest to, że energia nie przeskakuje bezpośrednio z barwnika do głęboko osadzonych atomów erbu — proces ten sięgałby tylko do tych bliskich powierzchni — lecz przepływa kaskadowo: z barwnika do powłoki bogatej w ytterb, a stamtąd do rdzenia erbowego. Ta „warstwa przekaźnikowa” skraca efektywną odległość transferu energii i pozwala aktywować znacznie więcej atomów erbu. Dzięki kombinacji kontroli struktury, pomiarów optycznych i spektroskopii ultrakrótkoczasowej zespół wykazał, że ta kaskadowa ścieżka może skierować około 90% wzbudzenia barwnika do nanocząstki i silnie zapełnić poziom energetyczny erbu odpowiadający emisji przy 1525 nm.
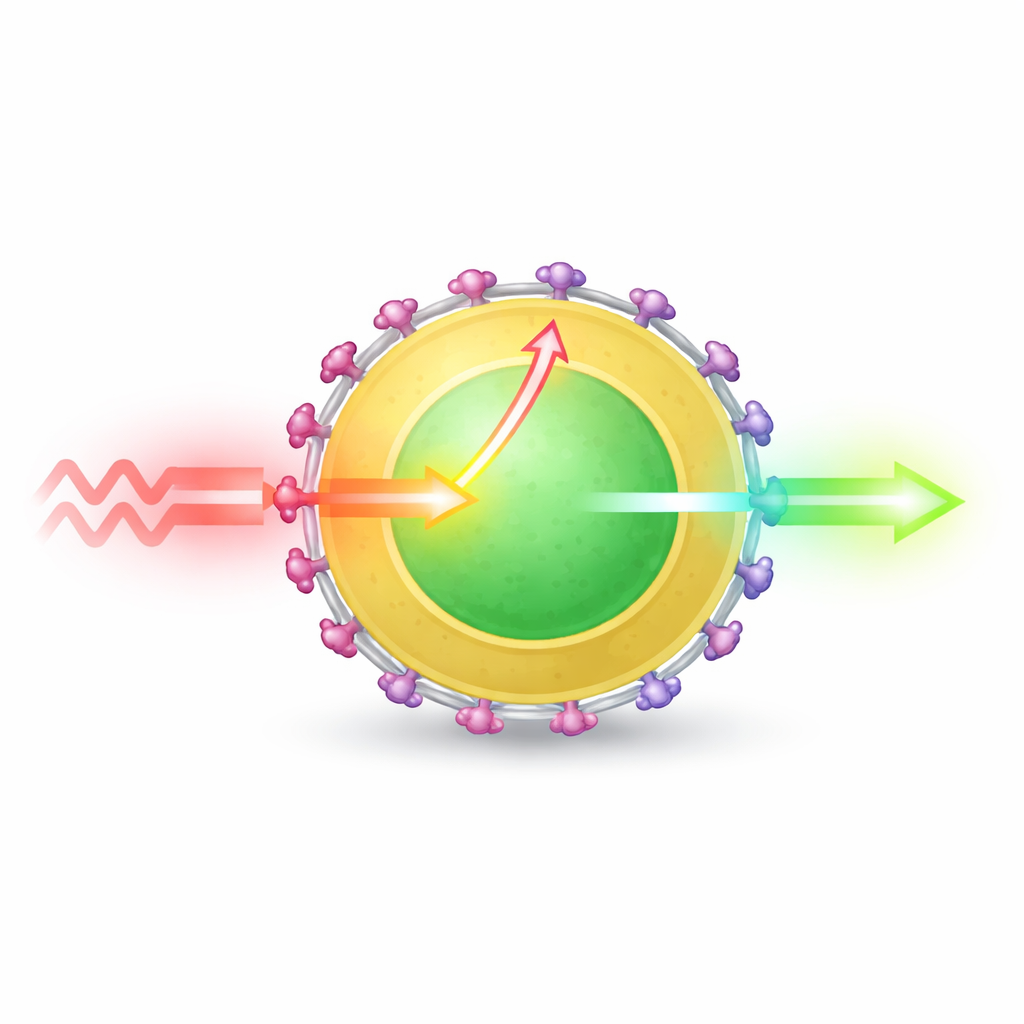
Dostrajanie warstw dla maksymalnego blasku
Autorzy starannie zmieniali zarówno grubość, jak i skład powłoki, aby zrozumieć, co pomaga, a co szkodzi jasności. Bezwartościowa powłoka, która jedynie izoluje rdzeń, zmniejsza straty energii na powierzchni, ale niewiele poprawia absorpcję światła. Powłoki domieszkowane dodatkowymi atomami erbu lub innym pierwiastkiem, neodymem, mogą wręcz pogorszyć działanie, ponieważ energia ucieka do defektów powierzchniowych i ginie, zanim zostanie wyemitowana. Natomiast powłoka zawierająca 50% ytterbu osiąga skuteczną równowagę: działa jako wydajny zbieracz i pomost energii bez wprowadzania nadmiernych strat. Po powleczeniu barwnikiem ten zoptymalizowany projekt zwiększa emisję przy 1525 nm o współczynnik 1965 w porównaniu z samym rdzeniem i 11‑krotnie względem już ulepszonej cząstki rdzeń–powłoka.
Od probówki do naczyń żywych organizmów
Aby uczynić cząstki kompatybilnymi z organizmem, zespół otoczył je ochronną, hydrofilową powłoką polimerową, poprawiając ich stabilność w płynach i zmniejszając skłonność do agregacji. W testach komórkowych powlekane cząstki wykazały niską toksyczność przy wysokich stężeniach i pozostały jasne przy długotrwałym oświetleniu. Wstrzyknięte do myszy nanoprobe krążyły we krwi i dawały wyraźne obrazy naczyń krwionośnych przy oświetleniu bezpiecznymi poziomami światła 808 nm i detekcji przy 1525 nm. Naczynia można było rozdzielić aż do około 200 mikrometrów szerokości, z sygnałem ponad trzykrotnie silniejszym niż otaczająca tkanka, a świecenie utrzymywało się wystarczająco długo — w skali około godziny — by umożliwić praktyczne obrazowanie przepływu krwi i struktury naczyń.
Co to oznacza dla przyszłego obrazowania
Przekształcając słabego emitera w podczerwieni w wyjątkowo jasną nanoskalową latarnię przez starannie zaprojektowany przekaźnik energii, ta praca przedstawia ogólny schemat projektowania sond obrazujących nowej generacji. Konkretnie opracowane tu cząstki są już potężnymi narzędziami do mapowania naczyń i badania krążenia w żywych zwierzętach, a podobne strategie można zastosować do innych długości fal, barwników i lantanowców. Choć bezpieczeństwo długoterminowe i stabilność barwnika wymagają dalszych badań przed zastosowaniem u ludzi, koncepcja kaskadowego transferu energii w warstwowych nanocząstkach oferuje obiecującą drogę do jaśniejszych, głębszych i bardziej informacyjnych optycznych widoków wnętrza ciała.
Cytowanie: Long, F., Gan, D., Chen, H. et al. Dye-sensitized cascaded energy transfer for amplified 1525 nm luminescence in highly doped lanthanide nanoparticles. Light Sci Appl 15, 215 (2026). https://doi.org/10.1038/s41377-026-02302-9
Słowa kluczowe: obrazowanie w bliskiej podczerwieni, nanocząstki lantanowców, sensytyzacja barwnikowa, obrazowanie naczyń, nanoprobe