Clear Sky Science · pl
Określenie subkomórkowych reakcji błony maziowej przy początku choroby zwyrodnieniowej stawu skroniowo‑żuchwowego za pomocą modeli przeciążenia mechanicznego i przemieszczenia dysku stawowego
Dlaczego zużycie stawu żuchwy ma znaczenie
Staw żuchwy, czyli staw skroniowo‑żuchwowy (TMJ), pozwala żuć, mówić i ziewać. Gdy zaczyna się rozpadać — stan określany jako choroba zwyrodnieniowa TMJ — pacjenci mogą cierpieć z powodu przewlekłego bólu, trudności w jedzeniu i pogorszenia jakości życia. W porównaniu z kolanami czy biodrami ten mały, lecz złożony staw był jednak znacznie mniej badany. W artykule zastosowano nowoczesne narzędzia do mapowania genetycznego w modelach mysich, by w bezprecedensowym szczególe pokazać, co dzieje się wewnątrz miękkiej wyściółki stawu na wczesnym etapie choroby zwyrodnieniowej TMJ.
Dwa sposoby przeciążenia stawu żuchwy
Aby naśladować powszechne problemy obserwowane u pacjentów, badacze stworzyli dwa typy uszkodzeń TMJ u myszy. W jednym zmienili stykanie się zębów tak, że żuchwa zamykała się skośnie, wielokrotnie przeciążając staw — co odpowiada mechanicznemu obciążeniu wynikającemu z nieprawidłowego zwarcia. W drugim chirurgicznie przesunęli amortyzujący dysk stawowy do przodu i przymocowali go w niewłaściwym miejscu, imitując przemieszczenie dysku często związane z bólem TMJ. Oba modele porównano ze zdrowymi kontrolami przez trzy tygodnie, mierząc zmiany w strukturze kości i tkanek za pomocą trójwymiarowych skanów rentgenowskich i mikroskopii. 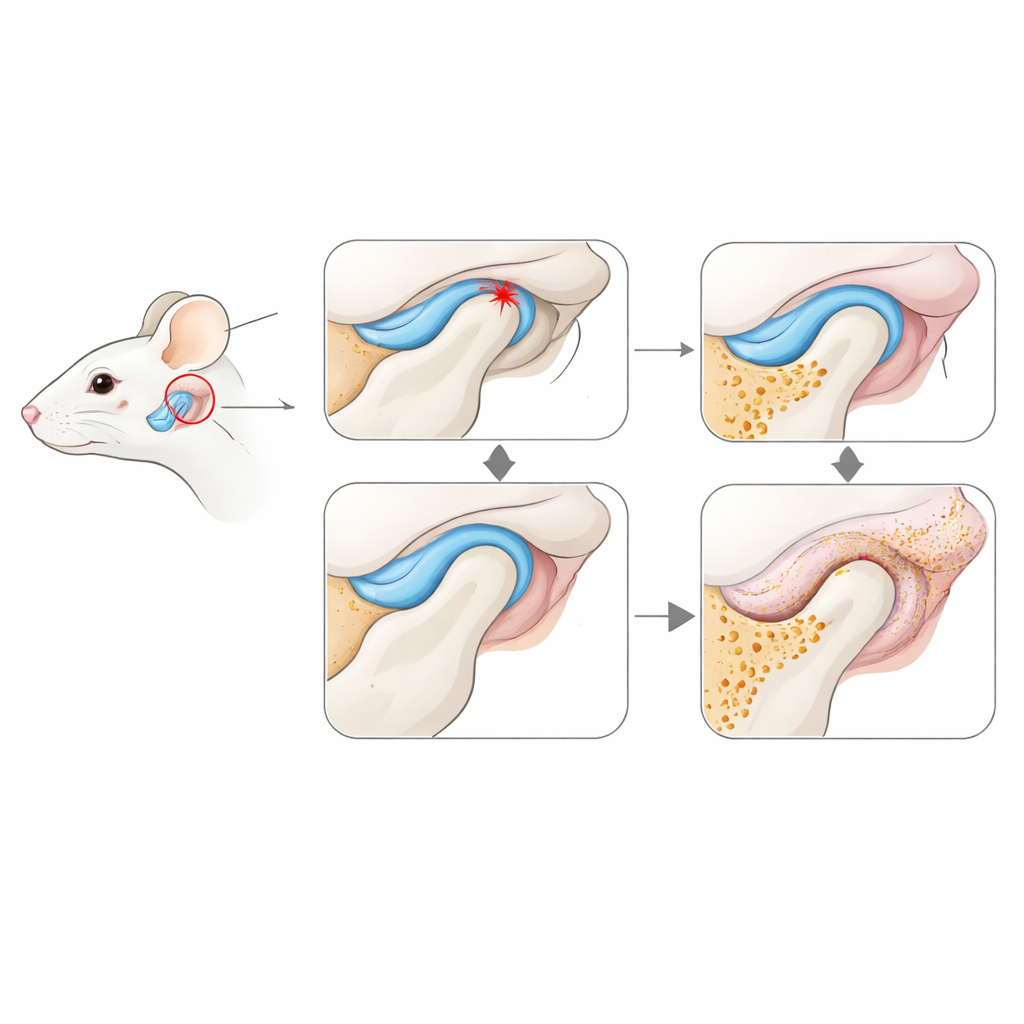
Wczesne uszkodzenia kości, chrząstki i wyściółki stawu
Zarówno stawy przeciążone, jak i z przemieszczeniem dysku szybko wykazały charakterystyczne oznaki wczesnej choroby zwyrodnieniowej. Głowa żuchwy straciła gęstość mineralną i rozwinęła ubytki, dodatkowe wyrośla kostne oraz zwiększoną aktywność komórek resorbujących kość, co wskazuje na zbyt szybkie przebudowywanie wewnętrznego rusztowania stawu. Chrząstka, która normalnie zapewnia gładką powierzchnię poślizgową, zaczęła się przerzedzać, pękać i tracić protekcyjne cząsteczki, szczególnie w modelu z przemieszczeniem dysku. Jednocześnie błona maziowa — cienka, miękka tkanka wyściełająca staw i odżywiająca go — ulegała pogrubieniu, napływowi komórek, a w niektórych obszarach przekształcała się w tkankę tłuszczową lub włóknistą. Te zmiany strukturalne sugerują, że wyściółka stawu nie jest jedynie biernym obserwatorem, lecz kluczowym uczestnikiem rozpoczynającego się niszczenia stawu.
Odczytywanie molekularnych sygnałów stawu komórka po komórce
Aby wyjść poza anatomię i zobaczyć, co robią poszczególne komórki, zespół zbadał, które geny są aktywne w tysiącach komórek, używając sekwencjonowania RNA z próbek zbiorczych, pojedynczych komórek oraz wysokorozdzielczej transkryptomiki przestrzennej. Metody te pozwoliły ustalić, kiedy i gdzie różne typy komórek zmieniają swoje zachowanie. Na końcu kostnym stawu geny zwykle wspierające zdrowie chrząstki były wyciszone, podczas gdy geny powiązane z rozkładem tkanki i aktywnością resorpcyjną kości były wzmocnione, szczególnie w modelu z przemieszczeniem dysku. W błonie maziowej komórki zwiększyły produkcję mediatorów zapalnych, enzymów trawiących tkankę oraz cząsteczek związanych ze bliznowaceniem i włóknieniem. Szczególnie istotnym punktem zapalnym była tylna (posterior) część wyściółki dysku, gdzie wczesnemu zapaleniu, gromadzeniu tłuszczu i włóknistemu pogrubieniu towarzyszyły się nawzajem.
Komunikacja międzykomórkowa i nowa mapa stawu żuchwy
Analizując aktywność genów komórka po komórce i umieszczając te komórki z powrotem w ich dokładnych pozycjach w tkance, autorzy zidentyfikowali odrębne „sąsiedztwa” fibroblastów (komórek podporowych), komórek układu odpornościowego i komórek tworzących naczynia krwionośne w obrębie błony maziowej. Wygląda na to, że typy te komunikują się między sobą za pośrednictwem szlaków sygnałowych reagujących na odkształcenie mechaniczne i zapalenie. Na przykład sygnały w szlaku Notch — znanym z regulacji naczyń i przebudowy tkanek — były szczególnie aktywne w komórkach śródbłonka (wyściełających naczynia) w uszkodzonych stawach, prawdopodobnie pod wpływem pobliskich fibroblastów. Te same rejony wykazywały także wysokie poziomy enzymów rozkładających chrząstkę i markerów włóknienia, co wzmacnia hipotezę, że zestresowane komórki maziowe mogą napędzać utratę chrząstki i ból. 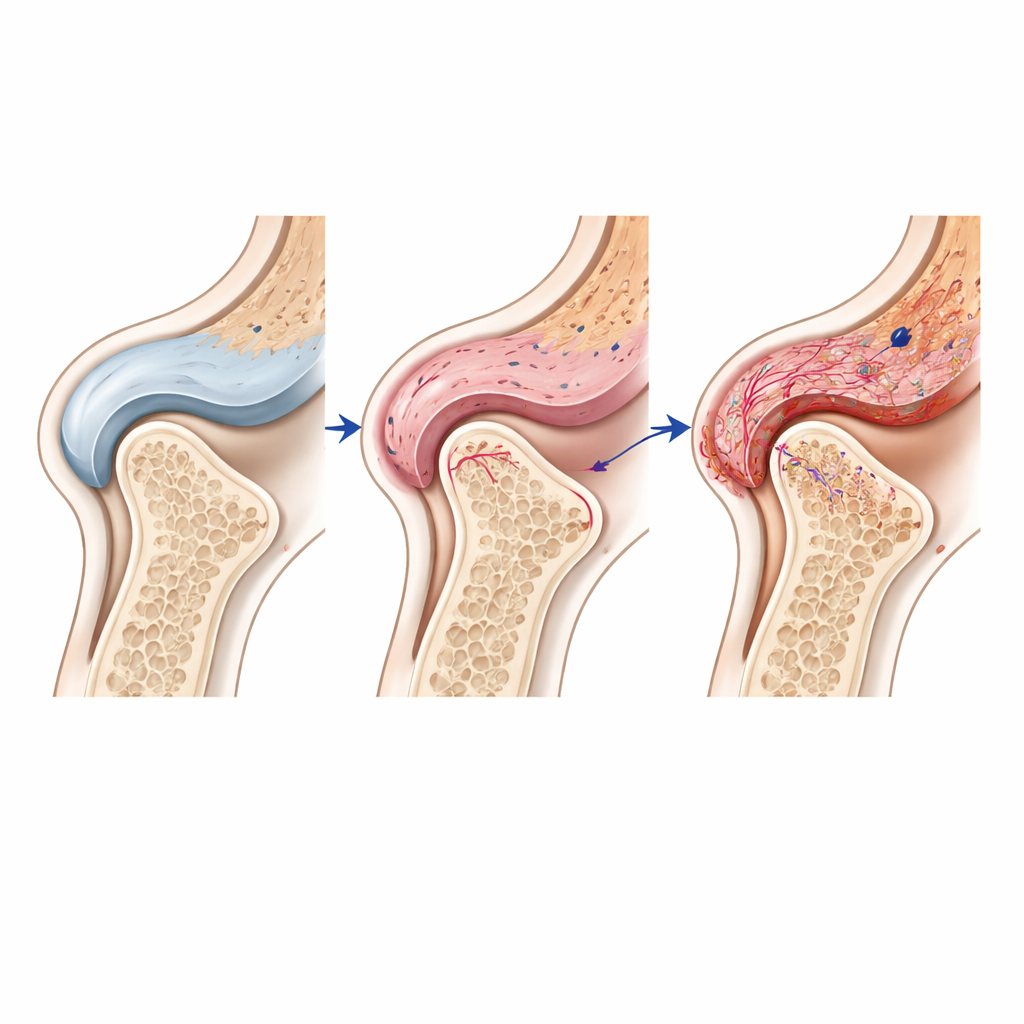
Jak ta praca może wpłynąć na przyszłe terapie
Zamiast testować konkretny lek, badanie dostarcza szczegółowego atlasu reakcji miękkiej wyściółki TMJ i chrząstki na szkodliwe siły na samym początku choroby. Pokazuje, że wczesna choroba zwyrodnieniowa TMJ cechuje się skoordynowanymi zmianami w kości, chrząstce i w szczególności komórkach błony maziowej, które stają się zapalne i włókniejące, jednocześnie wysyłając szkodliwe sygnały do stawu. Przypisując te zmiany do precyzyjnych typów komórek i lokalizacji, praca wskazuje nowe potencjalne cele terapeutyczne — takie jak szlaki związane z sygnalizacją Notch, sygnalizacją chemokinową czy enzymami degradującymi macierz — które można by zablokować zanim uszkodzenia stawu staną się nieodwracalne. Krótko mówiąc, artykuł dostarcza potężnego planu działania do zrozumienia i ostatecznego przerwania łańcucha wydarzeń, który zamienia codzienne ruchy żuchwy w przewlekły ból TMJ.
Cytowanie: Shibusaka, K., Negishi, S., Terashima, A. et al. Defining subcellular synovial responses in TMJ osteoarthritis onset via mechanical stress and articular disk derangement models. Int J Oral Sci 18, 28 (2026). https://doi.org/10.1038/s41368-025-00411-6
Słowa kluczowe: staw skroniowo‑żuchwowy, choroba zwyrodnieniowa stawów, błona maziowa, obciążenie mechaniczne, transkryptomika pojedynczych komórek