Clear Sky Science · nl
Kunstmatige intelligentie voor echografische diagnose en stratificatie van folliculaire schildklierneoplasmata: een multicenterstudie
Waarom dit belangrijk is voor mensen met schildklierknobbels
Veel mensen ontdekken schildklierknobbels tijdens routinecontroles en maken zich vervolgens wekenlang zorgen terwijl ze wachten om te horen of de groei goedaardig of kwaadaardig is. Deze studie onderzoekt of kunstmatige intelligentie (AI) echobeelden van een specifieke groep schildkliergroeiingen — zogeheten folliculaire neoplasmata — nauwkeuriger kan interpreteren dan menselijke experts, zodat patiënten onnodige operaties kunnen vermijden en gevaarlijke tumoren niet over het hoofd worden gezien.
Wanneer onschuldig en gevaarlijk er hetzelfde uitzien
Folliculaire schildkliertumoren komen hoofdzakelijk in twee vormen voor: adenomen, die goedaardig zijn, en carcinomen, die bloedvaten kunnen aantasten en uitzaaien. Zowel onder de microscoop als op echobeelden lijken deze tumoren vaak opvallend veel op elkaar. Zelfs ervaren radiologen en pathologen hebben moeite ze voor de operatie uit elkaar te houden, waardoor veel patiënten de helft of de gehele schildklier laten verwijderen alleen om een definitieve diagnose te krijgen. De inzet is hoog: sommige carcinomen zijn slechts licht invasief en hebben een gunstige prognose, terwijl andere agressiever zijn; het exacte type bepaalt dus hoeveel operatie en nazorg een patiënt daadwerkelijk nodig heeft.
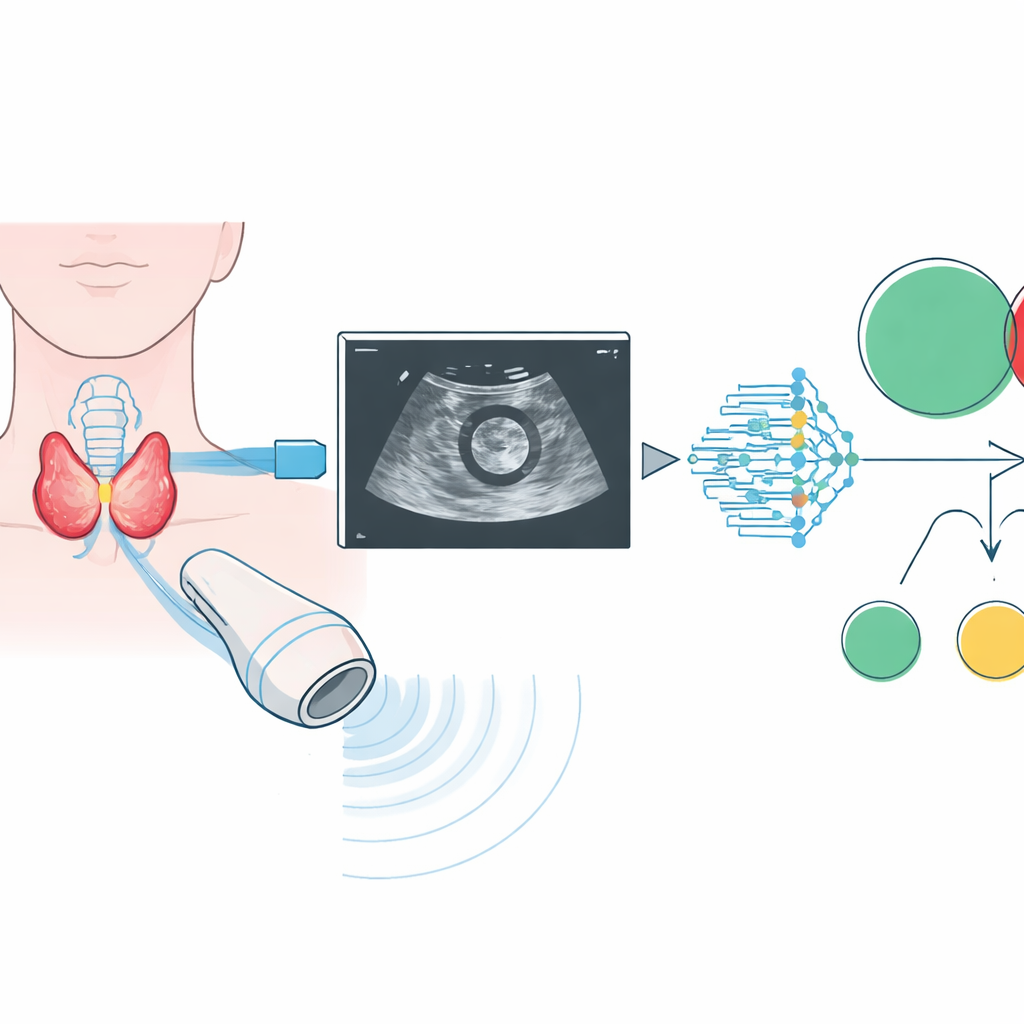
Een computer leren schildklier-echografieën te lezen
De onderzoekers stelden een van de grootste verzamelingen folliculaire schildklier-echobeelden tot nu toe samen, gebaseerd op 2.567 patiënten uit 31 ziekenhuizen in heel China. Voor elke knobbel tekenden radiologen het relevante gebied af op standaard zwart-wit echobeelden. Een modern deep-learningsysteem, gebaseerd op een visuele architectuur bekend als ConvNeXt, werd vervolgens in fasen getraind. Eerst leerde het onderscheid te maken tussen goedaardige adenomen en carcinomen. Daarna leerde het, binnen de carcinomen, ze in minder invasieve en meer invasieve subtypes te classificeren, die globaal overeenkomen met laag-, midden- en hoogrisicoziekte. Het team testte verschillende soorten echografie-informatie en vond dat eenvoudige B-modusbeelden — standaard grijswaardenbeelden — betrouwbaarder waren voor de AI dan kleurendopplerbeelden van de bloedstroom, die in kwaliteit te veel varieerden.
Hoe goed de AI in de praktijk presteerde
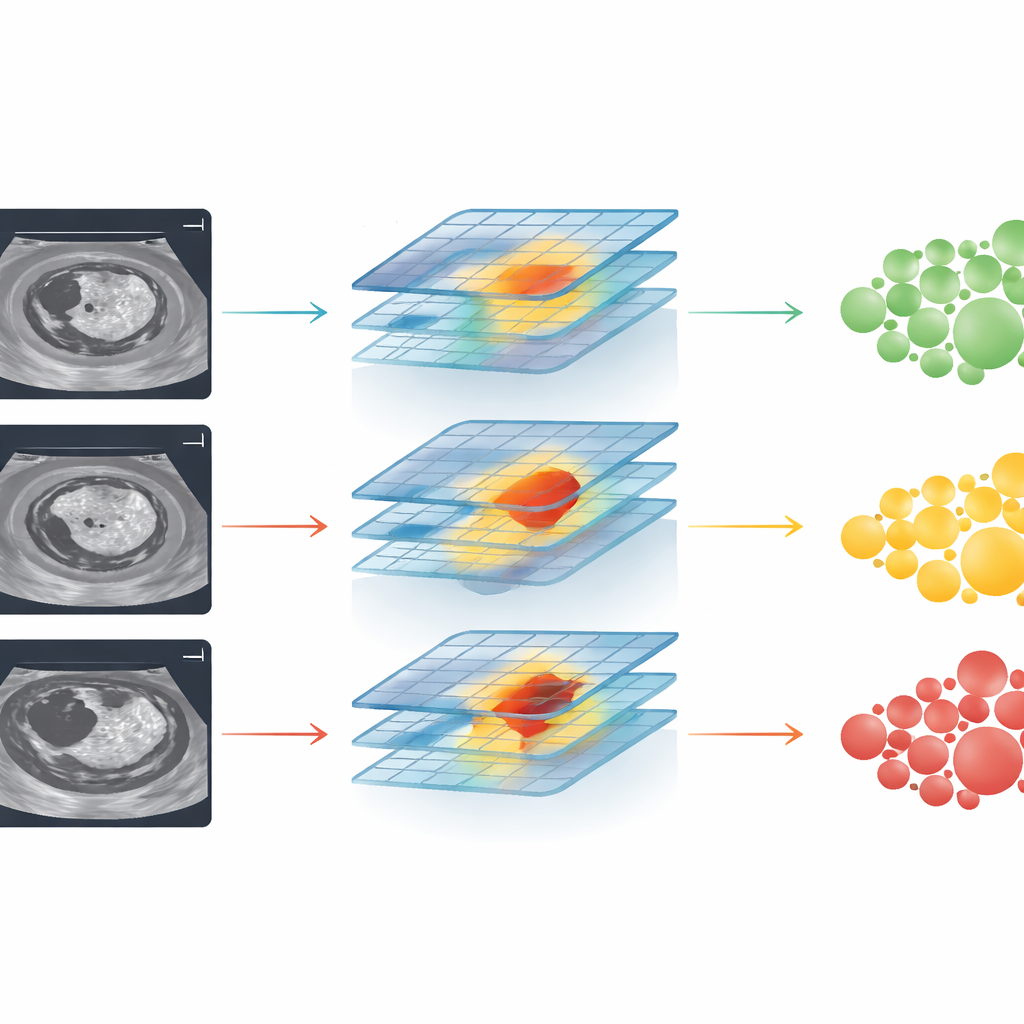
Om te beoordelen of het systeem ook buiten de laboratoria waar het werd ontwikkeld standhield, testten de auteurs het op drie onafhankelijke patiëntengroepen uit andere ziekenhuizen, elk met verschillende verhoudingen van goedaardige en kwaadaardige tumoren. Over deze centra heen toonde de AI consequent sterke prestaties bij het scheiden van adenomen en carcinomen, met nauwkeurigheidsmaten (AUC-waarden) rond 0,82 tot 0,85. Het slaagde ook goed in de zwaardere taak: tumoren in drie groepen rangschikken — goedaardig, minimaal invasief carcinoma en meer agressief invasief carcinoma — waarbij het in alle ziekenhuizen hoge prestaties behield. Belangrijk is dat het model ongeveer even goed werkte voor mannen en vrouwen, voor verschillende chirurgische benaderingen en in de meeste geografische regio’s, wat erop wijst dat het in uiteenlopende klinische omgevingen bruikbaar zou kunnen zijn.
Samenwerken met radiologen, niet vervangen
De studie stelde ook een praktische vraag: helpt deze AI artsen daadwerkelijk betere beslissingen te nemen? Wanneer radiologen alleen gevestigde score-systemen voor schildklier-echografie gebruikten, was hun prestatie bij het herkennen van carcinomen duidelijk zwakker dan die van de AI. Wanneer ze de output van de AI en de bijbehorende gemarkeerde “attention maps” op dezelfde afbeeldingen te zien kregen, steeg hun nauwkeurigheid en in sommige gevallen benaderde die bijna die van de computer. Beginnende artsen hadden het meeste profijt, maar ook ervaren specialisten kregen een voordeel. Tegelijk toonde analyse van gevallen die de AI fout had gemaakt een belangrijke zwakte: bij die beelden richtte het systeem zich vaak op gebieden buiten de daadwerkelijke tumor in plaats van op de verdachte interne kenmerken, wat aangeeft waar verdere verfijningen nodig zijn.
Wat dit voor patiënten kan betekenen
In eenvoudige bewoordingen suggereert dit werk dat een goed getrainde AI kan fungeren als een tweede, zeer consistente paar ogen wanneer artsen schildklier-echografieën beoordelen. Voor patiënten met folliculaire schildklierknobbels zou zo’n hulpmiddel de kans kunnen vergroten dat een gevaarlijk carcinoma vóór een operatie wordt herkend, terwijl het de kans verkleint dat een onschuldige adenoom leidt tot te agressieve behandeling. Het model is niet klaar om deskundig oordeel te vervangen en moet nog worden getest in andere landen en bij meer gevarieerde patiëntengroepen. Maar als onderdeel van een echografiewerkstation of -scanner kan het binnenkort helpen operatie en nazorg af te stemmen op iemands werkelijke risiconiveau, waardoor een vroeger troebele zone in de schildklierdiagnostiek duidelijker wordt gemaakt.
Bronvermelding: Li, J., Zhang, H., Zheng, H. et al. Artificial intelligence-enabled ultrasound diagnosis and stratification of follicular thyroid neoplasms: a multi-center study. npj Digit. Med. 9, 313 (2026). https://doi.org/10.1038/s41746-026-02489-6
Trefwoorden: schildklier-echografie, folliculair neoplasma, kunstmatige intelligentie, kankerrisicostratificatie, medische beeldvorming