Clear Sky Science · nl
Gepersonaliseerde analyse van signaalroutes in gastro-intestinale tumoren voor patiëntstratificatie en evaluatie van medicijndoelen met klinisch verkregen kernbiopten
Waarom dit onderzoek van belang is voor patiënten
Oncologen proberen steeds vaker behandelingen af te stemmen op de unieke biologische eigenschappen van iemands tumor. Voor kankers van het spijsverteringsstelsel — zoals van de alvleesklier, dikke darm, lever of galwegen — is dit extra urgent, omdat ze veel voorkomen, vaak laat worden ontdekt en moeilijk te behandelen zijn. Deze studie onderzoekt een nieuwe laboratoriummethode die de activiteit van veel eiwitten die bij kanker betrokken zijn kan aflezen uit piepkleine biopten, met als doel artsen te helpen nauwkeuriger therapieën voor individuele patiënten te kiezen.
Van DNA-lijsten naar levende signalen
Tegenwoordig berust de meeste “gepersonaliseerde” kankerzorg op het lezen van DNA-veranderingen in een tumor. Hoewel dat krachtig is, toont DNA op zichzelf niet welke signalen in de cel daadwerkelijk aanstaan en de groei aansturen. Die signalen worden gedragen door eiwitten, van veel waarvan medicijnen direct gebruik kunnen maken. De onderzoekers gebruikten een high-throughput techniek genaamd DigiWest, een moderne variant van de klassieke Western blot, om ongeveer 130–200 eiwitten en hun geactiveerde vormen tegelijk te meten. Belangrijk is dat deze methode slechts ongeveer zoveel materiaal nodig heeft als een enkele naaldbiopsie, waardoor hij geschikt is voor gebruik in de klinische praktijk.
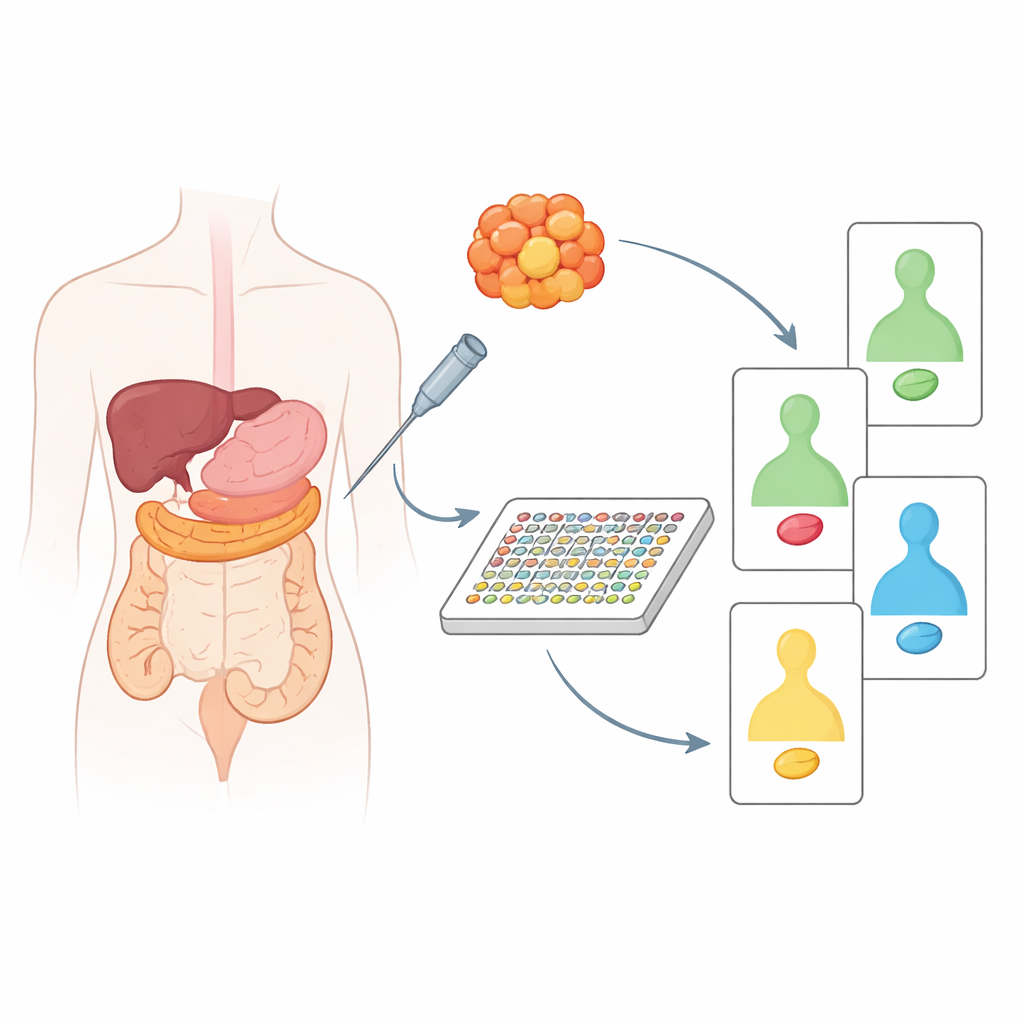
Vergelijken van tumorgewebe met het gezonde naburige weefsel
Het team analyseerde eerst bewaard weefsel van 20 patiënten met pancreas- of colorectale kanker, telkens gekoppeld aan nabijgelegen niet-kankerachtig weefsel van dezelfde persoon. Door tumoren met hun eigen gezonde tegenhangers te vergelijken, konden ze zien welke eiwitten echt door kanker waren veranderd en welke normale verschillen tussen organen weerspiegelden. Dit toonde duidelijke contrasten in het gedrag van bekende tumorbewakers en -stimulatoren, zoals p53, Ras, PTEN en anderen. Pancreastumoren bijvoorbeeld lieten vaak versterkte groeibevorderende signalen en verlies van beschermende eiwitten zien, terwijl darmtumoren hun eigen karakteristieke patroon van verstoorde paden hadden. Toen de onderzoekers de monsters clusterden op basis van deze eiwitveranderingen, konden ze pancreaskankers in twee biologisch verschillende groepen verdelen en betekenisvolle verschillen bij darmkankers detecteren die samenhingen met de leeftijd van de patiënt en de locatie van de tumor in de darm.
Individuele tumorkerndata’s van signaalactiviteit
Verder dan groepsgemiddelden bouwden de wetenschappers een gedetailleerd eiwitprofiel voor elke tumor. Deze profielen gaven aan welke signaalroutes — zoals die rond mTOR, MAPK/Erk, Wnt of immuungerelateerde factoren — bijzonder actief of uitgeschakeld waren. Veel van de gemeten eiwitten zijn directe doelen van bestaande geneesmiddelen, of liggen net stroomafwaarts van zulke doelen, waardoor het team kon afleiden welke middelen mogelijk de belangrijkste groeimotoren van een tumor zouden kunnen verstoren. In driekwart van de retrospectieve gevallen konden ze wijzen op een of meer paden die waarschijnlijk de tumorprogressie aandreven. Ze identificeerden ook tumoren met veel immuuncelmarkers, wat wijst op “hete” kankers die mogelijk op immunotherapie reageren, en uitzonderlijke gevallen met opvallend unieke signaturen.
De methode toepassen bij echte patiënten
Om het nut aan het bed te testen, pasten de onderzoekers DigiWest toe op verse naaldbiopten van 14 patiënten met verschillende gastro-intestinale kankers waarvan de dossiers door een Moleculair Tumor Board werden beoordeeld. Deze patiënten hadden vaak complexe ziektegeschiedenissen en eerdere behandelingen. Omdat er geen gezond weefsel beschikbaar was om mee te vergelijken, werden de eiwitniveaus van elke tumor vergeleken met het mediaaniveau van de groep om te bepalen wat als abnormaal hoog of laag gold. Zelfs met deze strengere opzet toonden 12 van de 14 tumoren duidelijke, voor de behandeling relevante patronen van padactiviteit. In twee gedetailleerde voorbeelden bevestigden de eiwitgegevens een DNA-niveau amplificatie van het FGFR2-gen in een coloncarcinoom en het verlies van een mTOR-rem in een leverkanker, wat de overweging van FGFR-remmende of mTOR-remmende geneesmiddelen door het Board sterk ondersteunde. In het algemeen stonden de DigiWest-resultaten in overeenstemming met belangrijke genetische drijfveren en suggereerden ze medicijndoelen in de meeste evalueerbare gevallen.
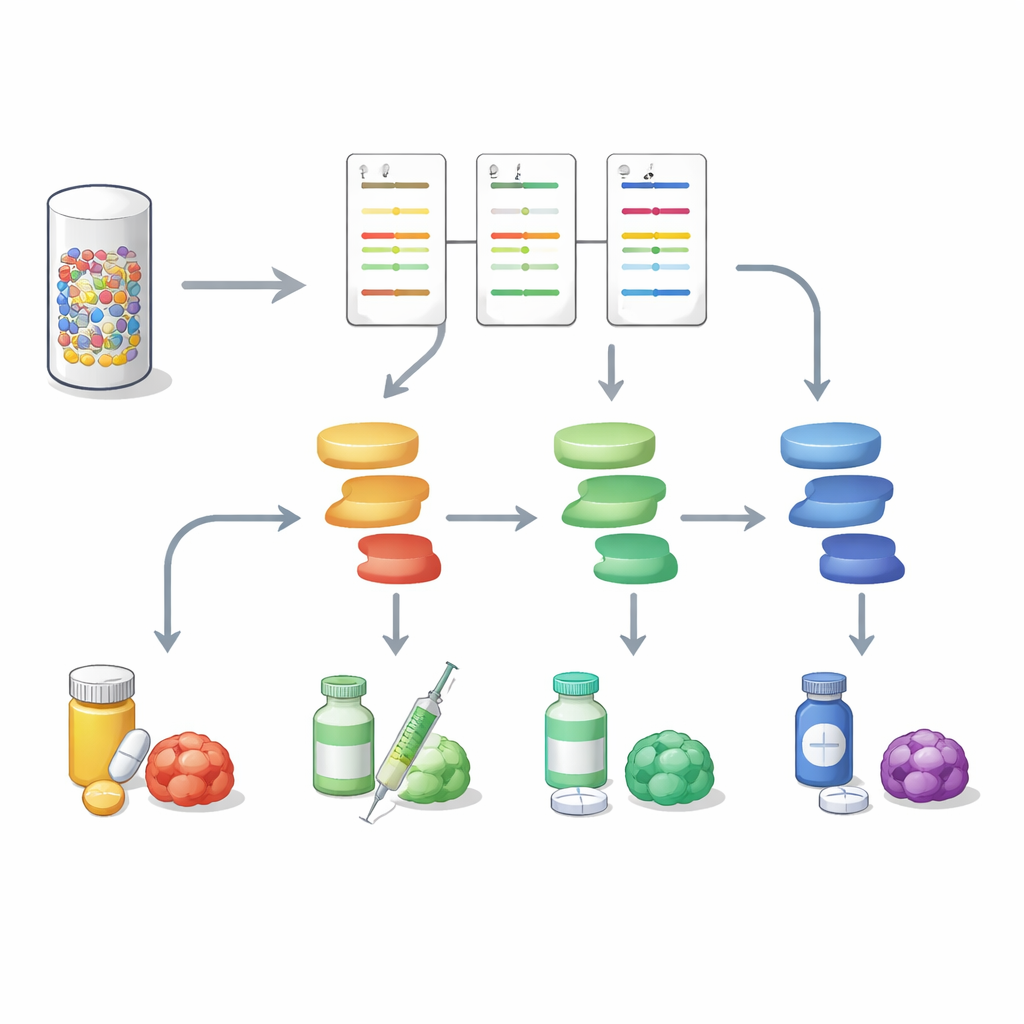
Op weg naar meer volledige tumorportretten
Dit werk laat zien dat het analyseren van eiwitsignaling parallel aan DNA-sequencing een rijker en meer bruikbaar beeld van gastro-intestinale tumoren kan bieden. Door een klein biopt om te zetten in een multi-paden activiteitskaart, helpt DigiWest te onderscheiden welke moleculaire schakelaars in een gegeven kanker echt aanstaan en welke medicijnen ze het beste kunnen raken, en kan het ook opkomende resistentiewegen aanwijzen. Hoewel grotere studies nog nodig zijn, biedt de aanpak een praktische manier om hoogwaardige eiwitprofilering onderdeel te maken van alledaagse precisie-oncologie en dichterbij behandelingsplannen te komen die zijn afgestemd op iemands levende tumor, en niet alleen op het genetische blauwdruk.
Bronvermelding: Stahl, A., Büringer, K., Missios, P. et al. Personalized signaling pathway analysis of gastrointestinal tumors for patient stratification and drug target evaluation using clinically derived core biopsies. npj Precis. Onc. 10, 124 (2026). https://doi.org/10.1038/s41698-026-01304-5
Trefwoorden: precisie-oncologie, gastro-intestinale kanker, proteomica, biopsieprofilering, gerichte therapie