Clear Sky Science · nl
LASSO–HHO tweefasig hybride genselectiekader voor nauwkeurige diagnose van de ziekte van Alzheimer
Waarom dit onderzoek belangrijk is voor hersengezondheid
De ziekte van Alzheimer berooft mensen van geheugen en zelfstandigheid, en we hebben nog geen eenvoudige, breed beschikbare middelen om de ziekte vroeg te detecteren. Moderne laboratoriumtechnieken kunnen de activiteit van tienduizenden genen meten in een klein stukje hersenweefsel of bloed, maar die datastroom is moeilijk te vertalen naar duidelijke ja/nee-antwoorden voor artsen. Dit artikel introduceert een slimme, tweeledige methode om die genetische informatie te filteren en een klein aantal genen te selecteren dat Alzheimer met zeer hoge nauwkeurigheid kan diagnosticeren, terwijl de methode snel en praktisch genoeg blijft voor gebruik in de praktijk.
Van een hooiberg aan genen naar een handvol aanwijzingen
Elke genexpressiedataset voor Alzheimer die in deze studie is gebruikt bevat meer dan 20.000 genen maar slechts enkele honderden patiënten. Die scheve verhouding is als proberen iemands identiteit vast te stellen aan de hand van duizenden vragen, met antwoorden van slechts een kleine groep vrijwilligers: het is makkelijk om toevalsgeluiden te overschatten. De auteurs pakken dit aan door eerst een techniek toe te passen die LASSO heet, die fungeert als een krachtige filter. Deze techniek drukt de signaalsterkte van de meeste genen naar nul en behoudt alleen diegenen die echt helpen onderscheid te maken tussen mensen met Alzheimer en gezonde controles. Op zichzelf reduceert deze eerste stap vaak de genlijst met meer dan 99%, waardoor de complexiteit en de kans op overfitting sterk afnemen, terwijl er nog voldoende informatie overblijft om de ziekte te voorspellen.
Een tweede intelligente doorloop indien nodig
Na deze initiële snoei lanceert het kader conditioneel een tweede stap op basis van een in de natuur geïnspireerde zoekstrategie genaamd Harris Hawks Optimization. Hier stelt elke “havik” een mogelijke subset genen voor, en de haviken passen herhaaldelijk hun posities aan om combinaties te vinden die tot een betere diagnose leiden. Cruciaal is dat deze stap niet altijd wordt gebruikt. Als LASSO op zichzelf al minstens 99% nauwkeurigheid bereikt en de geselecteerde genenset kleiner is dan 40 genen, stopt het proces daar. Anders verfijnt de havik-gebaseerde zoekprocedure de overgebleven genen verder, gestuurd door een scoringsregel die hoge diagnostische accuraatheid sterk beloont maar nog steeds voorkeur geeft aan een zo klein mogelijke set genen. Dit adaptieve ontwerp voorkomt het verspillen van rekentijd wanneer de eenvoudigere oplossing al goed genoeg is.
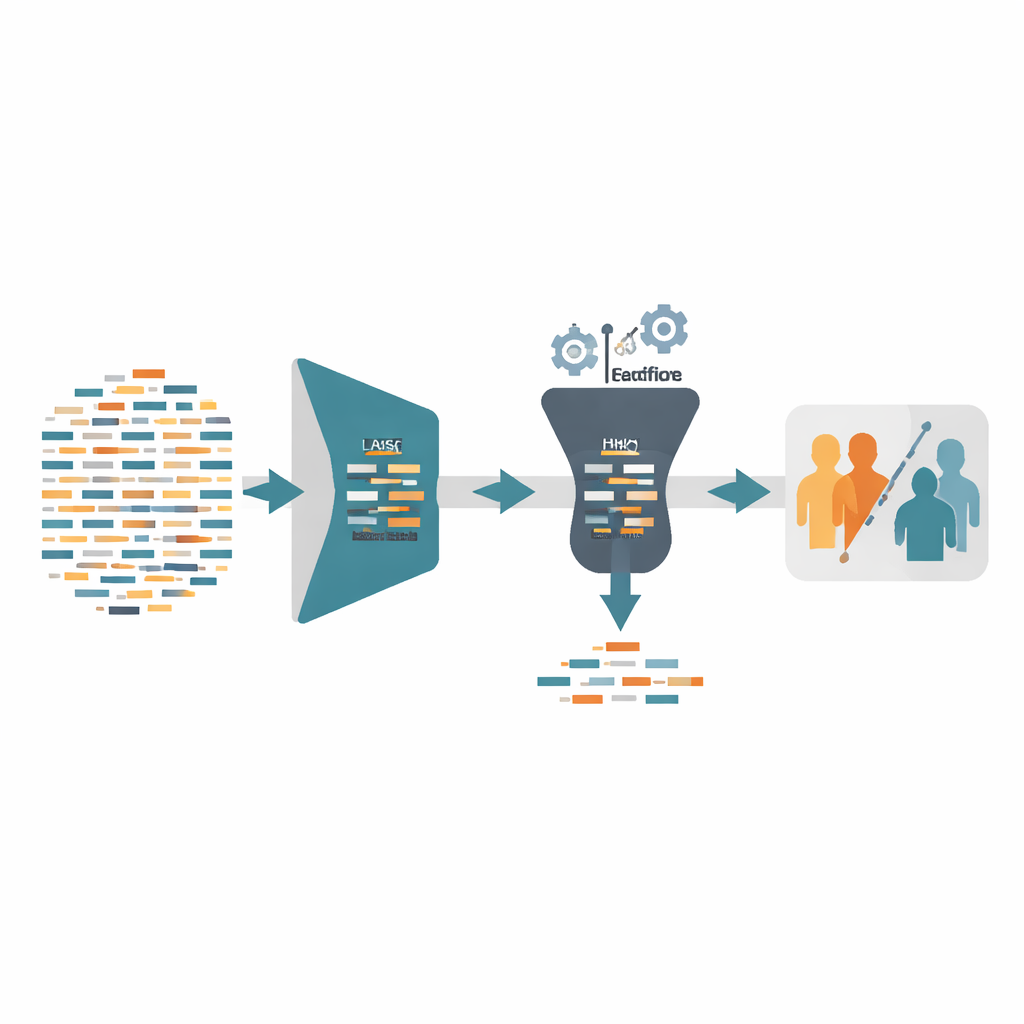
De methode op de proef gesteld
De auteurs evalueerden hun kader — LHGS genoemd — op vier openbare Alzheimer-datasets afkomstig uit verschillende hersengebieden en onderzoeksgroepen. Ze trainden een standaard machine-learningclassifier, een support vector machine, uitsluitend met de geselecteerde genen en beoordeelden de prestaties met gangbare maatstaven zoals nauwkeurigheid, precisie en recall. In sommige datasets was LASSO op zichzelf voldoende om perfecte of bijna perfecte nauwkeurigheid te bereiken: één dataset had slechts drie genen nodig om alle Alzheimer- en gezonde monsters correct te scheiden. In lastigere datasets verbeterde het toevoegen van de havik-gebaseerde zoekstap de nauwkeurigheid tot 100% terwijl de uiteindelijke set toch tussen ongeveer 11 en 37 genen bleef. Vergeleken met een reeks andere populaire optimalisatiemethoden was de tweefasige aanpak zowel nauwkeuriger als veel sneller, omdat de zware zoekactie alleen plaatsvindt in de drastisch verkleinde ruimte die door LASSO is gecreëerd.
Veelbelovende genmarkers ontdekken
Naast het bouwen van een goede voorspeller benadrukt de studie ook concrete genen die mogelijk bijzonder belangrijk zijn in de biologie van Alzheimer. Door te kijken naar hoe sterk elk gen bijdroeg in de LASSO-stap, identificeerden de auteurs een korte lijst van consequent invloedrijke genen in elke dataset. Sommige, zoals TRPM7 en genen die betrokken zijn bij stresssignaalroutes, ontstekingsregulatie en synaptische communicatie, zijn al in verband gebracht met hersengezondheid en neurodegeneratie. Andere zijn minder goed begrepen, wat nieuwe richtingen voor laboratoriumonderzoek suggereert. Het feit dat betrouwbare diagnose mogelijk is met slechts enkele tientallen of zelfs een paar genen wijst erop dat toekomstige tests zich mogelijk kunnen richten op kleine, gerichte panelen in plaats van brede, dure arrays.

Wat dit betekent voor toekomstige Alzheimer-diagnostiek
Voor een leek is de kernboodschap dat het steeds beter mogelijk wordt het moleculaire „handtekening” van Alzheimer te lezen aan de hand van een verrassend klein aantal genen, gekozen uit tienduizenden door een zorgvuldige tweestapsprocedure. Het LHGS-kader laat zien dat we een snelle statistische filter kunnen combineren met een selectieve tweede doorloop om zowel nauwkeurigheid als snelheid te bereiken, waardoor de aanpak geschikter wordt voor uiteindelijke klinische toepassingen. Hoewel de auteurs waarschuwen dat hun resultaten bevestiging behoeven in grotere en meer gevarieerde patiëntengroepen, en dat eerdere experimenten de prestaties mogelijk iets te optimistisch hebben ingeschat, wijst het werk in de richting van bloed- of weefselgebaseerde genetische tests die Alzheimer vroeg kunnen signaleren met een compact, goed gekozen setje genmarkers.
Bronvermelding: Asiry, O., El-Gawady, A., Eltoukhy, M.M. et al. LASSO–HHO two-stage hybrid gene selection framework for accurate Alzheimer’s disease diagnosis. Sci Rep 16, 13393 (2026). https://doi.org/10.1038/s41598-026-48742-6
Trefwoorden: Diagnose van Alzheimer, genexpressie, kenmerkselectie, machine learning, biomarkers