Clear Sky Science · nl
Verbetering van biomedische signalen met genetische-algoritme geoptimaliseerde exponentiële getransmuteerde Weibull-ruisonderdrukkingsmethoden
Waarom het opschonen van medische signalen belangrijk is
Elke hartslag op een elektrocardiogram en elke rimpeling in een hersengolfenspoor kan aanwijzingen bevatten voor ernstige aandoeningen. In echte ziekenhuizen en klinieken liggen deze signalen echter vaak begraven onder lagen ongewenste ruis door spiertrillingen, knipperen van de ogen, elektrische interferentie en onvolmaakte sensoren. Dit artikel introduceert een nieuwe manier om die rommelige signalen te zuiveren, zodat artsen en computeralgoritmen belangrijke patronen helderder kunnen zien—zonder enorme trainingsdatasets of supercomputers.
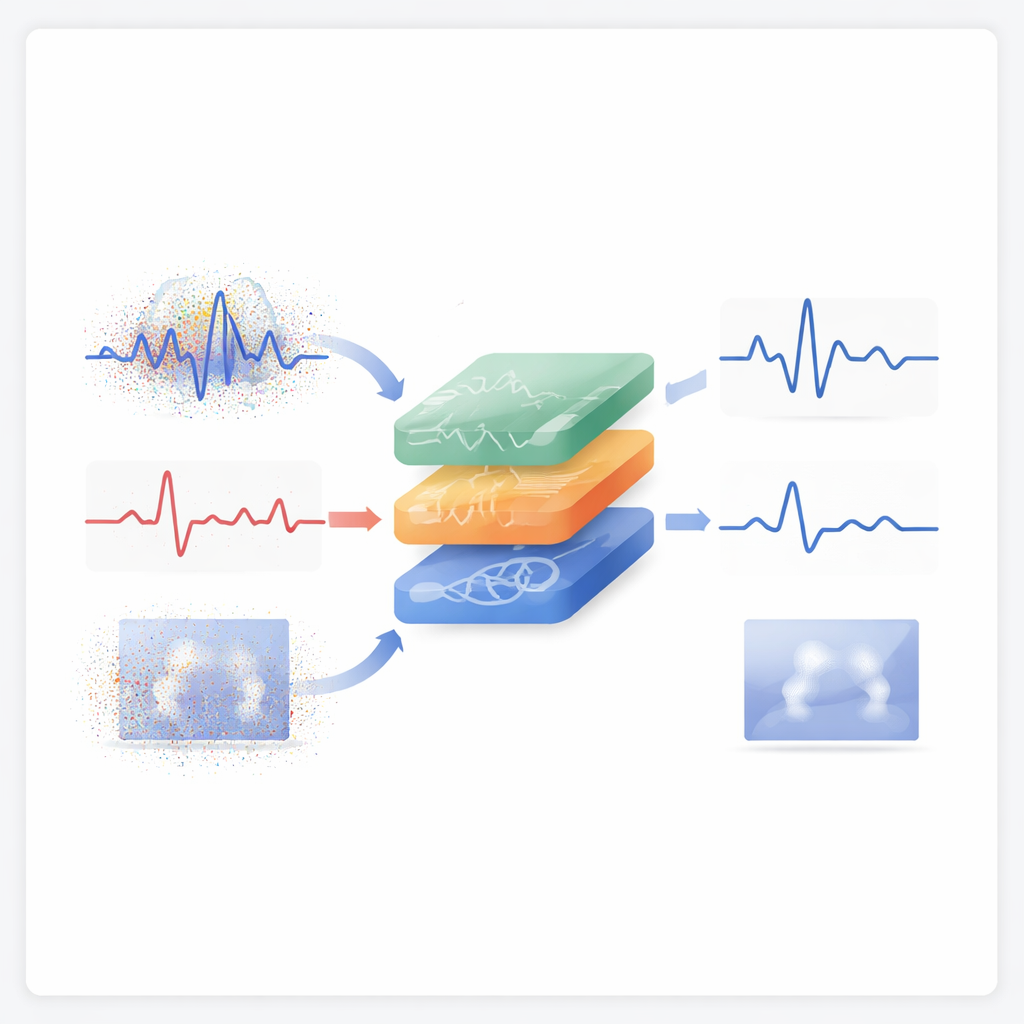
Het probleem van rommelige hartslagen en hersengolven
Electroencefalogrammen (EEG), elektrocardiogrammen (ECG) en medische beelden zoals MRI- en röntgenscans zijn cruciaal voor het diagnosticeren van epilepsie, hartritmestoornissen en structurele afwijkingen. Maar deze opnames raken gemakkelijk vervormd. Oogbewegingen kunnen epileptische pieken maskeren, lichaamsbeweging kan belangrijke ECG-kenmerken verbergen en korrelige ruis kan kleine details in beelden vervagen. Traditionele opschoonmethoden—zoals eenvoudige filters, wavelets of gangbare blindescheidingstechnieken—gaan er vaak van uit dat ruis zich op een nette, symmetrische manier gedraagt. In werkelijkheid is klinische ruis onregelmatig, scheef verdeeld en soms gedomineerd door zeldzame, extreme uitbarstingen. Wanneer methoden op te simplistische ruismodellen vertrouwen, verwijderen ze óf onvoldoende interferentie óf ze effenen per ongeluk juist die details weg die clinici belangrijk vinden.
Een flexibele manier om lastige ruis te beschrijven
De auteurs pakken dit aan door een zeer aanpasbaar ruismodel te introduceren, de Exponentiated Transmuted Weibull-verdeling, of ETWD. In plaats van aan te nemen dat ruis één vaste vorm heeft, gebruikt ETWD drie hoofdinstellingen om zijn kromme te herschikken, waardoor het een brede familie van bekende verdelingen kan nabootsen en zowel zwaar-gestoorde als asymmetrische patronen kan volgen. In de praktijk betekent dit dat hetzelfde wiskundige raamwerk oogknipperartefacten in EEG, bewegingspieken in ECG en korrelige ruis in medische beelden kan beschrijven. Het team gaat verder door een speciale “scorefunctie” uit de ETWD af te leiden en deze in een snel signaalscheidingsalgoritme (FastICA) te verwerken. Die scorefunctie stuurt het algoritme richting de meest plausibele verborgen bronnen, waardoor signaal en ruis op een manier worden gescheiden die zich aanpast aan de werkelijke statistiek van de data.
De reiniger laten afstemmen door evolutie
Aangezien ETWD zo flexibel is, zou het handmatig kiezen van parameters zijn als proberen een complex instrument op gehoor af te stemmen in een drukke ruimte. Om dit te automatiseren gebruiken de onderzoekers een genetisch algoritme—een zoekprocedure geïnspireerd op natuurlijke selectie. Kandidaten voor parametersets worden behandeld als individuen in een populatie; de best presterende, beoordeeld op hoe goed ze bij de data passen, worden geleidelijk verfijnd over generaties. Deze evolutionaire stap voorkomt dat het proces vastloopt in slechte oplossingen en vereist geen berekening van gecompliceerde afgeleiden. Dezelfde optimalisatie past ook regels voor sparsity in het wavelet-domein aan, die kleine, door ruis gedomineerde coëfficiënten selectief verkleinen terwijl grote, structureel rijke coëfficiënten behouden blijven. Samen vormen ETWD, FastICA, genetische zoekoplossing en sparsity een enkele ruisonderdrukkingspijplijn die trainingvrij is maar sterk data-gedreven.

De methode bewijzen op hersenen, hart en beelden
Om de aanpak te testen passen de auteurs deze toe op drie verschillende typen biomedische data. Voor EEG reinigen ze opnames die verontreinigd zijn door spier- en oogartefacten en voeren daarna een piekdetectieroutine uit op de resultaten. De detectienauwkeurigheid stijgt van 71% in de ruisende data naar 94% na het denoisen met de sparsity-versterkte ETWD-methode, terwijl het aantal vals alarmen sterk daalt. Voor ECG evalueren ze hoe goed standaard hartslagdetectoren de karakteristieke R-pieken vinden. Na denoising stijgt de F1-score van de detector, een evenwicht tussen treffers en missers, van 0,89 naar 0,97, wat aangeeft dat cruciale hartslagen zowel beter behouden blijven als gemakkelijker te detecteren zijn. In medische beelden met toegevoegde Gaussiaanse, speckle- of Rician-ruis verbetert de methode consequent de piek signaal-ruisverhouding vergeleken met verschillende standaardfilters, en herstelt subtiele anatomische details trouwer en in minder tijd.
Opgewassen tegen moderne deep learning
Diepe neurale netwerken zijn populair geworden voor denoising, maar ze vereisen grote gelabelde datasets en aanzienlijke trainingstijd, en ze maken soms fijne structuren glad. De auteurs vergelijken hun raamwerk met convolutionele auto-encoders die zijn getraind op dezelfde EEG-, ECG- en beelddata. Over de taken heen evenaart of overtreft de op ETWD gebaseerde pijplijn deze diepe modellen op belangrijke kwaliteitsmaatstaven, terwijl het een aparte trainingsfase vermijdt. Het toont ook goede robuustheid wanneer het zonder herafstemming op volledig nieuwe datasets met andere protocollen wordt toegepast—de prestatie daalt slechts licht en overtreft nog steeds standaard op Gauss gebaseerde referenties, wat suggereert dat de methode redelijk goed overdraagbaar is tussen locaties.
Wat dit betekent voor patiënten en clinici
Kort gezegd levert dit werk een slimmer gum voor ruis in medische signalen. Door een zeer flexibele beschrijving van ruis te gebruiken en een evolutionair algoritme het automatisch te laten afstemmen, slaagt het raamwerk erin rommel weg te strippen terwijl kleine pieken, scherpe hartslagen en vage beeldranden behouden blijven—juist de kenmerken die vaak diagnostische waarde hebben. Het resultaat zijn duidelijkere EEG-sporen, schonere ECG-ritmes en scherpere medische beelden, bereikt zonder enorme trainingsverzamelingen of black-box modellen. Als dit breed wordt gevalideerd in klinische omgevingen, zou dit type adaptieve, trainingvrije denoising dagelijkse monitoringsapparatuur en ziekenhuissystemen betrouwbaarder kunnen maken, waardoor zowel mensen als algoritmen veiliger en met meer vertrouwen diagnoses kunnen stellen.
Bronvermelding: Sayedelahl, M.A., Farouk, R.M. & Adam, A.M. Enhancing biomedical signals through genetic algorithm optimized Exponentiated transmuted weibull denoising techniques. Sci Rep 16, 13409 (2026). https://doi.org/10.1038/s41598-026-46088-7
Trefwoorden: ruisonderdrukking van biomedische signalen, verwijdering van ruis in EEG en ECG, verbetering van medische beelden, onafhankelijke componentenanalyse, optimalisatie met genetisch algoritme