Clear Sky Science · nl
CSF1 reguleert ontsteking en apoptose bij tussenwervelschijfdegeneratie
Waarom rugpijn van diep in de wervelkolom begint
Hoge rug- en lage rugpijn is een van de meest voorkomende redenen waarom mensen een arts bezoeken of werk missen. Een groot deel van die pijn is terug te voeren op slijtage van de zachte kussentjes tussen de wervellichamen, de zogenaamde tussenwervelschijven. Deze studie stelt een verrassend eenvoudige vraag met grote implicaties: bestaat er één signaalmolecuul in het lichaam dat zowel ontsteking als celdood binnen deze schijven aanstuurt, en zou het een doelwit kunnen zijn voor eerdere diagnose of minder ingrijpende behandelingen?
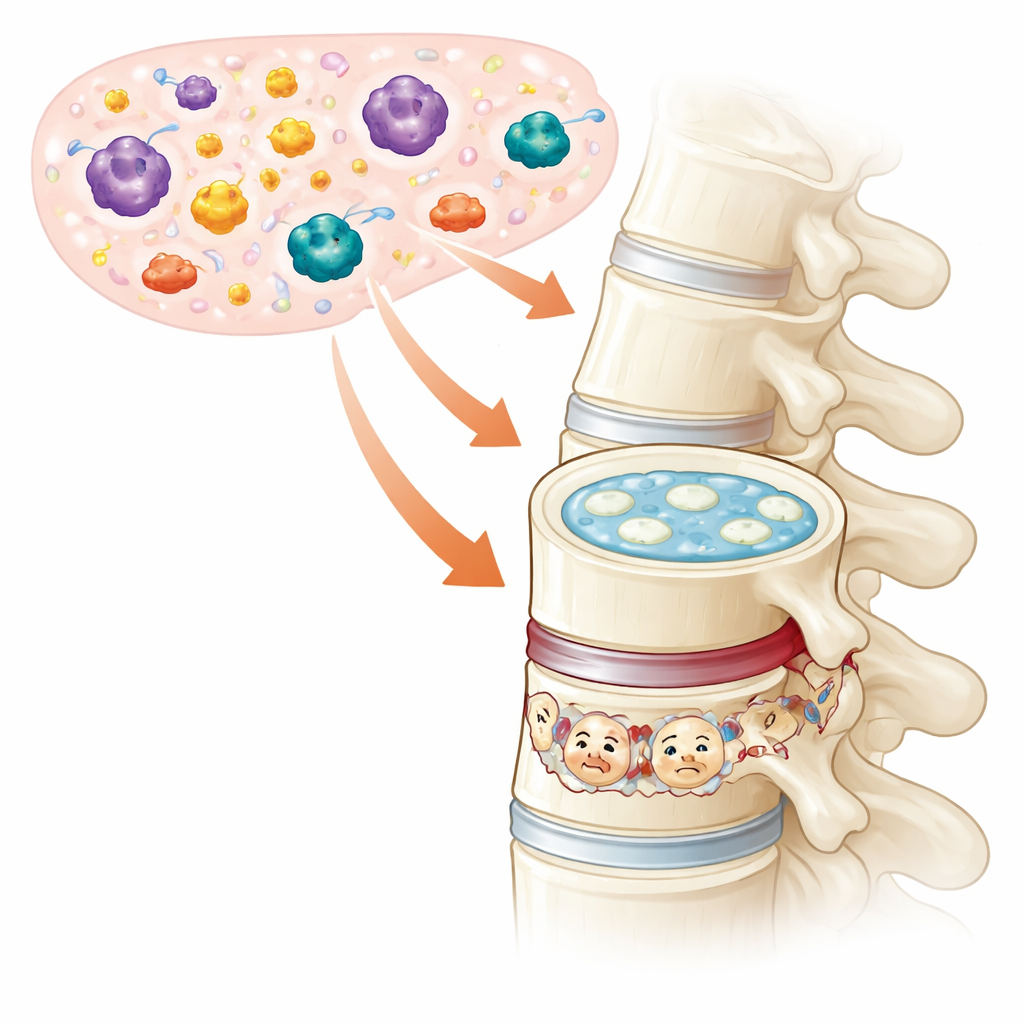
Een nadere blik op de schokdempers van de wervelkolom
Tussenwervelschijven fungeren als flexibele pads tussen aangrenzende wervels; ze laten ons buigen, draaien en de krachten van het dagelijks leven absorberen. In hun kern bevindt zich een gelachtige kern vol gespecialiseerde cellen die een veerkrachtige mix van collageen en andere matrixcomponenten in stand houden. Als deze cellen verzwakken, droogt de schijf uit, wordt dunner en kan uitpuilen of scheuren — een proces dat bekendstaat als tussenwervelschijfdegeneratie. Mensen met gevorderde degeneratie leven vaak met chronische pijn en beperkte beweeglijkheid, terwijl huidige therapieën vooral gericht zijn op symptoombestrijding in plaats van het stoppen of omkeren van de onderliggende schade.
Op zoek naar probleemveroorzakende genen in menselijke data
De onderzoekers begonnen met het doorzoeken van bestaande genetische gegevens van mensen met en zonder gedegenereerde schijven. Ze analyseerden twee grote datasets van genexpressie — in feite welke genen omhoog- of omlaaggereguleerd zijn in ziek weefsel en bloed vergeleken met gezond weefsel. Uit duizenden veranderende genen selecteerden ze 52 die in dezelfde richting verschooften in beide datasets. Onder deze gedeelde genen viel er één op: CSF1. CSF1 staat bekend om zijn invloed op immuuncellen en weefselherstel elders in het lichaam, dus het sterke signaal bij schijfdegeneratie suggereerde dat het een belangrijke coördinator van ontsteking en celsurvival in de wervelkolom zou kunnen zijn.
Hoe één signaal het vuur in de schijf kan aanwakkeren
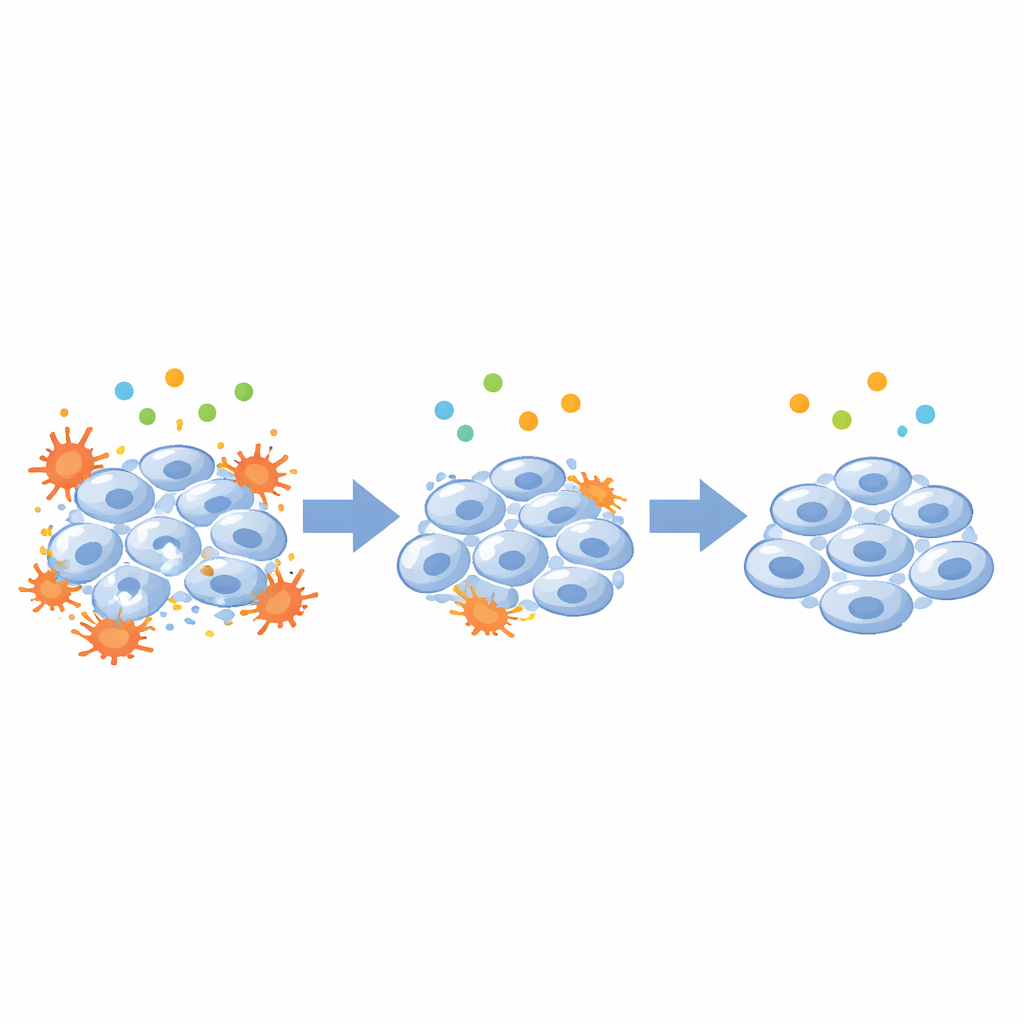
Om de rol van CSF1 directer te testen, werkten de onderzoekers met schijfcellen gekweekt in het laboratorium. Ze verwisselden nucleus pulposus-cellen — de sleutencellen in het centrum van de schijf — met een ontstekingsprikkel en zagen dat CSF1-niveaus stegen samen met klassieke ontstekingsmarkers en verhoogde celdood. Vervolgens gebruikten ze genetische instrumenten om CSF1 in deze cellen te onderdrukken. Toen CSF1 werd uitgeschakeld, daalden ontstekingsproteïnen en verschoof de balans tussen celdood en overleving in een beschermende richting: eiwitten die overleving bevorderen namen toe, terwijl die geassocieerd met zelfvernietiging afnamen. Parallelle computeranalyses van immuuncelpatronen suggereerden dat hogere CSF1 samenhangt met verschuivingen in veel typen immuuncellen, wat erop wijst dat dit ene signaal kan helpen een breder ontstekingsmilieu in degenererende schijven te orkestreren.
Sporen in het bloed: een mogelijke waarschuwingssignaal
Aangezien het nemen van monsters rechtstreeks uit schijven invasief is, zou een door bloed meetbare indicator veel praktischer zijn in de kliniek. De wetenschappers maten daarom CSF1-niveaus in het bloed van patiënten met uiteenlopende gradaties van schijfdegeneratie en bij gezonde vrijwilligers. Ze vonden dat mensen met ernstiger degeneratie hogere CSF1-waarden in hun bloed hadden, en dat CSF1 de neiging had te stijgen naarmate de ziekte ernstiger werd. Deze bevindingen roepen de mogelijkheid op dat CSF1 als een handig biomarker zou kunnen dienen — iets dat een eenvoudige bloedtest zou kunnen volgen om vroege schades aan schijven te signaleren of om te monitoren hoe goed behandelingen werken.
Wat dit betekent voor toekomstige zorg bij rugpijn
Gezamenlijk suggereren de resultaten dat CSF1 meer is dan een omstander: het lijkt bij te dragen aan ontsteking en celverlies in spinale schijven en weerspiegelt tegelijkertijd de ziekte-ernst in het bloed. Voor patiënten opent dit twee veelbelovende wegen. Ten eerste zouden CSF1 of zijn signaalpartners doelwitten kunnen worden voor nieuwe geneesmiddelen die schadelijke ontsteking in schijven kalmeren zonder grootschalige chirurgie. Ten tweede zouden bloedtests gebaseerd op CSF1 mensen kunnen helpen identificeren die risico lopen voordat onomkeerbare schade optreedt. Meer onderzoek, inclusief dierstudies en grotere patiëntengroepen, is nodig om deze mogelijkheden te bevestigen, maar deze studie legt belangrijk fundament voor het omzetten van een moleculair signaal in betere instrumenten voor diagnose en behandeling van lage rugpijn.
Bronvermelding: Zhang, F., Wu, W., Yuan, Y. et al. CSF1 regulates inflammation and apoptosis in intervertebral disc degeneration. Sci Rep 16, 10566 (2026). https://doi.org/10.1038/s41598-026-44984-6
Trefwoorden: tussenwervelschijfdegeneratie, lage rugpijn, CSF1, spinale ontsteking, biomarkers