Clear Sky Science · nl
Cross-indicatie-eiwitexpressieanalyse mogelijk maken met een gecureerde pan-kanker dataset en een afgestemde workflow
Waarom het vergelijken van kankereiwitten zo moeilijk is
Medicijnen tegen kanker richten zich steeds vaker op hetzelfde biologische doelwit in meerdere tumortypes, maar bepalen waar een doelwit het belangrijkst is, is niet eenvoudig. Grote publieke projecten zoals CPTAC van het National Cancer Institute leveren tegenwoordig gedetailleerde eiwitmetingen van duizenden tumoren. Deze metingen worden echter in verschillende centra, op verschillende momenten en met verschillende methodieken uitgevoerd. Daardoor kan de eenvoudige vraag “is dit eiwit hoger in longkanker dan in niertumoren?” misleidende antwoorden opleveren. Deze studie beschrijft een praktische, data-gedreven methode om deze complexe eiwitdatasets schoon te maken, aan te vullen en op elkaar af te stemmen, zodat eerlijke vergelijkingen tussen kankertypes mogelijk worden.
Een gedeelde kaart van kankereiwitten opbouwen
De auteurs beginnen met CPTAC’s pan-kankerverzameling: meer dan duizend tumoren en bijbehorende normale weefsels uit tien kankertypes, allemaal gemeten met massaspectrometrie. Deze experimenten leggen per monster duizenden eiwitten vast, maar niet altijd dezelfde eiwitten in elke tumor en niet met dezelfde verdeling tussen cohorten. Het team heeft daarom alle ruwe data opnieuw verwerkt met één uniforme rekenpipeline, zodat elk cohort consequent werd behandeld. Vervolgens concentreerden ze zich op een kernset van meer dan 10.000 “robust tot expressie gekomen” eiwitten—eiwitten die redelijk abundant zijn en zelden ontbreken in ten minste één kankertype—zodat vergelijkingen tussen kankertypes gebaseerd zijn op stabiele metingen in plaats van op gefragmenteerde signalen.
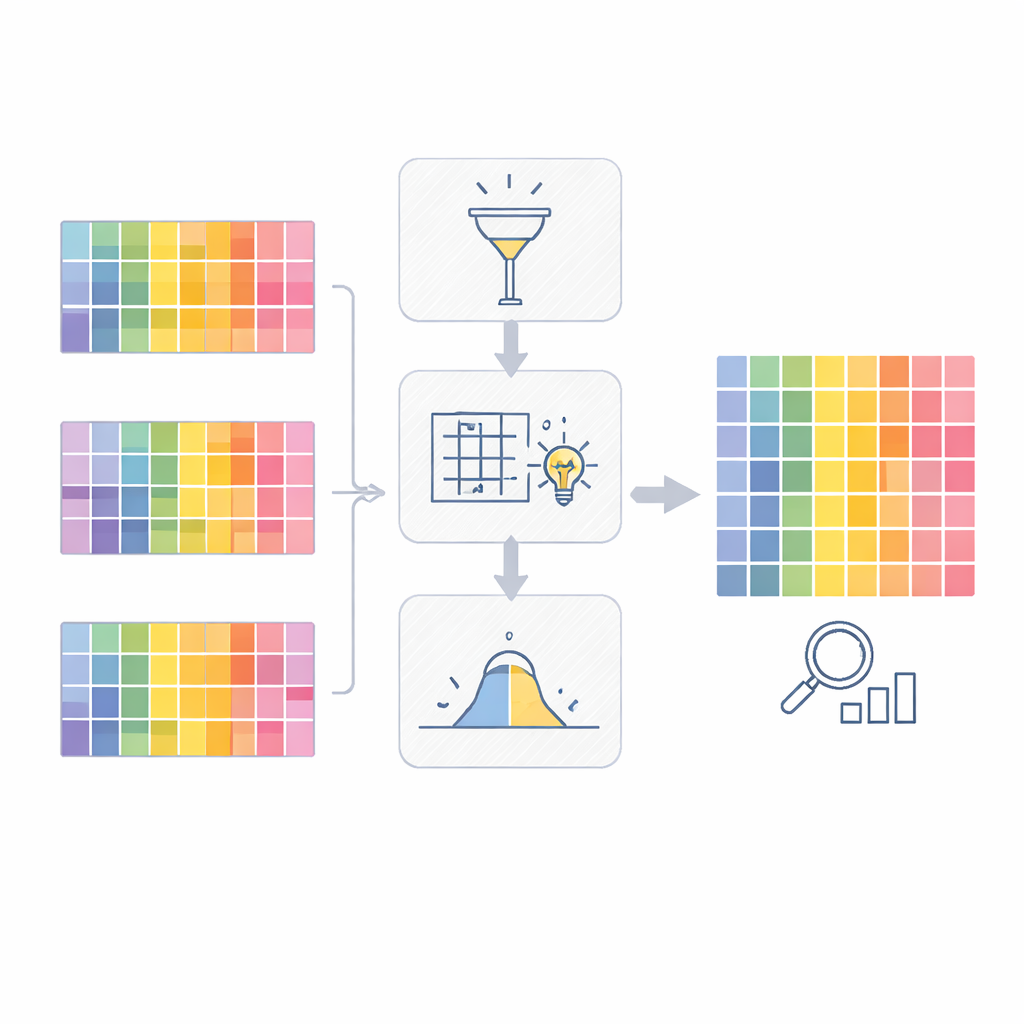
De lege plekken vullen zonder het beeld te vertekenen
Zelfs na zorgvuldige selectie blijven veel eiwitwaarden ontbreken. Sommige ontbreken willekeurig, vergelijkbaar met incidentele typfouten; andere ontbreken omdat het eiwitniveau onder de detectiegrens van het instrument lag. Als je alle missende waarden hetzelfde behandelt, kan dat tot bias leiden. Daarom gebruikte het team een “cohort-hybride” strategie die verschillende patronen van ontbrekende waarden per kankertype verschillend benadert. Voor eiwitten die waarschijnlijk alleen onderbemonsterd zijn, lenen ze informatie van vergelijkbare monsters om de ontbrekende waarden te schatten. Voor eiwitten die consequent te laag lijken om te detecteren, gebruiken ze een methode gericht op links-gecensureerde data, waarbij die waarden praktisch dichtbij de ondergrens van het instrument worden geplaatst. Deze genuanceerde aanpak heeft tot doel een realistisch beeld van eiwitniveaus te herstellen zonder kunstmatige verschillen te verzinnen.
Verdelingen vergelijkbaar maken tussen kankers
Nadat de gaten zijn opgevuld, blijft nog een probleem bestaan: sommige cohorten laten over het geheel hogere of meer variabele eiwitsignalen zien dan andere, grotendeels door technische factoren zoals sample-preparatie of instrumentkalibratie. Om dit te corrigeren zet het team eiwitintensiteiten om in een absolute-achtig meetniveau en test vervolgens twee normalisatiestrategieën. De ene, globale kwantielnormalisatie, dwingt alle monsters—over alle kankers en weefsels heen—om dezelfde algehele verdeling van eiwitwaarden te delen. De andere, ‘soepele’ kwantielnormalisatie, harmoniseert monsters binnen elk kankertype of weefsel terwijl verschillen tussen groepen behouden mogen blijven. Door variatiepatronen te onderzoeken en vele gevoeligheidscontroles uit te voeren, tonen de auteurs aan dat globale kwantielnormalisatie het beste ongewenste technische verschillen reduceert en tegelijk betekenisvolle biologische contrasten behoudt, zoals tumor‑versus‑normaal veranderingen.
Vergelijken met onafhankelijke RNA-data
Om te beoordelen of hun opgeschoonde eiwitdataset realistisch reageert over kankertypes heen, vergelijken de auteurs die met RNA-metingen uit The Cancer Genome Atlas. Voor een kleine set eiwitten waarvan de niveaus scherp samengaan met het corresponderende RNA over kankers heen, vergelijken ze hoe tumortypes rangschikken op eiwitexpressie versus RNA-expressie. Als de cross-kanker normalisatie succesvol is, zouden deze rangschikkingen overeen moeten komen. Inderdaad levert de combinatie van cohort-hybride imputatie en globale kwantielnormalisatie de hoogste rangovereenstemming tussen eiwit en RNA op, beter dan zowel ongenormaliseerde data als de alternatieve normalisatiemethode. Extra tests laten zien dat belangrijke biologische signalen—zoals welke eiwitten veranderen tussen tumoren en normaal weefsel en welke cellulaire paden aangepast zijn—grotendeels stabiel blijven na de volledige verwerkingsworkflow.
Wat dit betekent voor toekomstig kankeronderzoek
In eenvoudige bewoordingen verandert dit werk een rumoerige, ongelijkmatige verzameling eiwitmetingen in een betrouwbaardere, gedeelde referentie voor het vergelijken van kankers. Door zorgvuldig te beslissen welke eiwitten te behouden, hoe missende waarden aan te vullen en hoe verdelingen tussen studies op elkaar af te stemmen, creëren de auteurs een pan-kanker eiwitresource die beter overeenkomt met onafhankelijke RNA-data en de tumorbiologie behoudt. Deze gestandaardiseerde dataset en de open workflow kunnen onderzoekers helpen om medicijndoelen over vele tumortypes te rangschikken, kankerselectieve eiwitten te identificeren en nieuwe hypothesen voor behandeling te genereren—waardoor de route van grootschalige gegevens naar praktische vooruitgang in de oncologie wordt versneld.
Bronvermelding: Wang, J., Tian, X., Yu, W. et al. Enabling cross-indication protein expression analysis using a curated pan-cancer dataset and a tailored workflow. Sci Rep 16, 14623 (2026). https://doi.org/10.1038/s41598-026-44872-z
Trefwoorden: pan-kanker proteomica, normalisatie van eiwitexpressie, CPTAC, imputatie van ontbrekende gegevens, ontdekking van kankertargets