Clear Sky Science · nl
Statistische modellen ter karakterisering van heterogeniteit in stijfheid van colon-tumoren via representatieve atomic force microscopy-kaarten
Het voelen van de verborgen krachten bij darmkanker
Wanneer artsen colon-tumoren onder de microscoop bekijken, richten ze zich meestal op de vormen van cellen en de aanwezigheid van bepaalde moleculen. Tumoren hebben echter ook een minder zichtbaar kenmerk: hun stijfheid. Deze studie onderzoekt hoe het “gevoel” van colonkankergewebe — de zachtheid en hardheid op microschaal — samenhangt met leeftijd van de patiënt, tumoirstadium, genmutaties en andere klinische factoren. Door ultrasensitieve mechanische metingen te combineren met geavanceerde statistiek en machine learning, laten de onderzoekers zien dat tumorstijfheid rijke informatie bevat die mogelijk op termijn diagnose en behandeling kan sturen.
Waarom tumorstijfheid ertoe doet
Onze organen zijn niet zomaar zakken met cellen; ze bestaan uit een dragend netwerk, de extracellulaire matrix, doordrenkt met vloeistoffen en doorzet met bloedvaten en immuuncellen. Deze omgeving is niet passief. Ze duwt, trekt en biedt weerstand, en beïnvloedt zo hoe cellen groeien, bewegen en zelfs reageren op medicijnen. In veel vaste tumoren treedt verharding op naarmate collageen en andere vezels zich ophopen en meer kruisverbindingen vormen. Kanker-geassocieerde fibroblasten, gespecialiseerde steuncellen, drijven dit proces vaak aan. Een stijvere omgeving kan kankercellen ertoe aanzetten van identiteit te veranderen, invasiever te worden en soms therapie te weerstaan. Bij colorectale kanker suggereerden eerdere bevindingen dat stijfheid gekoppeld kan zijn aan veelvoorkomende mutaties en aan de agressiviteit van de tumor, maar er ontbrak een geïntegreerd, algemeen beeld.
Tumoren bevragen met een piepkleine mechanische vinger
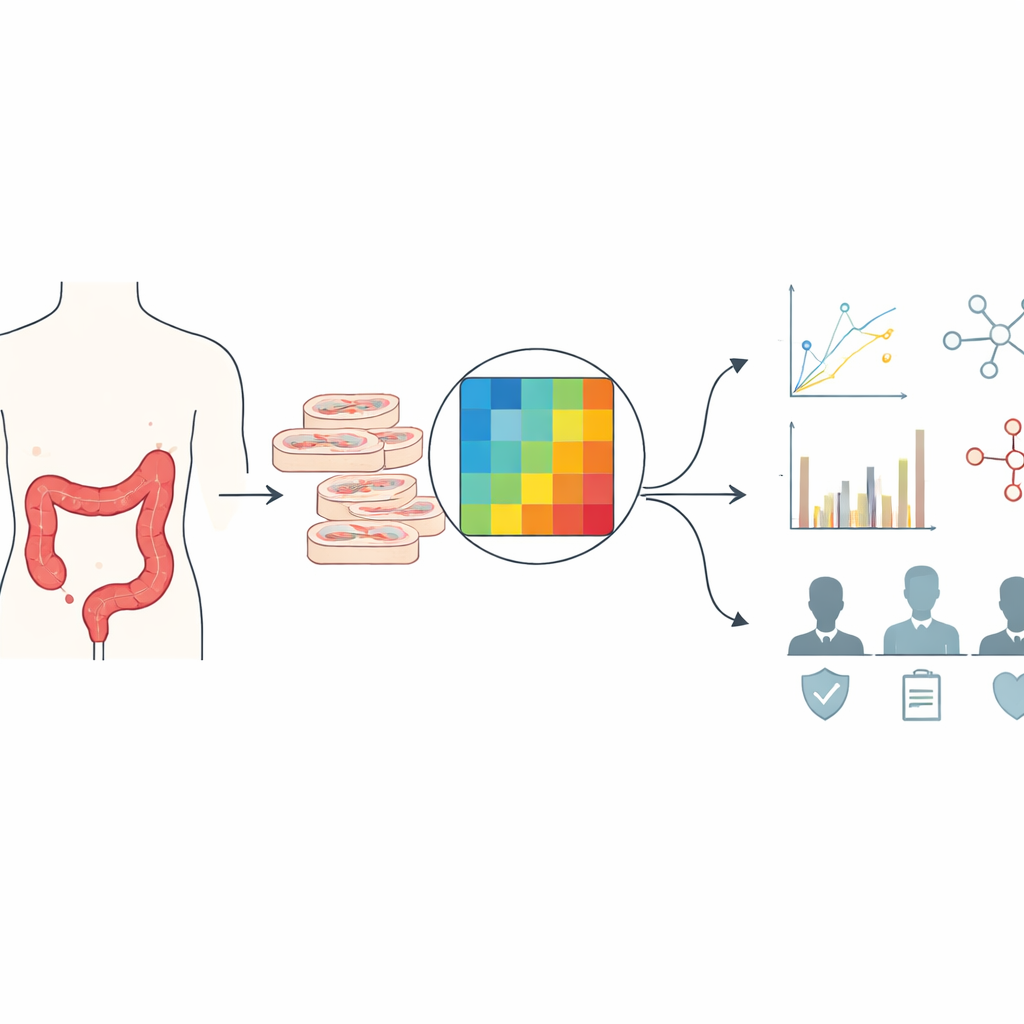
Om stijfheid te kwantificeren gebruikte het team atomic force microscopy, een techniek waarbij een microscopische veer met een afgeronde punt zachtjes in een weefseldun snede drukt. Door te meten hoeveel de punt buigt bij een gegeven kracht, kunnen ze de lokale stijfheid op elk punt berekenen. Van 18 patiënten met onbehandelde colonkanker bereidden ze dunne secties van tumor en naburig gezond weefsel en registreerden daarna kleine vierkante kaarten van stijfheid, elk bestaande uit een raster van indenteringspunten dat slechts 50 micrometer aan elke zijde besloeg. Deze kaarten legden aparte gebieden vast die werden gedomineerd door normaal epitheel, kankercellen, vezelig stroma of mengsels daarvan. Na zorgvuldige filtering van lawaaierige of onvolledige metingen analyseerden de onderzoekers 88 hoogkwalitatieve kaarten, elk met tientallen betrouwbare stijfheidswaarden.
Hoe gezond en tumorweefsel verschillen
De eerste vergelijking betrof het gezonde colonoppervlak in gebieden dicht bij de tumor en verder ervan. Beide toonden zeer zachte waarden en ondanks enige persoonsverschillen was er geen zinvol verschil tussen deze twee gezonde zones. Tumorweefsel vertelde echter een ander verhaal. Het kankerepitheel was duidelijk stijver dan het normale slijmvlies, en het omringende stroma — rijk aan collageen en steuncellen — was nog stijver. Gebieden waarin tumor en stroma gemengd waren, hadden een tussenniveau van stijfheid, zoals verwacht op grond van hun samengestelde samenstelling. Gesofisticeerde statistische modellen die rekening hielden met herhaalde metingen binnen patiënten bevestigden deze trends en benadrukten sterke individuele verschillen, wat suggereert dat ieders basisweefselmechanica en geschiedenis van tumorremodellering een eigen signatuur achterlaten.
Van kaarten naar medische aanwijzingen
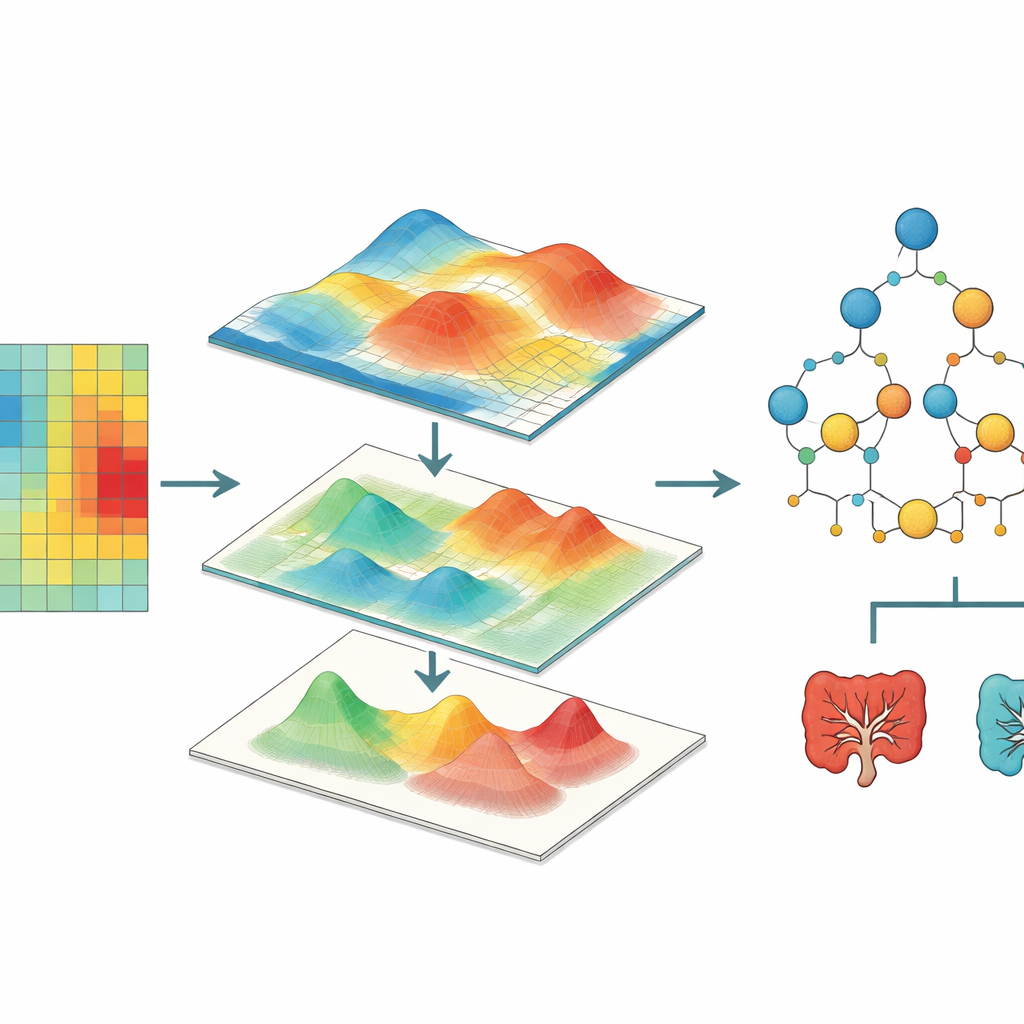
Vervolgens onderzochten de onderzoekers of de stijfheid van alle kankergedeelten samenhang vertoonde met klinische en genetische kenmerken. Met generalized linear mixed models vonden ze dat stijvere patronen geassocieerd waren met hogere leeftijd, een gevorderder tumoirstadium en de aanwezigheid van mutaties in RAS-genen, waarvan bekend is dat ze beïnvloeden hoe cellen mechanische signalen waarnemen en erop reageren. Tumoren aan de linker- en rechterkant van de darm, die biologisch en prognostisch verschillen, vertoonden ook onderscheiden stijfheidsgedrag. Een andere opmerkelijke associatie betrof microsatellietinstabiliteit, een fout in DNA-reparatie die een specifieke subtype van colorectale kanker kenmerkt. Om verder te gaan dan gemiddelde waarden zetten de onderzoekers elke stijfheidskaart om in een glad oppervlak, maten kenmerken zoals ruwheid en patchiness en voerden deze in random forest machine-learningmodellen. Deze modellen konden met matige nauwkeurigheid variabelen afleiden zoals tumoirstadium, RAS-mutatiestatus en of tumorcellen bloed- of lymfevaten waren binnengedrongen.
Wat dit voor patiënten betekent
Dit werk toont aan dat het mechanische landschap van colon-tumoren — hoe stijf ze zijn en hoe die stijfheid van punt tot punt varieert — informatie bevat over tumor-genetica, locatie en progressie. Door stijfheidskaarten als datarijke beelden te behandelen en moderne statistiek en machine learning toe te passen, schetsen de auteurs een kader dat uiteindelijk mechanische metingen in praktische biomarkers zou kunnen omzetten. Hoewel meer patiënten en fijnmazigere kaarten nodig zullen zijn, en de studie nog geen direct causaal verband bewijst, ondersteunt het de gedachte dat het gevoel van een tumor net zo belangrijk is als het uiterlijk. In de toekomst kan het combineren van stijfheidsprofilering met moleculaire tests artsen helpen colorectale kankers beter te classificeren en behandelingen af te stemmen op zowel de fysieke als de genetische identiteit van elke tumor.
Bronvermelding: Gadouas, G., Tosato, G., Costa, L. et al. Statistical models to characterize colon tumor stiffness heterogeneity through representative atomic force microscopy maps. Sci Rep 16, 14314 (2026). https://doi.org/10.1038/s41598-026-43396-w
Trefwoorden: darmkanker, tumorstijfheid, atomic force microscopy, tumormicro‑omgeving, machine learning in oncologie