Clear Sky Science · nl
Geïntegreerde multi-omicsanalyse identificeert en valideert endoplasmatisch reticulumstress- en mitofagie-gerelateerde biomarkers bij MASLD
Waarom gestreste levercellen van belang zijn voor de gezondheid van alledag
Metabole dysfunctie-geassocieerde steatotische leverziekte (MASLD) is tegenwoordig een van de meest voorkomende leveraandoeningen wereldwijd en hangt nauw samen met obesitas en type 2-diabetes. Bij MASLD hoopt vet zich geleidelijk op in de lever en kan dit uitmonden in ontsteking, littekenvorming en zelfs leverkanker. Deze studie kijkt diep in levercellen om te begrijpen hoe twee belangrijke vormen van celstress, en één regulatorische molecule genaamd NR4A1, die progressie zouden kunnen aansturen en kansen voor nieuwe behandelingen zouden kunnen openen.
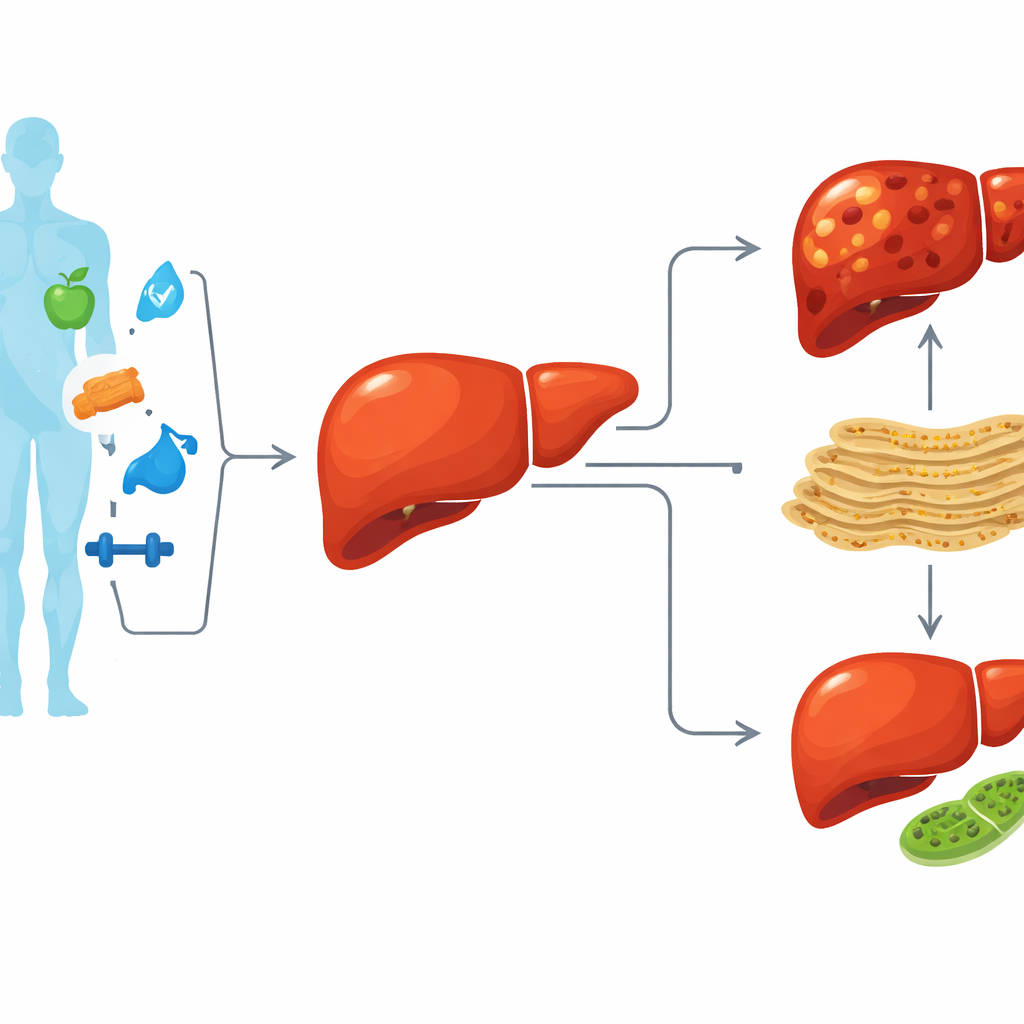
Vette lever als waarschuwingsteken voor het hele lichaam
MASLD is meer dan alleen een “vette lever”; het weerspiegelt een bredere verstoring in hoe het lichaam energie verwerkt. Wanneer de lever langdurig wordt overbelast met vet en voedingsstoffen, kan zij verschuiven van eenvoudige vetophoping naar ernstigere schade, waaronder ontsteking, fibrose, cirrose en leverkanker. De huidige therapieën richten zich vooral op dieet en leefstijl, wat helpt maar vaak niet voldoende is. Onderzoekers willen daarom de moleculaire schakelaars binnen levercellen begrijpen die het evenwicht doen kantelen van een gestrest-maar-aanpassend orgaan naar een orgaan dat geleidelijk faalt.
Twee gestreste celfabrieken in de lever
De auteurs richten zich op twee cruciale structuren binnen levercellen. De ene is het endoplasmatisch reticulum, een membraanachtige “fabriek” die eiwitten verwerkt. Wanneer dit orgaan overbelast raakt, treedt een toestand in die stress wordt genoemd; aanvankelijk helpt die cellen zich aan te passen, maar bij aanhoudende stress leidt het tot ontsteking en celschade. De ander is het mitochondrium, de energiecentrale van de cel, die gezond wordt gehouden door een opruimproces genaamd mitofagie, waarbij beschadigde energiecentrales selectief worden verwijderd. Bij MASLD staan zowel deze eiwitfabriek als de energiecentrales onder chronische druk, en kan het evenwicht tussen herstel en schade verloren gaan. De studie onderzoekt welke genen op het kruispunt liggen van deze stressreacties en de vetophoping in de lever.
Een centrale schakel vinden met big-databiologie
Het team combineerde meerdere lagen “omics”-data: bulk-genexpressie van leverweefsel van honderden patiënten, single-cell sequencing die individuele celtypen volgt, en geavanceerde computermethoden waaronder machine learning. Uit duizenden genen die gekoppeld zijn aan ER-stress en mitochondriale opruiming selecteerden zij een kleine set die actief is bij MASLD. Daarbij viel vooral één gen op: NR4A1. Dit gen kwam consistent lager tot expressie in de lever van MASLD-patiënten vergeleken met gezonde individuen, en de niveaus ervan konden aangetaste weefsels met hoge nauwkeurigheid van normale onderscheiden. In single-celldata bleek NR4A1 vooral belangrijk in macrofagen, de immuuncellen die de lever patrouilleren, waar de expressie afnam naarmate deze cellen verschoven van vroege, adaptieve toestanden naar meer agressieve, ontstekingsbevorderende staten.
Van celmodellen en muizen naar mogelijke medicijnen
Om verder te komen dan computervoorspellingen creëerden de onderzoekers vetachtige levercondities in humane levercel-lijnen door deze bloot te stellen aan een overschot aan vetzuren. Deze cellen stapelden vet op en toonden tegelijkertijd een duidelijke daling van NR4A1 op zowel RNA- als proteïneniveau. Vergelijkbare verminderingen werden gezien in de lever van muizen die een vetrijk dieet kregen en in weefselmonsters van MASLD-patiënten, waarbij NR4A1-niveaus verder daalden naarmate de ziekte vorderde richting cirrose en kanker. Analyse van genactiviteit suggereerde dat wanneer NR4A1 relatief hoog is, cellen sterkere stressadaptatie- en herstelroutes tonen, vooral die gekoppeld aan eiwitkwaliteitstoezicht en mitochondriale gezondheid. Tenslotte gebruikte het team virtuele screening om te zoeken naar kleine moleculen die NR4A1 zouden kunnen binden en stabiliseren, en identificeerde meerdere kandidaatverbindingen voor toekomstig experimenteel onderzoek.
Wat dit betekent voor toekomstige diagnose en behandeling
Gezamenlijk presenteren de bevindingen NR4A1 als een soort interne thermostaat die levercellen helpt zich aan te passen aan metabole overbelasting en gezondere eiwitfabrieken en energiecentrales te behouden. Wanneer deze thermostaat lager wordt gezet, lijken cellen vatbaarder om vet op te hopen, aanhoudende stress te ervaren en af te drijven naar chronische ontsteking en littekenvorming. Hoewel er meer werk nodig is om oorzaak en gevolg te bevestigen en om medicijnkandidaten in levende systemen te testen, suggereert deze studie dat het meten en uiteindelijk versterken van NR4A1-activiteit onderdeel zou kunnen worden van een gerichtere strategie om leververvetting te diagnosticeren, te monitoren en te behandelen voordat onomkeerbare stadia worden bereikt.
Bronvermelding: Chen, Q., Liu, L., Feng, J. et al. Integrated multi-omics analysis identifies and validates endoplasmic reticulum stress and mitophagy-related biomarkers in MASLD. Sci Rep 16, 12606 (2026). https://doi.org/10.1038/s41598-026-43311-3
Trefwoorden: leververvetting, celstress, mitochondriën, immuuncellen, biomarkers