Clear Sky Science · nl
FMCL: een transformer-gebaseerde feature-map classificatieleerbenadering voor verbeterde detectie van hersentumoren in MRI
Waarom het vroeg opsporen van hersentumoren belangrijk is
Hersentumoren worden vaak opgespoord met MRI-scans, maar zelfs ervaren radiologen kunnen moeite hebben wanneer tumoren klein, vaag of verborgen in ruisachtige beelden zijn. Zulke details missen kan de behandeling vertragen of leiden tot onnodige vervolgonderzoeken. Dit artikel introduceert een nieuwe computer‑visiemethode, Feature‑Map Contrast Learning (FMCL), die bedoeld is om computers hersen‑MRI’s beter te laten interpreteren—onderdeelgebieden te herkennen die verdacht zijn en misleidende visuele ruis te negeren.
Huidige tools en hun blinde vlekken
Traditionele computermethoden voor het lezen van MRI’s vertrouwen op handgemaakte beeldverwerking (zoals filtering en randdetectie) of op moderne deep‑learningmodellen zoals convolutionele neurale netwerken en transformers. Deze benaderingen hebben indrukwekkende vooruitgang geboekt, maar ze struikelen nog steeds bij tumoren met lage contrastwaarden, beelden met veel ruis en verschillen tussen scanners of ziekenhuizen. Veel modellen hebben ook zeer grote gelabelde datasets nodig en behandelen helderheid (intensiteit) en textuurverschillen (contrast) vaak als afzonderlijke of eenvoudig optelbare signalen. In de praktijk kan dat ertoe leiden dat het ene type signaal het andere overheerst, waardoor subtiele tumoren in de omgeving verdwijnen of valse alarmen ontstaan in gezond weefsel.
Een nieuwe manier om licht en textuur in balans te brengen
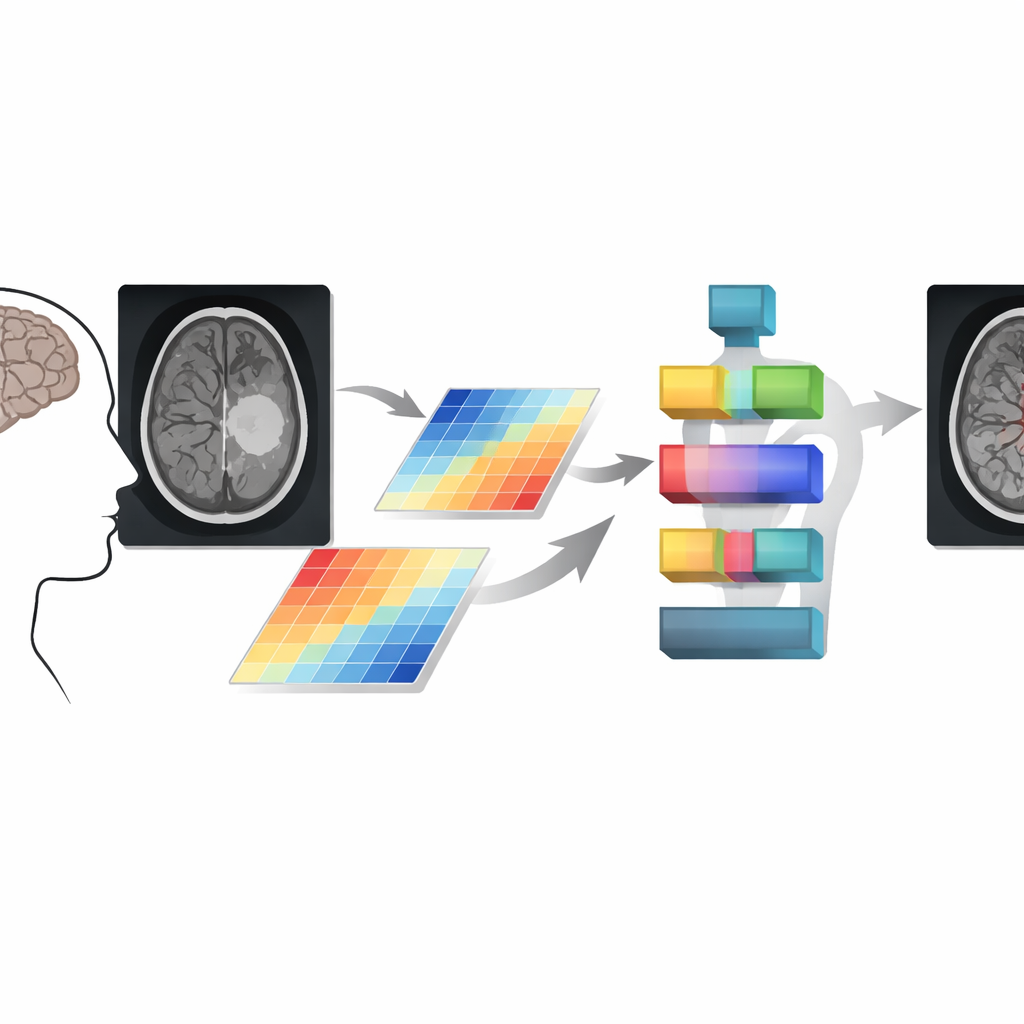
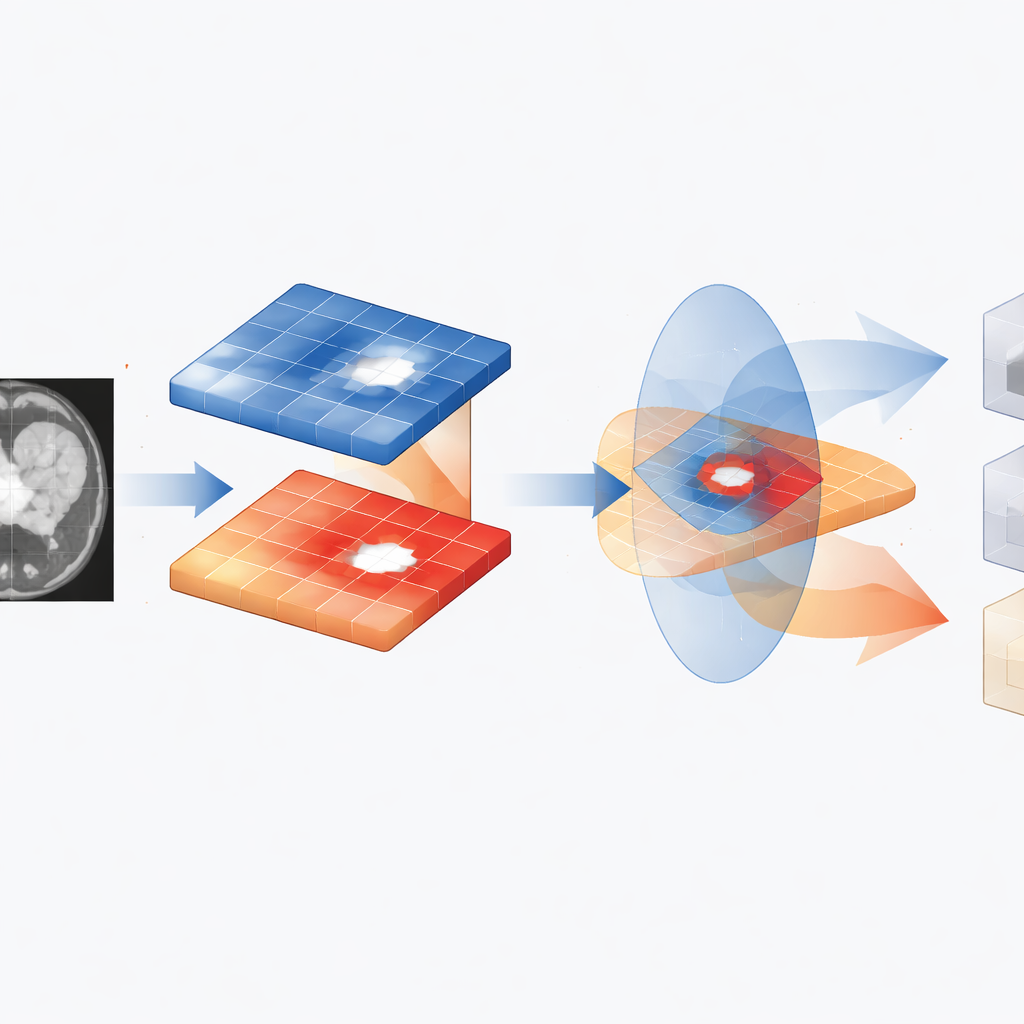
Het FMCL‑kader pakt dit aan door expliciet de relatie tussen contrast en intensiteit te beheren voor elke pixel in een MRI‑slice. De auteurs merken op dat in veel echte scans heldere gebieden vaak een lager contrast hebben en omgekeerd; tumorweefsel kan dit patroon op complexe manieren omkeren. FMCL bouwt wiskundige "feature maps" die niet alleen vastleggen hoe helder pixels zijn of hoe verschillend naburige pixels zijn, maar ook hoe deze eigenschappen in de tijd of tussen slices veranderen. Vervolgens dwingt het een inverse balans tussen contrast en intensiteit af, zodat geen van beide de beslissing domineert. Deze zorgvuldige afweging is ontworpen om subtiele tumoren zichtbaar te houden, zelfs wanneer het omringende hersenweefsel ongelijk verlicht of ruisachtig is.
Aandacht laten volgen waar de tumor zit
Zodra deze gereguleerde feature maps zijn geconstrueerd, voert FMCL ze in een transformer‑gebaseerd netwerk—een modeltype dat oorspronkelijk populair werd in taalverwerking en nu veel wordt gebruikt in visietaken. In plaats van naar ruwe beeldpatches te kijken, ontvangt de transformer reeds opgeschoonde en gebalanceerde kaarten, en gebruikt self‑attention om te leren welke hersengebieden onderling gerelateerd zijn. Het model splitst gebieden in drie hoofdtypen: duidelijk gezond achtergrondweefsel, duidelijk door tumor aangetast weefsel, en ambigue laag‑signaalgebieden. Daarna voert het een tweede controle uit op aangrenzende gebieden, waarbij naburige pixels worden vergeleken en gladgestreken met een gespecialiseerde SoftMax‑stap. Deze extra fase helpt ervoor te zorgen dat tumorranden continu zijn en dat kleine ruisflikkeringen niet voor ziekte worden aangezien.
Training, testen en prestaties
Om FMCL te evalueren gebruikten de auteurs een openbare Kaggle‑dataset met 3.264 hersen‑MRI‑afbeeldingen ingedeeld in vier groepen: geen tumor, glioma, meningeoom en hypofysetumor. Beelden werden voorbewerkt om grootte, helderheid en ruis te standaardiseren voordat ze werden gebruikt voor training. Het model werd vergeleken met meerdere sterke deep‑learning baselines, waaronder hybride capsule‑en‑CNN netwerken en beeldclassificeerders met hoge capaciteit. Over standaardmaatstaven zoals nauwkeurigheid, precisie, sensitiviteit en recall presteerde FMCL consequent beter. Het verbeterde de nauwkeurigheid met ongeveer negen procentpunten en verlaagde de gemiddelde classificatiefout met grofweg 11–16% vergeleken met eerdere methoden, terwijl de rekentijd per afbeelding binnen een bereik bleef dat geschikt is voor klinisch gebruik.
Wat dit betekent voor patiënten en klinieken
Voor leken is FMCL vergelijkbaar met het geven van een MRI‑leesassistent een betere bril en een meer gedisciplineerde manier van aandacht schenken. Door de weging van helderheid en textuur in balans te brengen en grenzen tussen aangrenzende gebieden dubbel te controleren, is het systeem minder geneigd moeilijke tumoren te missen of overdreven te reageren op onschuldige variaties. Hoewel het geen radiologen vervangt, kan het fungeren als een tweede lezer die verdachte gebieden markeert en snellere, zekerder beslissingen ondersteunt. De auteurs merken op dat er uitdagingen blijven voor zeer kleine of extreem vage tumoren, maar hun resultaten suggereren dat zorgvuldig ontworpen feature‑map learning computerondersteunde detectie van hersentumoren betrouwbaarder en nuttiger kan maken in echte ziekenhuizen.
Bronvermelding: Alanazi, T.M. FMCL: a transformer-based feature-map classifier learning approach for enhanced brain tumor detection in MRI. Sci Rep 16, 12571 (2026). https://doi.org/10.1038/s41598-026-42450-x
Trefwoorden: hersentumor MRI, medische beeldanalyse, deep learning, transformer modellen, tumordetectie