Clear Sky Science · nl
Onzekerheidsbewust feature‑gewogen ensemblekader voor voorspelling van hartziekten
Waarom het vroeg signaleren van hartproblemen ertoe doet
Hartziekten zijn nog steeds de belangrijkste doodsoorzaak wereldwijd, maar de meeste mensen worden pas gediagnosticeerd nadat symptomen ernstig zijn geworden. Artsen gebruiken steeds vaker computerprogramma’s om routinetesten en medische dossiers te doorzoeken op vroege waarschuwingssignalen die mensen gemakkelijk kunnen missen. Veel huidige kunstmatige‑intelligentietools gedragen zich echter als overmoedige leerlingen: ze geven een enkel ja‑of‑nee‑antwoord zonder toe te geven wanneer ze onzeker zijn. Dit artikel presenteert een slimmer systeem dat niet alleen nauwkeuriger hartziekten voorspelt, maar ook weet wanneer het zijn vinger moet opsteken en in feite zegt: “Ik ben niet zeker—controleer dit alstublieft nog eens.” 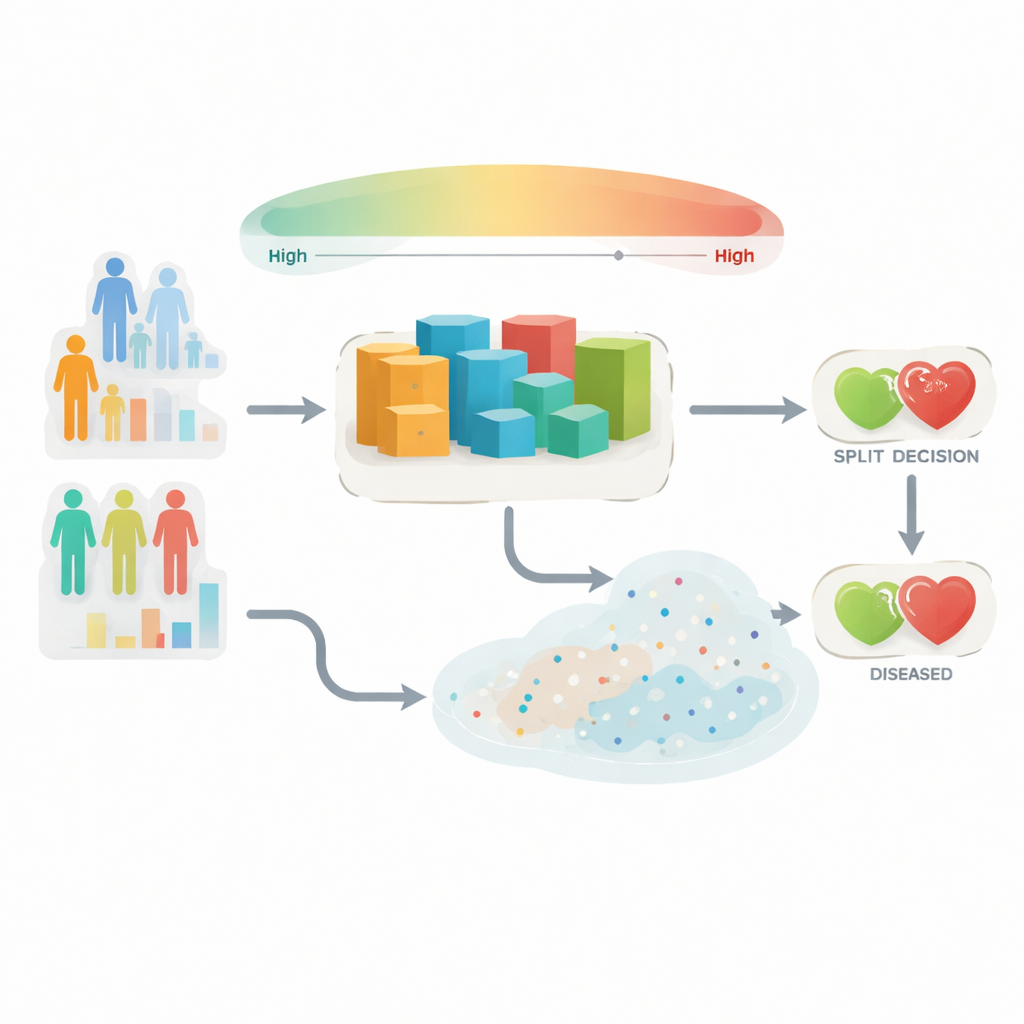
Waar hedendaagse slimme hulpmiddelen tekortschieten
De meeste bestaande voorspellingssystemen voor hartproblemen leren van tabellen met patiëntgegevens—zoals leeftijd, bloeddruk, cholesterol en pijn op de borst—en passen vervolgens machine‑learningmodellen toe om te beoordelen wie risico loopt. Twee grote zwaktes beperken hun bruikbaarheid in de kliniek. Ten eerste behandelen ze doorgaans elk invoerelement als even belangrijk. In werkelijkheid wegen sommige factoren veel zwaarder dan andere, en zwakkere maar toch nuttige signalen kunnen in het lawaai verdrinken. Ten tweede geven de meeste systemen geen indicatie van onzekerheid; ze leveren een enkele kans‑waarde of klasse‑label, zelfs wanneer de onderliggende gegevens verwarrend zijn. In de geneeskunde met hoge inzet kan dat soort blinde zekerheid leiden tot gemiste diagnosen of onnodige alarmen.
Het probleem in duidelijkere delen uiteenrafelen
De auteurs stellen een benadering voor die ze het Uncertainty‑Aware Feature‑Weighted Ensemble (UAFE) noemen om beide beperkingen aan te pakken. De methode begint met het rangschikken van alle klinische metingen op basis van hoe informatief ze zijn voor het detecteren van hartziekte, met behulp van een bekend boomgebaseerd algoritme als leidraad. Vervolgens splitst het deze metingen in drie groepen: zeer informatieve, matig informatieve en long‑tail kenmerken die mogelijk alleen in speciale gevallen helpen. Verschillende voorspellingsmodellen worden getraind op verschillende combinaties van deze groepen. Sommige richten zich alleen op de sterkste signalen, terwijl andere een breder beeld krijgen dat ook zwakkere patronen omvat. Door deze gespecialiseerde en algemene modellen te mengen, kan het systeem zowel duidelijke risicofactoren als subtiele combinaties vastleggen die alleen voor bepaalde patiënten van belang zijn.
Het systeem leren te twijfelen
Zodra het ensemble van modellen is getraind, let UAFE nauwkeurig op hoeveel de modellen het eens zijn met elkaar voor elke nieuwe patiënt. Als alle modellen vergelijkbare risicoschattingen geven, beschouwt het systeem dat geval als betrouwbaar en combineert hun meningen met gewichten gebaseerd op eerdere prestaties. Als de modellen sterk van mening verschillen, interpreteert UAFE dit als hoge onzekerheid. In die situaties vermindert het doelbewust de invloed van elk individueel model zodat geen overmoedige uitschieter de eindbeslissing domineert. Voor vooral twijfelachtige gevallen gaat het systeem een stap verder: het kijkt naar een kleine buurt van eerdere patiënten met vergelijkbare metingen en controleert hoeveel van hen daadwerkelijk hartziekte hadden. Deze lokale vergelijking fungeert als een second opinion die grensgevallen in een veiligere richting kan duwen. 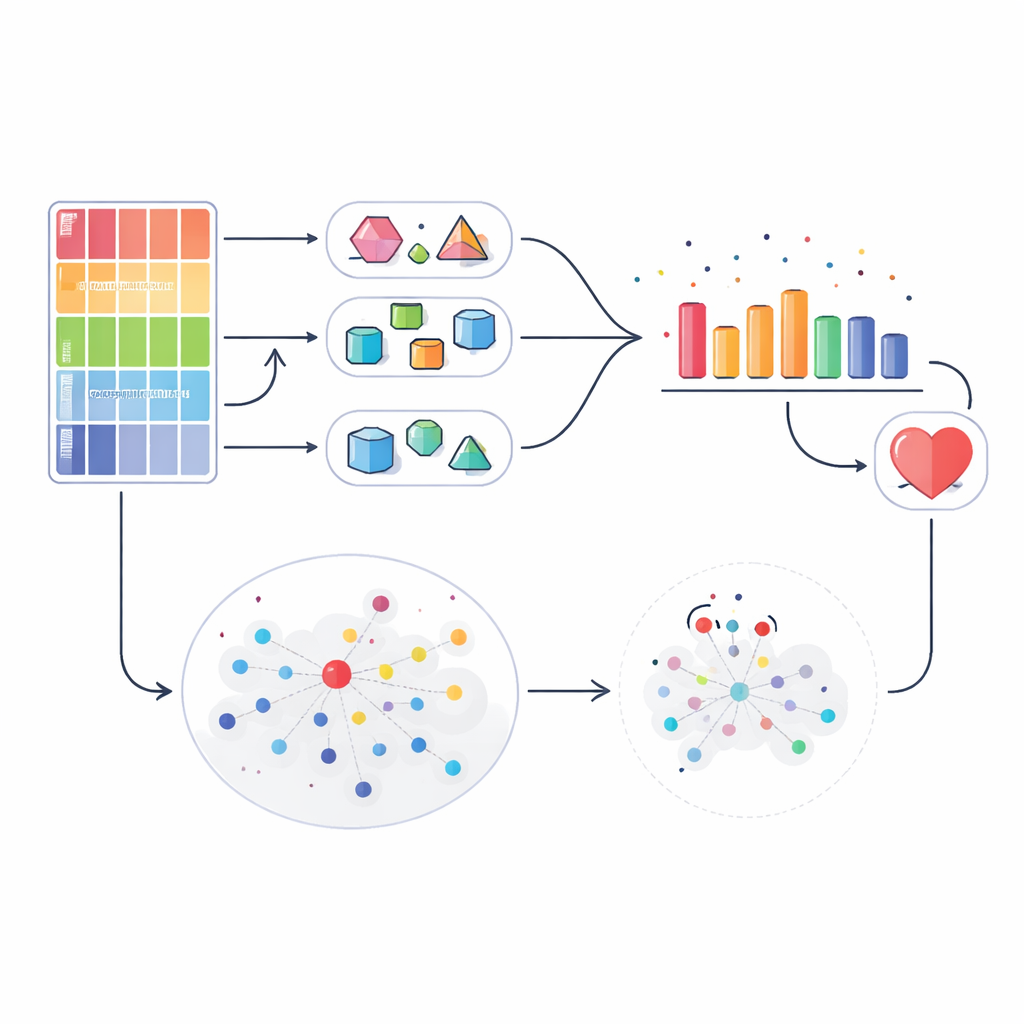
Hoe goed het nieuwe idee in de praktijk werkt
De onderzoekers testten UAFE op een veelgebruikt hartziektedataset en vergeleken het met standaardmethoden, waaronder logistische regressie, verschillende populaire boomgebaseerde modellen, een deep‑learning‑systeem en een conventioneel stemensemble. Over vijf gangbare kwaliteitsmaten behaalde UAFE de beste resultaten, met ongeveer 87% algehele nauwkeurigheid en een bijzonder sterke capaciteit om echte hartziektegevallen te detecteren terwijl valse alarmen beperkt bleven. Het halveerde bijna het aantal gemiste diagnosen vergeleken met sterke individuele modellen. Het team onderzocht ook hoe gevoelig de methode is voor de keuze van interne instellingen, zoals hoe kenmerken worden gegroepeerd en hoeveel gevallen als “onzeker” worden behandeld, en vond dat de prestaties robuust bleven over een breed scala aan waarden.
Betrouwbaar blijven in verschillende ziekenhuizen
Een veelgehoorde zorg bij AI‑hulpmiddelen is dat ze mogelijk alleen goed presteren op de gegevens waarop ze getraind zijn en falen wanneer ze naar een nieuw ziekenhuis met iets andere patiënten of registratiegewoonten worden verplaatst. Om dit te onderzoeken voerden de auteurs een leave‑one‑center‑out‑analyse uit over vier internationale klinische locaties. In elke ronde trainden ze UAFE op drie centra en testten het op het vierde, waarmee ze inzet in een nieuwe kliniek nabootsten. Het kader versloeg consequent een sterk basismodel en hield een gezonde marge in zijn vermogen om patiënten met en zonder hartziekte te scheiden. Dit suggereert dat het onzekerheidsbewuste ontwerp het systeem helpt te voorkomen dat het zich vastklampt aan eigenaardigheden van één enkel ziekenhuis en in plaats daarvan meer universele ziektepatronen oppikt.
Wat dit betekent voor patiënten en artsen
In gewone taal laat de studie zien dat het mogelijk is om een computerassistent te bouwen die niet alleen nauwkeuriger het risico op hartziekte voorspelt, maar ook weet wanneer zijn eigen oordeel wankel kan zijn. Door extra aandacht te besteden aan de meest veelzeggende medische details, meerdere complementaire modellen te combineren en grensgevallen te controleren aan de hand van vergelijkbare patiënten, verkleint UAFE de kans dat mensen met ernstige hartproblemen onopgemerkt blijven. Tegelijkertijd kan de ingebouwde onzekerheidsscore worden gebruikt om gevallen te markeren die nader menselijk onderzoek verdienen in plaats van automatische acceptatie. Hoewel het systeem nog op grotere en meer gevarieerde patiëntengroepen getest moet worden en uitgebreid moet worden naar rijkere gegevens zoals beelden en hartritmetracés, vormt het een concrete stap richting AI‑hulpmiddelen waarop clinici kunnen vertrouwen—niet alleen voor antwoorden, maar ook voor eerlijke inschattingen van zekerheid.
Bronvermelding: Wang, X., Fan, Y., Yu, M. et al. Uncertainty-aware feature-weighted ensemble framework for heart disease prediction. Sci Rep 16, 13321 (2026). https://doi.org/10.1038/s41598-026-42419-w
Trefwoorden: voorspelling van hartziekten, medische AI, ensemble learning, diagnostische onzekerheid, klinische besluitvorming