Clear Sky Science · nl
Tumor-geassocieerde epilepsie en hoge expressie van xCT vormen het proteoom van IDH-wildtype glioblastoom
Wanneer hersentumoren aanvallen uitlokken
Veel mensen zijn verbaasd te horen dat toevallen een van de meest voorkomende eerste tekenen van een hersentumor zijn. Tot acht van de tien patiënten met bepaalde gliomen zullen tijdens hun ziekte epilepsie ervaren. Deze studie stelt een praktische vraag met concrete gevolgen voor patiënten en hun naasten: wat is het aan sommige tumoren dat het omliggende brein elektrisch zo instabiel maakt, en kan die kennis leiden tot betere, meer gerichte anti-aanvalbehandelingen?
Signalen uit balans
Toevallen bij patiënten met een hersentumor hangen sterk samen met glutamaat, een boodschapperstof die zenuwcellen exciteert. Onder gezonde omstandigheden regelen hersencellen zorgvuldig hoeveel glutamaat wordt vrijgegeven en ruimen ze het snel op na elk signaal. Gliomen, aggressieve tumoren die uit ondersteunende hersencellen groeien, kunnen dit evenwicht verstoren. Ze kunnen te veel glutamaat in de extracellulaire ruimte brengen, waardoor nabijgelegen netwerken overactief raken en tot aanvallen leiden, terwijl dat ook de groei en invasie van de tumor zelf bevordert.
De transporteiwitten bij de poort
De glutamaatniveaus rond tumorcellen worden grotendeels beheerst door “transporters”, kleine proteïnemachines die aminozuren in en uit cellen verplaatsen. De onderzoekers concentreerden zich op vier hiervan: xCT en zijn partner CD98, die hoofdzakelijk glutamaat exporteren, en EAAT2 en ASCT1, die vooral helpen het op te ruimen. Ze onderzochten tumorstalen van 87 patiënten waarvan de gliomen met moderne genetische methoden waren geclassificeerd, en vroegen hoe de transporter-niveaus verschilden tussen mensen met en zonder tumor-gerelateerde epilepsie. Daarnaast voerden ze een diepgaande eiwitanalyse, of proteomische analyse, uit in een subset van glioblastoomstalen om te zien hoe aanvallen en hoge xCT-waarden het bredere moleculaire landschap van deze tumoren hervormen.
Wat tumoren vatbaar voor aanvallen onderscheidt
Gliomen van patiënten met epilepsie vertoonden hogere hoeveelheden van de opname-transporters EAAT2 en ASCT1, terwijl de exporttransporter xCT een zwakkere, meer variabele toename liet zien. Eén transporter, CD98, neigde lager te zijn wanneer aanvallen aanwezig waren. Vooral opvallend was ASCT1: tumoren met hoge ASCT1-waarden waren veel vaker gekoppeld aan epilepsie, wat suggereert dat dit eiwit als biomarker voor aanvalsgeneigde gliomen zou kunnen dienen, ook al richt geen enkel medicijn zich op dit eiwit. Het team bevestigde veel van deze patronen in onafhankelijke genetische datasets van andere patiëntengroepen, wat de gedachte ondersteunt dat transporteronevenwichten een reproduceerbaar kenmerk zijn van tumor-geassocieerde epilepsie.
Hoe xCT de innerlijke wereld van de tumor vormt
Bij nadere beschouwing van 16 glioblastoomstalen vergeleken de onderzoekers de volledige eiwitprofielen van tumoren met en zonder epilepsie, en keken ze vervolgens naar die met bijzonder hoge of lage xCT-niveaus. Tumoren van patiënten met aanvallen lieten veranderingen zien in meer dan 200 eiwitten, veel betrokken bij de verwerking van neurotransmitters, aminozuren en vetten. Binnen de aanvalsgroep hadden tumoren met sterke xCT-expressie een nog onderscheidender eiwitsignatuur. Deze tumoren waren niet alleen verrijkt voor glutamaatgerelateerde processen maar ook voor routes die samenhangen met myeline (de isolatie rond zenuwvezels) en synaptische plasticiteit, het vermogen van het brein om verbindingen te herschikken. Met andere woorden, hoge xCT leek een specifiek ‘bedradings- en metabolisme’-patroon op de tumor en zijn micro‑omgeving af te drukken.
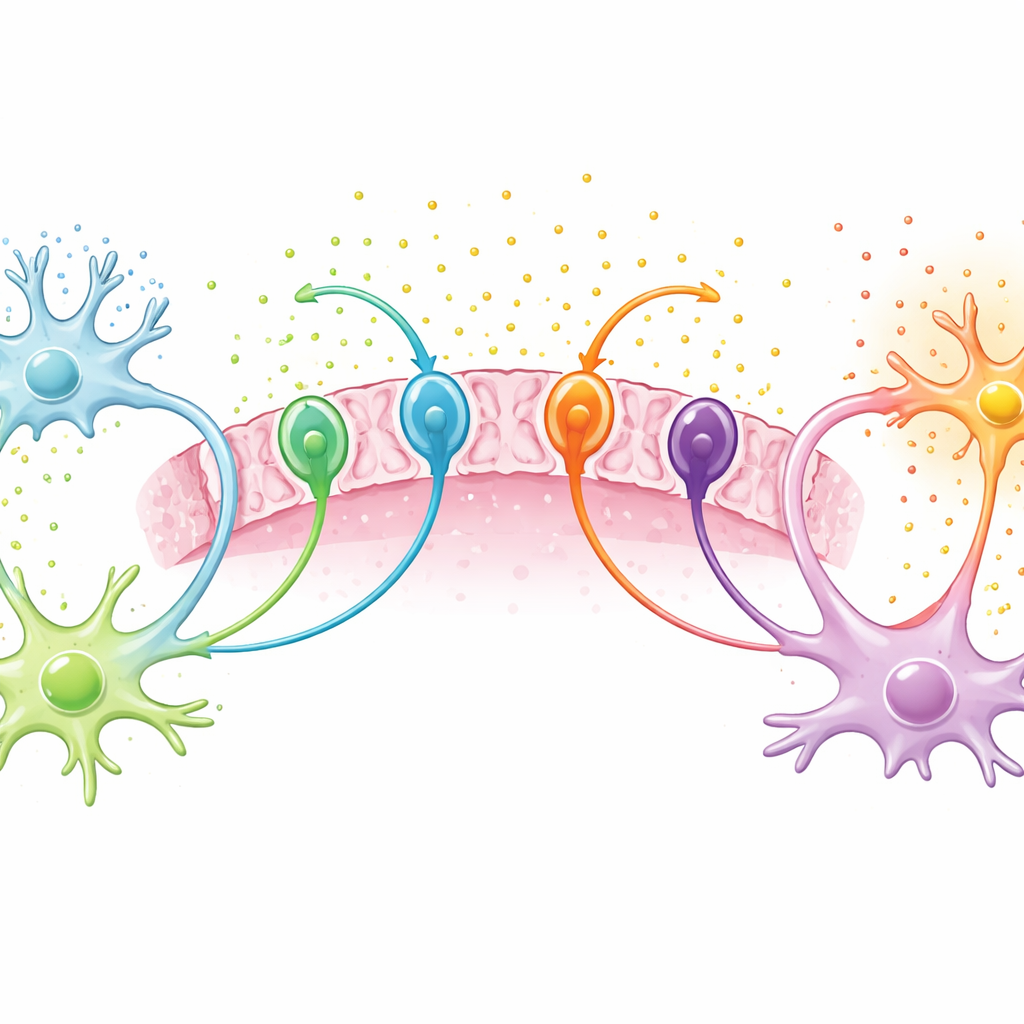
Wat het betekent voor patiënten
Men zou verwachten dat tumoren die aanvallen veroorzaken ook de overleving verkorten, maar dat bleek hier niet het geval. Over het geheel leefden patiënten met epilepsie langer, grotendeels omdat aanvallen vaker voorkwamen bij tumoren met specifieke genetische veranderingen (IDH-mutaties) die al bekendstaan als voorspellers van een betere uitkomst. Wanneer tumoren werden gegroepeerd naar deze genetica, had noch epilepsie zelf, noch de niveaus van de vier transporters een duidelijk effect op de overleving. De studie wijst daarom minder op prognose en meer op behandeling: ze benadrukt glutamaattransporters—vooral xCT, EAAT2 en ASCT1—als sleutelvormers van de aanvalsgeneigde tumoromgeving. Aangezien sommige van deze eiwitten al beïnvloedbaar zijn met bestaande geneesmiddelen en andere toekomstige doelwitten kunnen worden, kan het in kaart brengen van hun effecten op het tumorproteoom de ontwikkeling van preciezere anti‑aanvalsstrategieën voor mensen met gliomen sturen.
Bronvermelding: Divé, I., Schäfer, J.A., Weber, K.J. et al. Tumor-associated epilepsy and high expression of xCT shape the proteome of IDH-wildtype glioblastoma. Cell Death Discov. 12, 180 (2026). https://doi.org/10.1038/s41420-026-03029-7
Trefwoorden: glioblastoom, hersentumor epilepsie, glutamaattransporters, xCT, proteomica