Clear Sky Science · nl
Richten op oncogeen-geïnduceerde senescentie in ETV6::RUNX1 pre-leukemische cellen
Verborgen zaden van kinderleukemie
De meeste kinderen bij wie leukemie wordt vastgesteld, krijgen de diagnose pas als de ziekte al duidelijk aanwezig is. Toch begint het voor velen jaren eerder, met een kleine populatie veranderd bloedcellen die onopgemerkt in het lichaam blijven. Deze studie onderzoekt waarom die “pre-leukemische” cellen zo lang kunnen overleven, hoe ze later kanker kunnen aanjagen en of we ze kunnen verwijderen voordat ze schade veroorzaken—wat een voorproefje biedt van echt preventieve kankertherapie.
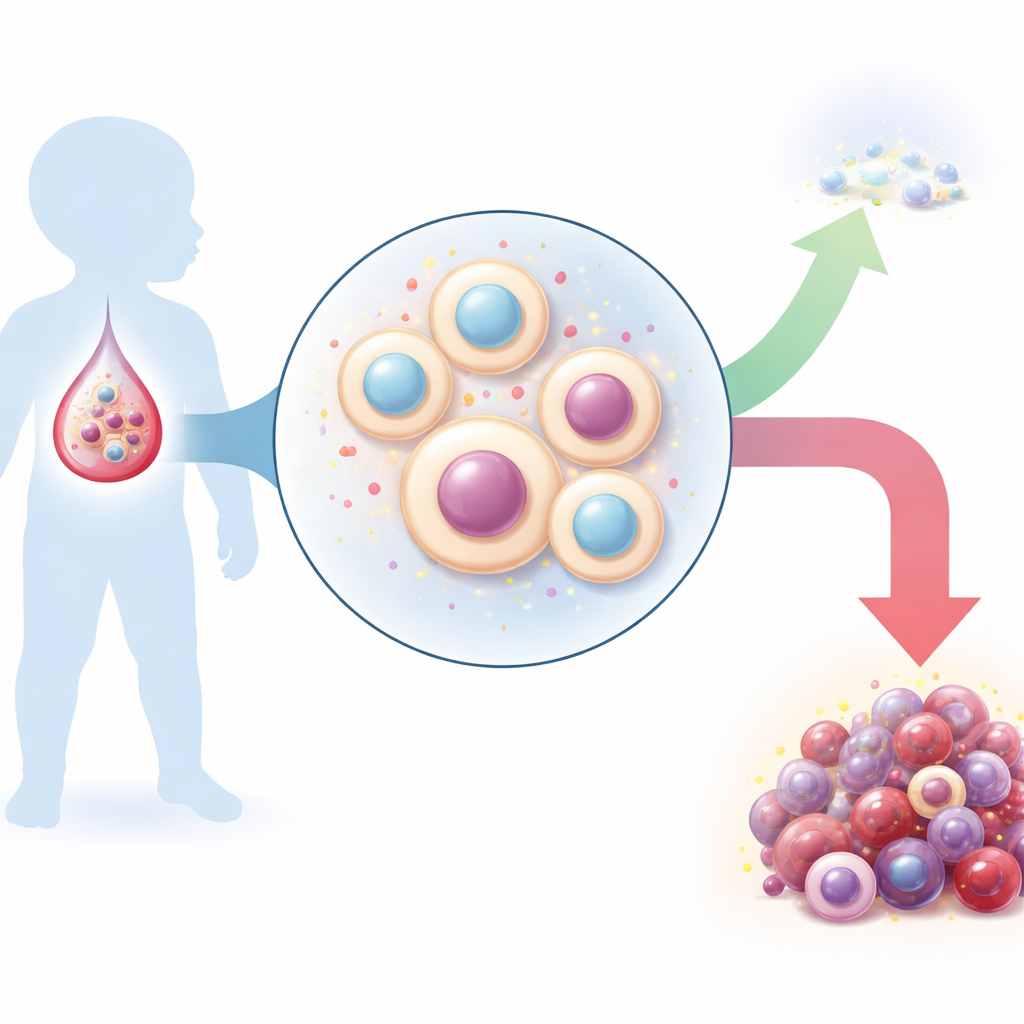
Een stille wijziging vóór de geboorte
Bij sommige pasgeborenen fuseert een kleine genetische herschikking twee genen, ETV6 en RUNX1, tot één hybride. Deze ETV6::RUNX1-fusie komt in het bloed van 2–5% van gezonde baby’s voor, maar slechts ongeveer 1% van deze kinderen ontwikkelt later een veelvoorkomende vorm van kinderlijke bloedkanker, B‑cel precursor acute lymfatische leukemie. Het fusiegen vormt abnormale vroege B‑cel voorlopers die deels rijpen en daarna stilvallen. Ze kunnen jaren aanhouden zonder symptomen te veroorzaken en vormen zo een verborgen reservoir van pre-leukemische cellen dat later aanvullende mutaties kan opnemen en kan transformeren tot volledig ontwikkelde leukemie.
Wanneer een kankergen cellen verouderd maakt
In plaats van simpelweg ongecontroleerde groei aan te jagen, duwt de ETV6::RUNX1-fusie cellen in een senescentie-achtige toestand—iets wat lijkt op cellulaire ouderdom. Met een muis pro‑B-cellijn en een transgene muismodel vonden de onderzoekers dat cellen die de fusie tot expressie brachten groter en platter werden en hun celcyclus vertraagden. Ze toonden hoge activiteit van een klassiek verouderingsmarker-enzym, produceerden teveel reactieve zuurstofsoorten en scheidden een mengsel van inflammatoire moleculen uit dat bekendstaat als het senescentie-geassocieerde secretiepatroon. Deze veranderingen weerspiegelen een proces dat oncogeen-geïnduceerde senescentie wordt genoemd, waarbij een vroeg kankerveroorzakend gebeuren paradoxaal genoeg cellen dwingt te stoppen met groeien.
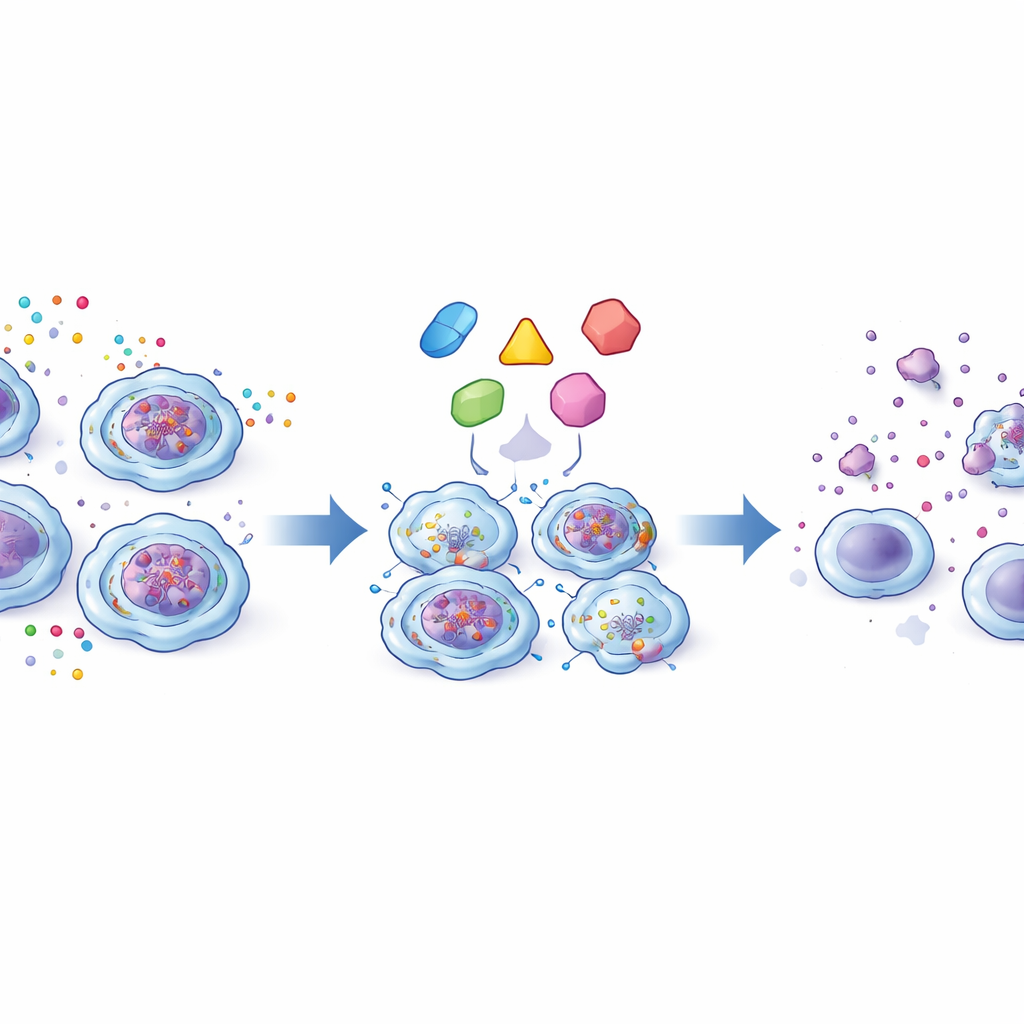
Een kromme veiligheidschakelaar in de cel
Normaal gesproken helpt een bewakerseiwit genaamd p53 bij het bepalen van het lot van cellen wanneer ze DNA-schade ophopen of sterke oncogene signalen ervaren—of ze stoppen met delen of zichzelf vernietigen. In de ETV6::RUNX1‑positieve cellen toonden genexpressiepatronen dat p53 sterk betrokken was bij het afdwingen van celcyclusarrest maar niet bij het inschakelen van veel van zijn gebruikelijke doodsbevorderende partners. De cellen bouwden p53-eiwit op en activeerden stressgerelateerde signaalroutes, maar één cruciale modificatie van p53—een fosfaatgroep op een specifieke plaats die nodig is voor efficiënte apoptose—ontbrak. Dit defect was gekoppeld aan verminderde niveaus van een kinase-enzym dat normaal gesproken deze tag toevoegt. Daardoor waren de cellen, wanneer ze werden blootgesteld aan DNA-beschadigende behandelingen zoals chemotherapie-achtige middelen of bestraling, meer geneigd te overleven dan hun normale tegenhangers.
Senescentie inzetten als therapeutisch doelwit
Aangezien ETV6::RUNX1‑positieve cellen senescent maar hardnekkig in leven bleken te zijn, testte het team of ze selectief konden worden verwijderd met senolytische geneesmiddelen die ontworpen zijn om senescentie cellen te doden. Eén verbinding, SSK1, wordt geactiveerd door hetzelfde beta-galactosidase-enzym dat in deze cellen overactief is en bracht alleen binnen die cellen een toxische lading vrij. Een ander, piperlongumine—een natuurlijk product uit de lange peper—benutte hun reeds hoge oxidatieve stress en duwde ze over de rand richting celdood terwijl normale cellen gespaard bleven. Een derde, TM5441, remde PAI‑1, een eiwit dat senescente cellen helpt apoptose te weerstaan. Alle drie de middelen doodden in cultuur bij voorkeur fusie‑positieve cellen. In de transgene muizen verminderde behandeling van beenmergvoorlopercellen met SSK1 de vorming van pre‑B-celkolonies afkomstig van ETV6::RUNX1‑expressing cellen, maar niet van normale cellen, wat het idee versterkt dat senescentie-gekoppelde kenmerken als therapeutische houvast kunnen dienen.
Van vroeg controlepunt naar preventiestrategie
Dit werk plaatst de ETV6::RUNX1-fusie niet als een eenvoudige aanzet tot leukemie, maar als een trigger voor een vreemde tussentoestand: cellen die gestopt zijn met delen, weerstand bieden aan celdood en stilletjes schade ophopen na verloop van tijd. Dat pre-leukemische controlepunt kan helpen verklaren waarom slechts een klein deel van de dragers uiteindelijk kanker ontwikkelt. Tegelijkertijd onthult het specifieke zwaktes—van enzymactiviteiten tot stressverdedigingen—die senolytische middelen kunnen benutten. In de toekomst zouden nauwkeurig gerichte behandelingen mogelijk deze aanhoudende pre-leukemische cellen bij hoogrisicopersonen kunnen opruimen, waardoor terugval na therapie vermindert of leukemie zelfs voorkomen wordt voordat ze begint.
Bronvermelding: Acunzo, D., Bertagna, M., Risca, G. et al. Targeting oncogene-induced senescence in ETV6::RUNX1 pre-leukemic cells. Cell Death Discov. 12, 145 (2026). https://doi.org/10.1038/s41420-026-03001-5
Trefwoorden: kinderleukemie, pre-leukemische cellen, cellulaire senescentie, ETV6-RUNX1 fusie, senolytische therapie