Clear Sky Science · nl
iS2C2: een cointelligente platform voor mechanistische ontdekking van cellulaire communicatie bij ziekte
Waarom slimme samenwerking tussen cellen en computers ertoe doet
Wanneer we ziek worden, beginnen onze cellen abnormale signalen naar elkaar te sturen en hervormen ze weefsels geruisloos lang voordat symptomen optreden. De moderne biologie kan deze signalen nu gen‑voor‑gen vastleggen in miljoenen individuele cellen, maar de resulterende gegevens zijn te omvangrijk en te complex voor menselijke experts om alleen te interpreteren. Dit artikel introduceert iS2C2, een nieuw platform waarmee rigoureuze data‑analyse en grote taalmodellen samenwerken om te achterhalen hoe cellen communiceren bij ziekten zoals Alzheimer en kanker, en dat richting geeft aan preciezere manieren om ziekte te diagnosticeren en te behandelen.
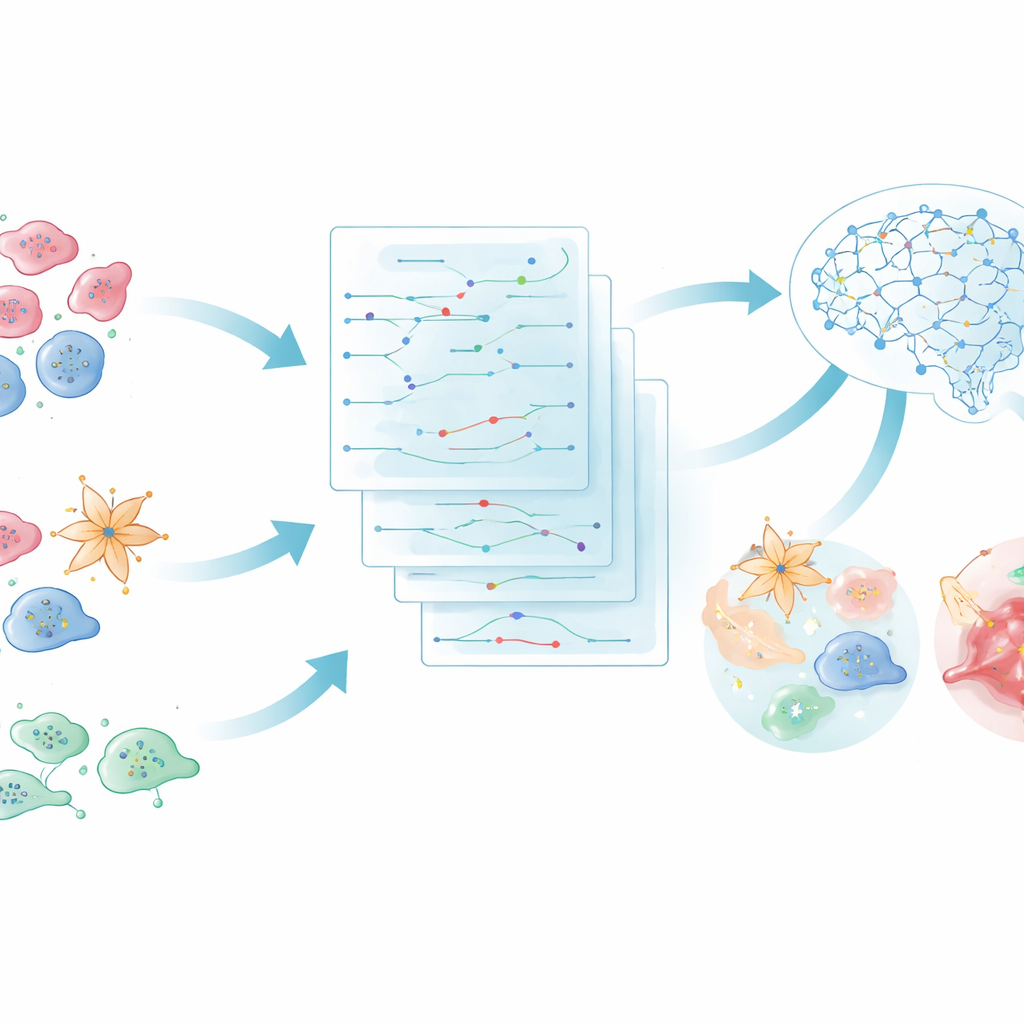
Hoe cellen stille gesprekken voeren bij ziekte
Elk weefsel in het lichaam is een drukke buurt van cellen die continu signalen uitwisselen. De ene cel geeft een molecuul af dat fungeert als een "ligand", en een andere cel ontvangt het via een bijpassende "receptor" op zijn oppervlak, wat interne veranderingen activeert. Als dit gesprek ontspoort, kan het aandoeningen aansturen, van geheugenverlies bij de ziekte van Alzheimer tot het uitzaaien van tumoren bij kanker. Nieuwe technieken die RNA in individuele cellen en in weefseldoorsneden meten, tonen nu welke genen actief zijn in elke cel en waar die cellen zich in driedimensionale ruimte bevinden. De uitdaging is die stroom cijfers om te zetten in duidelijke verhalen over wie met wie praat en hoe die boodschappen het ziekteverloop veranderen.
Een nieuwe kaart van cel‑tot‑cel boodschappen
De eerste helft van iS2C2 is een gespecialiseerd analyse‑mechanisme genaamd S2C2. Het verwerkt single‑cell en ruimtelijke genexpressiegegevens uit menselijk of muisweefsel en zoekt naar celparen waarbij de ene cel sterk een signaalmolecuul tot expressie brengt en de andere zijn bijbehorende receptor tot expressie brengt. In plaats van daar te stoppen, volgt S2C2 het signaal naar binnen en traceert het door ketens van bekende routecomponenten tot aan sleutelregulatoren in de kern. Elke zodanige route, een zogenaamde pathway‑tak, krijgt een activiteitscore die zowel weerspiegelt hoe sterk het signaal wordt verzonden als hoe sterk de downstreamgenen reageren. Dit scoresysteem helpt de specifieke takken te benadrukken die in een bepaalde ziekte het meest veranderd zijn, zelfs wanneer de oorspronkelijke gegevens ruis bevatten of onvolledig zijn.
De taalmodellen biologische redeneerprocessen laten uitvoeren
Het tweede deel van iS2C2 gebruikt een groot taalmodel als redeneerpartner. S2C2 genereert gestructureerde bestanden met belangrijke signaalparen, pathway‑takken en hun context. Zorgvuldig opgestelde prompts sturen vervolgens het taalmodel om deze bestanden stap voor stap te lezen, de meest invloedrijke signalen te selecteren, ze te verbinden met bestaande biologische kennis en toetsbare hypothesen te genereren over hoe ze de ziekte zouden kunnen beïnvloeden. De auteurs toonden aan dat het gebruik van voorbeelden en stapsgewijze redeneerprompts de neiging van het model om ononderbouwde verbanden te verzinnen vermindert en verbetert hoe goed de suggesties overeenkomen met de onderliggende gegevens. Deskundige beoordelaars vonden de resulterende verklaringen beter begrijpelijk en nuttiger voor het plannen van experimenten dan die van eerdere methoden.
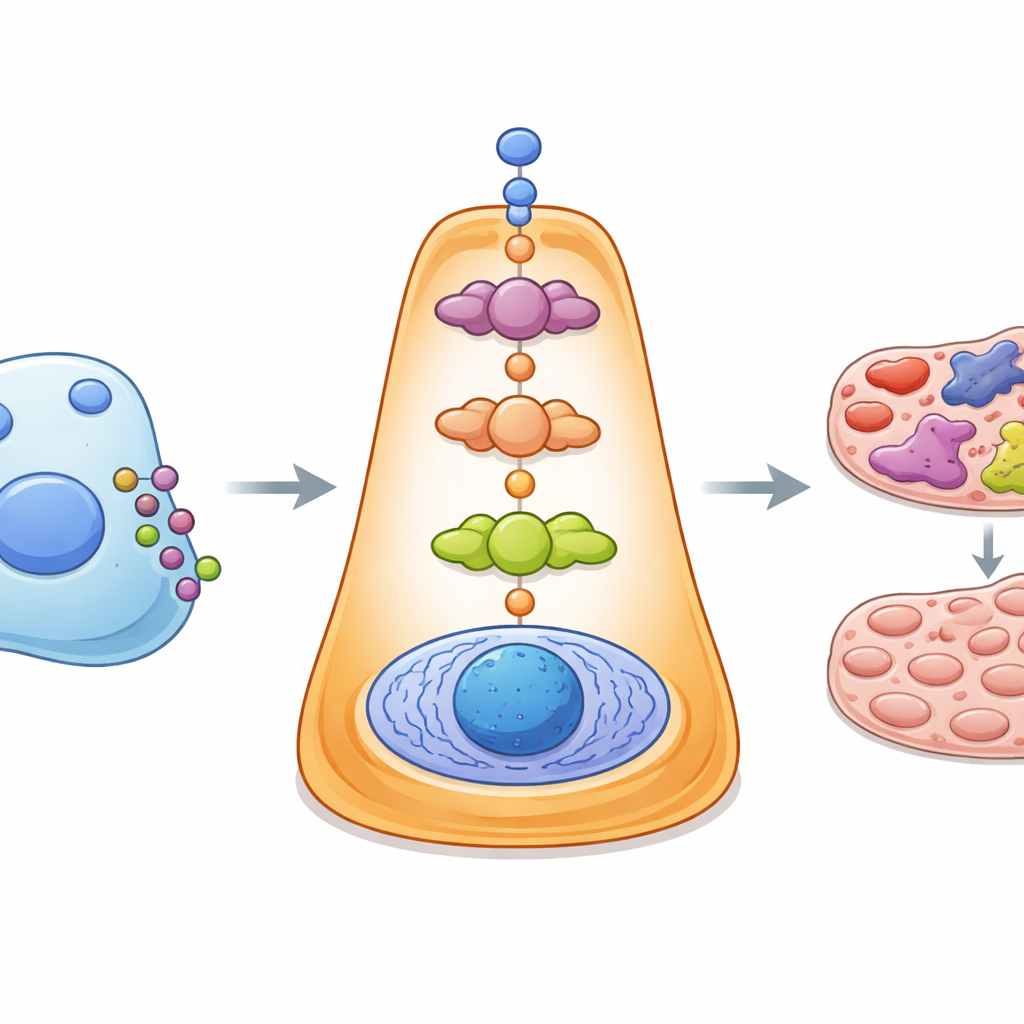
Wat het platform onthulde bij Alzheimer en kanker
Om iS2C2 in echte ziektecontexten te testen, paste het team het toe op meerdere grote hersendatasets van mensen met de ziekte van Alzheimer. Het platform benadrukte een onverwacht gesprek tussen ondersteunende cellen, astrocyten genoemd, en nabijgelegen neuronen, gecentreerd rond een signaalpaar bekend als CSF1 en zijn receptor. Celkweekexperimenten bevestigden dat het verstoren van deze koppeling beschermende routes in neuronen verzwakte en hun inflammatoire gedrag veranderde, wat de suggestie ondersteunt dat deze kruiscommunicatie bijdraagt aan het overleven van zenuwcellen. In een tweede casestudy van borstkankercellen die naar bot uitzaaien, combineerde iS2C2 single‑cell en ruimtelijke gegevens om te laten zien hoe tumorcellen en bot‑resident stamcellen elkaar beïnvloeden via verstrengelde signaalroutes. Deze analyse wees op een gemeenschappelijk controlepunt dat wordt beïnvloed door het geneesmiddel tamoxifen, dat bij muizen de vroege botuitzaaiing vertraagde.
Wat dit betekent voor de toekomstige geneeskunde
In eenvoudige bewoordingen is iS2C2 een slimme tussenpersoon die rommelige cellulaire data vertaalt naar gestructureerde patronen en vervolgens een AI‑systeem vraagt uit te leggen wat die patronen voor de ziekte zouden kunnen betekenen. Door te verbeteren hoe we verborgen communicatielijnen tussen cellen opsporen en interpreteren, helpt het platform onderzoekers helderdere, beter toetsbare ideeën te genereren over wat ziekten als Alzheimer en uitgezaaide kanker aandrijft. Hoewel de suggesties nog steeds zorgvuldige menselijke controle en laboratoriumvalidatie vereisen, wijst deze cointelligente aanpak op een toekomst waarin computers wetenschappers sneller door complexe biologie leiden en met meer vertrouwen helpen bij het zoeken naar nieuwe diagnostica en behandelingen.
Bronvermelding: Sheng, J., Ahn, J.Y., Yang, L. et al. iS2C2: a cointelligent platform for mechanistic discovery of disease cellular crosstalk. Sig Transduct Target Ther 11, 172 (2026). https://doi.org/10.1038/s41392-026-02691-8
Trefwoorden: celcommunicatie, single‑cell data, grote taalmodellen, Ziekte van Alzheimer, kankeruitzaaiing