Clear Sky Science · nl
Ontwikkeling van therapeutische strategieën bij mantelcellymfoom: vooruitgang en toekomstige richtingen
Waarom dit kankerverhaal ertoe doet
Mantelcellymfoom is een zeldzame vorm van bloedkanker die vroeger een somber vooruitzicht had, waarbij veel patiënten slechts enkele jaren na de diagnose overleefden. In het laatste decennium heeft echter een reeks nieuwe precisiegeneesmiddelen en immuun-gebaseerde behandelingen dat beeld doen veranderen. Dit overzichtsartikel legt uit hoe artsen afstappen van een universele chemotherapie naar slimmer, meer op maat gemaakte strategieën die de ziekte langer onder controle kunnen houden met minder bijwerkingen. Ook voor lezers zonder medische achtergrond biedt het een inkijk in hoe moderne kankerzorg gerichter, persoonlijker en hoopvoller wordt.
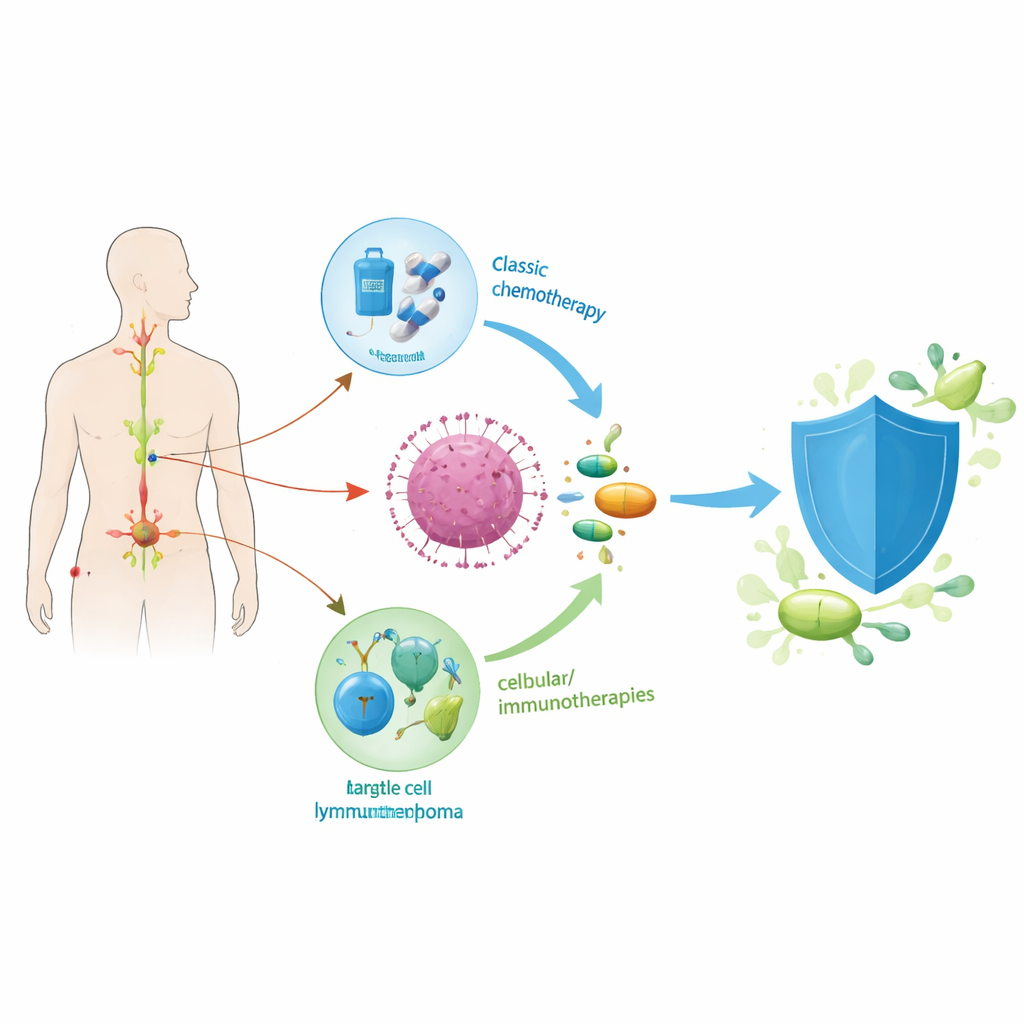
Een complexe bloedkanker begrijpen
Mantelcellymfoom ontstaat uit witte bloedcellen die B-cellen worden genoemd en normaal gesproken helpen bij het bestrijden van infecties. Bij deze ziekte zorgt een belangrijke genetische afwijking ervoor dat deze cellen ongecontroleerd gaan groeien en zich verspreiden naar lymfeklieren, beenmerg en soms organen zoals de milt en darmen. Artsen hebben geleerd dat mantelcellymfoom geen eenduidige ziekte is: bij sommige mensen verloopt het langzaam, terwijl het bij anderen snel en agressief is. Om patiënten in brede risicogroepen in te delen, combineren clinici nu eenvoudige klinische maten (zoals leeftijd en bloedonderzoeken), microscopische kenmerken van de kanker, genetische veranderingen en zeer gevoelige tests die kleine sporen van ziekte na behandeling opsporen. Deze instrumenten helpen voorspellen wie waarschijnlijk vroeg zal terugvallen en wie langer in remissie kan blijven.
Van intensieve chemotherapie naar gerichte pillen
Jarenlang bestond de standaardbehandeling uit intensieve chemotherapie gecombineerd met een antistofmedicijn genaamd rituximab, vaak gevolgd door een stamceltransplantatie bij jongere, fitte patiënten. Hoewel deze aanpak diepe remissies kon opleveren, ging het gepaard met lange ziekenhuisopnames en ernstige bijwerkingen, en leken de voordelen kleiner te worden zodra nieuwere middelen beschikbaar kwamen. Grote onderzoeken hebben nu aangetoond dat het toevoegen van een pil die een Bruton-tyrosinekinase (BTK)-remmer bevat aan standaardregimes verlengt hoe lang patiënten ziektevrij blijven, en dat in sommige gevallen die pil meer uitmaakt dan de transplantatie zelf. Bij oudere patiënten die zeer zware behandelingen niet verdragen, heeft het combineren van BTK-remmers met mildere chemotherapie remissies verlengd met een aanvaardbaarder veiligheidsprofiel, wat een verschuiving weg van alleen chemotherapie markeert.
Opbouw van chemo-vrije en lage-chemo benaderingen
Een belangrijk thema van het artikel is de opkomst van "chemo-vrije" combinaties. Deze regimens koppelen immuunversterkende antilichamen aan pillen die kankercellen aan het immuunsysteem blootstellen of hun overlevingssignalen blokkeren. Vroege studies van dergelijke combinaties — waaronder twee- en driecomponenten-cocktails rond BTK-remmers, venetoclax (dat een overlevings-eiwit target) en immuunmodulerende tabletten — hebben zeer hoge responspercentages en vaak diepe opruiming van residuele ziekte laten zien, zelfs bij patiënten met zorgwekkende genetische kenmerken zoals TP53-mutaties. Sommige programma’s onderzoeken korte kuren van gerichte therapie gevolgd door een enkele infusie van geconstrueerde immuuncellen, met als doel lange remissies te bereiken zonder jarenlange doorlopende behandeling. Hoewel de follow-up nog relatief kort is, wijzen deze strategieën op een toekomst waarin veel patiënten traditionele chemotherapie helemaal kunnen vermijden.
Nieuwe hoop na terugval
Ondanks vooruitgang zien veel mensen met mantelcellymfoom hun kanker nog steeds terugkeren, vooral na blootstelling aan BTK-remmers van de eerste generatie. Het overzicht beschrijft hoe de opties voor deze lastige groep zijn uitgebreid. Een nieuwere, flexibeler BTK-remmer genaamd pirtobrutinib kan werken wanneer eerdere BTK-middelen falen en lijkt minder vaak hart- en bloedingsproblemen te veroorzaken. De meest dramatische vorderingen komen echter van chimerische antigeenreceptor (CAR) T-celtherapieën, waarbij de eigen T-cellen van een patiënt worden aangepast om lymfomacellen te herkennen en aan te vallen. Bij zwaar voorbehandelde patiënten hebben CAR-T-cellen snelle en vaak complete remissies teweeggebracht, ook bij mensen met hoog-risico ziekte, hoewel bijwerkingen zoals koorts, verwardheid en infecties zorgvuldig beheerd moeten worden. Voor patiënten die geen CAR-T kunnen krijgen, tonen opkomende "kant-en-klare" antilichaammiddelen die de T-cellen van het lichaam direct naar kankercellen trekken, evenals antilichaam–medicijnconjugaten die chemotherapie precies naar tumorcellen brengen, veelbelovende resultaten in vroege onderzoeken.
Vooruitkijken naar meer gepersonaliseerde zorg
De auteurs concluderen dat mantelcellymfoom verschuift van een uniform moeilijk behandelbare kanker naar een aandoening waarbij veel patiënten langere en beter kwalitatieve levens kunnen verwachten. De belangrijkste aanjagers zijn slim samengestelde medicijncombinaties, eerder gebruik van immuun-gebaseerde therapieën en verfijndere risicoinstrumenten die aangeven wie welke behandeling nodig heeft en wanneer. Tegelijk benadrukken zij dat toegang en langdurige follow-up grote uitdagingen blijven: de meeste van de nieuwste behandelingen zijn duur en nog niet wijdverbreid beschikbaar, en artsen moeten nog leren hoe ze deze middelen het beste over de levensloop van een patiënt kunnen sequencen. Voor niet-specialistische lezers is de kernboodschap dat hoewel mantelcellymfoom ernstig blijft, de behandelopties snel uitbreiden en het voormalige korte, starre traject veranderen in een flexibelere, gepersonaliseerde routekaart gericht op duurzame controle en kwaliteit van leven.
Bronvermelding: Tavarozzi, R., Maher, N., Catania, G. et al. Evolving therapeutic strategies in mantle cell lymphoma: advancements and future directions. Leukemia 40, 857–871 (2026). https://doi.org/10.1038/s41375-026-02942-1
Trefwoorden: mantelcellymfoom, gerichte therapie, CAR-T-cellen, BTK-remmers, bispecifieke antilichamen