Clear Sky Science · nl
Subcellulaire synoviale reacties bij het ontstaan van TMJ‑artrose definiëren via modellen van mechanische stress en articulair schijfverplaatsing
Waarom slijtage van het kaakgewricht ertoe doet
Het kaakgewricht, of temporomandibulair gewricht (TMJ), maakt kauwen, spreken en gapen mogelijk. Wanneer het begint af te breken — een aandoening die TMJ‑artrose wordt genoemd — kunnen mensen chronische pijn, moeite met eten en een verminderde levenskwaliteit ervaren. Vergeleken met knieën of heupen is dit kleine maar complexe gewricht echter veel minder bestudeerd. Dit artikel gebruikt geavanceerde genetische kaartleggingstools in muismodellen om, op een ongekende manier, te onthullen wat er gebeurt in de zachte bekleding van het gewricht zodra TMJ‑artrose begint.
Twee manieren om een kaakgewricht te overbelasten
Om veelvoorkomende problemen bij patiënten na te bootsen, creëerden de onderzoekers twee typen TMJ‑schade bij muizen. In het ene model veranderden ze hoe de tanden op elkaar sluiten zodat de kaak scheef sloot en het gewricht herhaaldelijk werd overbelast — dit staat voor mechanische stress door een slechte beetuitlijning. In het andere model trokken ze chirurgisch de dempende schijf in het gewricht naar voren en zetten die op de verkeerde plaats vast, wat een verplaatste schijf nabootst die vaak met TMJ‑pijn wordt geassocieerd. Beide modellen werden gedurende drie weken vergeleken met gezonde controledieren, terwijl botstructuur en weefselveranderingen werden gemeten met 3D‑röntgenscans en microscopie. 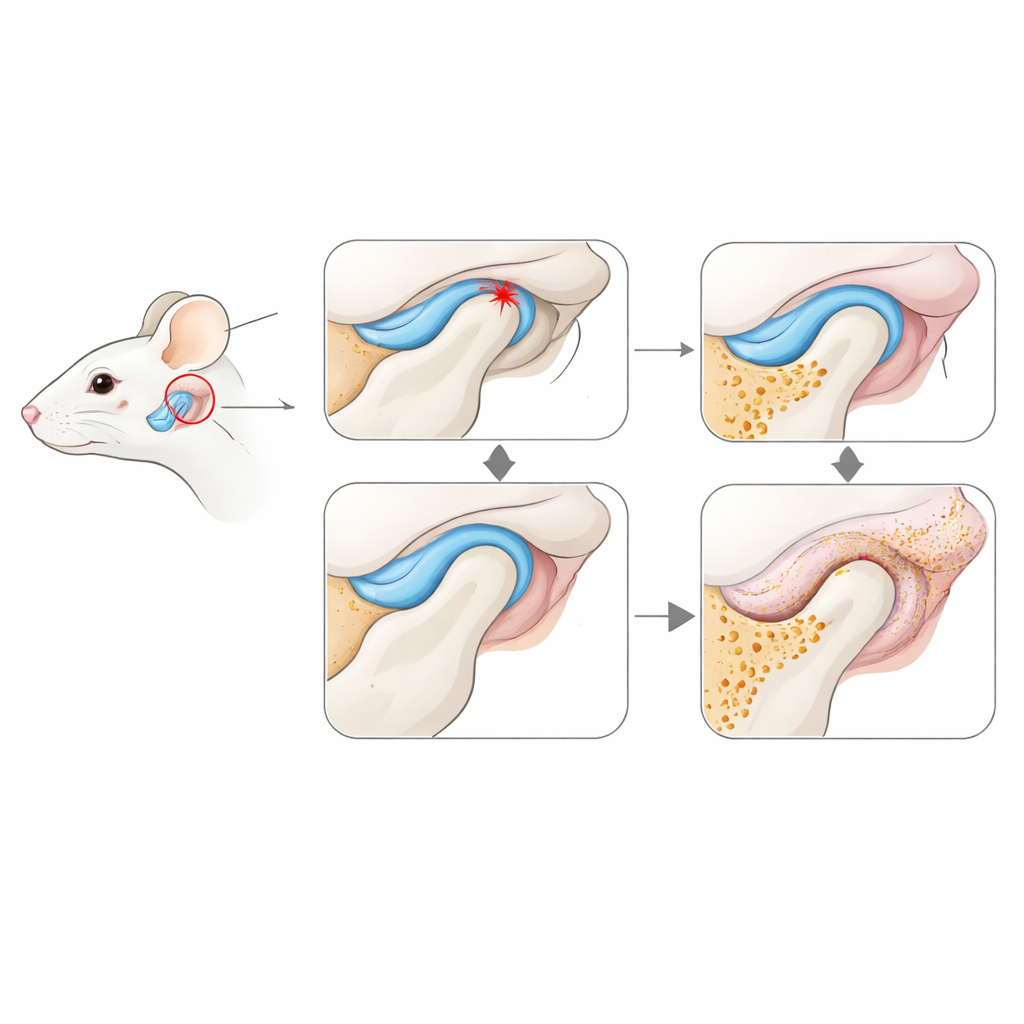
Vroege schade in bot, kraakbeen en gewrichtsbekleding
Zowel overbelaste als schijf‑verplaatste gewrichten vertoonden snel kenmerkende tekenen van vroege artrose. De botkop van de kaak verloor mineraaldichtheid en ontwikkelde putjes, extra botgroei en meer actieve botafbrekende cellen, wat aangeeft dat het inwendige raamwerk van het gewricht te snel werd omgebouwd. Het kraakbeen dat normaal een glad glijdend oppervlak biedt, begon dunner te worden, te scheuren en beschermende moleculen te verliezen, vooral in het schijf‑verplaatsingsmodel. Tegelijkertijd werd het synovium — het dunne, zachte weefsel dat het gewricht voedt — dikker, gevuld met meer cellen en op sommige plaatsen vetter of fibreuzer. Deze structurele veranderingen suggereren dat de gewrichtsbekleding niet slechts een passieve toeschouwer is, maar een belangrijke rol speelt bij het starten van gewrichtsdegeneratie.
De moleculaire signalen van het gewricht per cel lezen
Om verder te gaan dan anatomie en te zien wat individuele cellen deden, onderzocht het team welke genen actief waren in duizenden cellen met behulp van bulk RNA‑sequencing, single‑cell RNA‑sequencing en hoogresolutie ruimtelijke transcriptomics. Met deze methoden konden ze nauwkeurig vaststellen wanneer en waar verschillende celtypen hun gedrag veranderden. In het botuiteinde van het gewricht werden genen die normaal behulpzaam zijn voor het behoud van gezond kraakbeen naar beneden bijgesteld, terwijl genen die verbonden zijn met weefselafbraak en botafbrekende activiteit juist omhoog gingen, vooral in het schijf‑verplaatsingsmodel. In het synovium verhoogden cellen de productie van ontstekingsboodschappers, weefselafbrekende enzymen en moleculen die met littekenvorming en fibrose worden geassocieerd. Een bijzonder belangrijk brandpunt was het achterste deel van de schijfbekleding, waar ontsteking, vetophoping en fibrotische verdikking vroegtijdig samenkwamen.
Cellulaire kruisgesprekken en een nieuwe kaart van het kaakgewricht
Door genactiviteit per cel te analyseren en die cellen terug te plaatsen in hun exacte posities in het weefsel, identificeerden de auteurs distincte buurten van fibroblasten (ondersteunende cellen), immuuncellen en bloedvatvormende cellen binnen het synovium. Deze celtypen leken met elkaar te communiceren via signaalroutes die reageren op mechanische rek en ontsteking. Bijvoorbeeld waren signalen in de Notch‑route — bekend voor het regelen van bloedvaten en weefselremodellering — bijzonder actief in endotheliale (vatbekleding) cellen in beschadigde gewrichten, waarschijnlijk beïnvloed door nabijgelegen fibroblasten. Dezelfde regio’s toonden ook hoge niveaus van enzymen die kraakbeen afbreken en markers van fibrose, wat het idee versterkt dat gestreste synoviale cellen kraakbeenverlies en pijn kunnen aansturen. 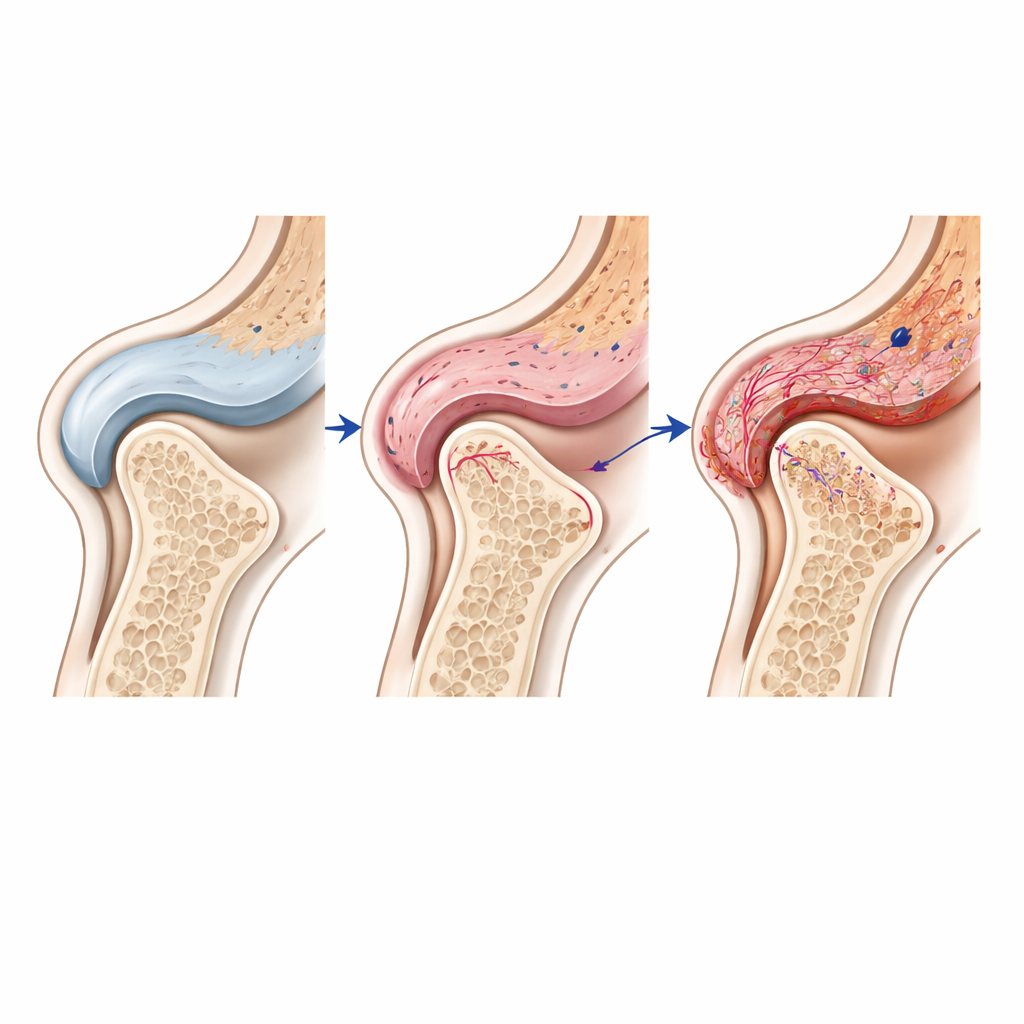
Hoe dit werk toekomstige behandelingen kan vormen
In plaats van een specifiek geneesmiddel te testen, levert deze studie een gedetailleerde atlas van hoe de zachte bekleding en het kraakbeen van de TMJ reageren op schadelijke krachten in het allereerste begin van de ziekte. Het toont aan dat vroege TMJ‑artrose wordt gekenmerkt door gecoördineerde veranderingen in bot, kraakbeen en vooral synoviale cellen, die ontstekingsachtig en fibrotisch worden terwijl ze schadelijke signalen het gewricht insturen. Door deze veranderingen te koppelen aan precieze celtypen en locaties, belicht het werk nieuwe potentiële behandeldoelen — zoals routes betrokken bij Notch‑signaaltransductie, chemokinesignalering en matrixafbrekende enzymen — die mogelijk geblokkeerd kunnen worden voordat gewrichtsschade onomkeerbaar wordt. Kort gezegd biedt het artikel een krachtig stappenplan om te begrijpen en uiteindelijk de keten van gebeurtenissen te onderbreken die alledaagse kaakbeweging verandert in chronische TMJ‑pijn.
Bronvermelding: Shibusaka, K., Negishi, S., Terashima, A. et al. Defining subcellular synovial responses in TMJ osteoarthritis onset via mechanical stress and articular disk derangement models. Int J Oral Sci 18, 28 (2026). https://doi.org/10.1038/s41368-025-00411-6
Trefwoorden: temporomandibulaire gewricht, artrose, synovium, mechanische stress, single-cell transcriptomics