Clear Sky Science · ja
臨床由来のコア生検を用いた消化管腫瘍の個別化シグナル伝達経路解析:患者層別化と薬剤標的評価
この研究が患者にとって重要な理由
がん医はますます、各患者の腫瘍の個別の生物学に治療を合わせようとしています。膵臓、結腸、肝臓、胆管など消化器系のがんでは、発症頻度が高く、しばしば診断が遅れ、治療が困難であるため、こうした取り組みが特に重要です。本研究は、微量の生検試料から多数のがん関連タンパク質の活性を読み取る新たな実験的方法を検討し、個々の患者により精密な治療選択を支援することを目指しています。
DNA列挙から生きたシグナルへ
現在、多くの「個別化」がん医療は腫瘍のDNA変化の解析に依拠しています。DNA解析は強力ですが、細胞内で実際にどのシグナルがオンになって増殖を駆動しているかは示しません。そうしたシグナルはタンパク質によって伝えられ、多くは薬剤で直接標的にできるものです。研究者らはDigiWestと呼ばれる高スループット技術(古典的なウェスタンブロットの現代版)を用いて、およそ130〜200種類のタンパク質とその活性化形態を同時に測定しました。重要なのは、この方法が単一の針生検程度の試料量しか必要としないため、実臨床での利用に適している点です。
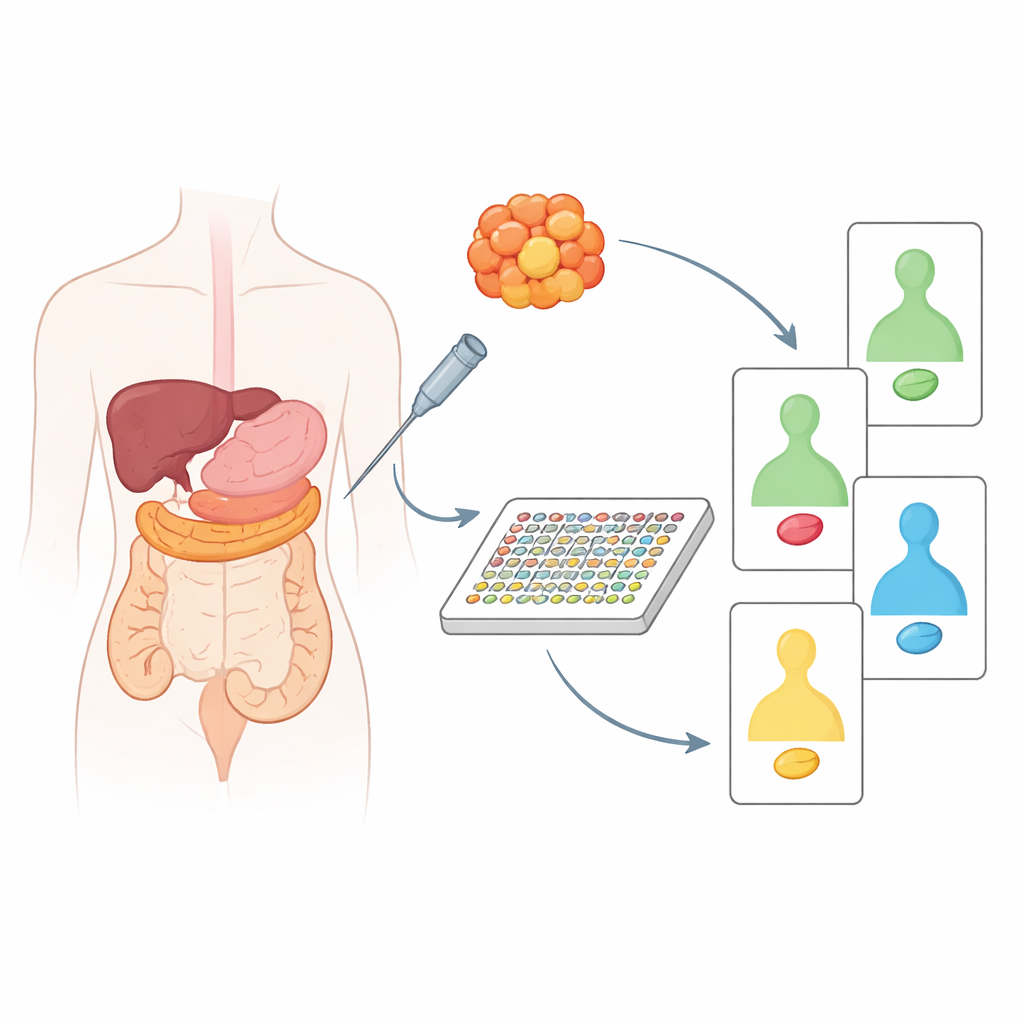
腫瘍組織とその近傍の健康組織の比較
研究チームはまず、膵臓がんまたは結腸がんの20人分の保存組織を解析し、常に同一人物の近傍の非がん組織と対で比較しました。腫瘍を自身の健康な対照と比較することで、器官間の正常な違いを反映したものではなく、がんによって真に変化したタンパク質が明らかになります。これにより、p53、Ras、PTENなどのよく知られたがんの保護因子やドライバーたちの振る舞いに明確な対照が見られました。たとえば膵臓腫瘍は増殖促進シグナルの強化や保護タンパク質の喪失を示す傾向があり、結腸腫瘍は別個の乱れた経路パターンを示しました。サンプルをこれらのタンパク質変化に基づいてクラスタリングすると、膵臓がんを生物学的に異なる2群に分けられ、結腸がんについても患者年齢や腫瘍の腸内位置に関連する意味のある差異を検出できました。
個々の腫瘍のシグナル活動の「バーコード」
群平均を超えて、研究者らは各腫瘍の詳細なタンパク質プロファイルを構築しました。これらのプロファイルは、mTOR、MAPK/Erk、Wnt、免疫関連因子といったシグナル経路のどれが特に活性化しているか、あるいは抑制されているかを明らかにしました。測定されたタンパク質の多くは既存薬の直接標的であるか、その下流に位置しているため、どの薬剤が腫瘍の主要な増殖機構を阻害しうるかを推測できます。回顧的症例の4分の3では、腫瘍進展に寄与していると思われる一つ以上の経路を挙げることができました。また、免疫細胞マーカーに富む「ホット」ながんを示す腫瘍や、特異な署名を持つ異常ケースも同定しました。
実患者での応用
臨床での有用性を検証するため、研究者らは分子腫瘍カンファレンスで審議中だった14人の消化管がん患者からの新鮮な針生検にDigiWestを適用しました。これらの患者は病歴が複雑で、しばしば既往治療を受けていました。対照となる健康組織が利用できなかったため、各腫瘍のタンパク質レベルは群の中央値と比較して異常高値または低値を定義しました。このより制約のある設定でも、14例中12例の腫瘍で治療に関連する明確な経路活動パターンが示されました。詳細な2例では、タンパク質データが結腸がんにおけるFGFR2遺伝子のDNAレベルでの増幅や、肝がんでのmTOR抑制機構の喪失を確認し、FGFR阻害薬やmTOR阻害薬の検討を強く支持しました。全体として、DigiWestの所見は主要な遺伝的ドライバーと一致し、大部分の評価可能な症例で薬剤標的を示唆しました。
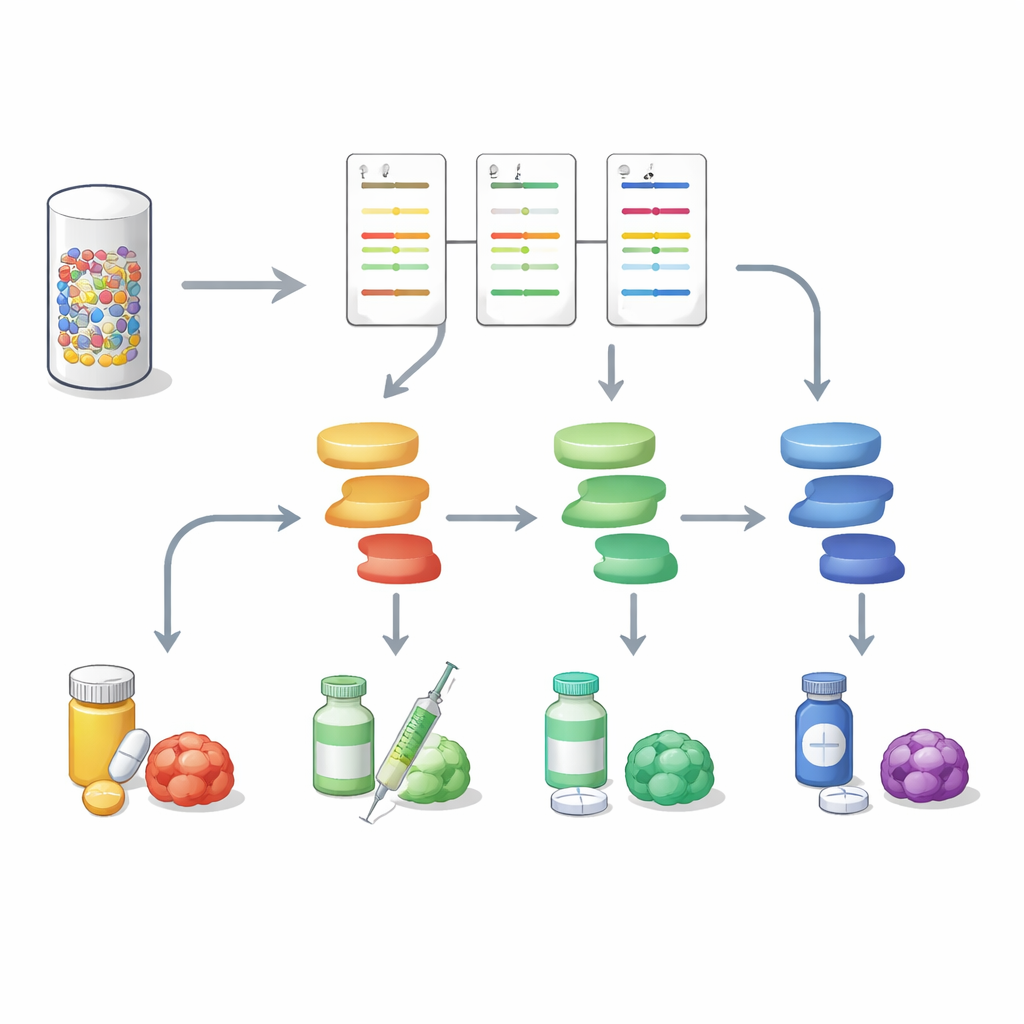
より完全な腫瘍像に向けて
本研究は、DNAシーケンシングと並行してタンパク質シグナルを解析することで、消化管腫瘍のより豊かで実行可能な像が得られることを示しています。微小な生検試料から多経路の活動マップを作成することで、DigiWestは特定のがんでどの分子スイッチが実際にオンになっているか、どの薬剤がそれらを最も効果的に攻撃しうるかを識別し、さらに新たな耐性経路の出現を示唆することもできます。より大規模な研究は依然必要ですが、このアプローチは高内容のタンパク質プロファイリングを日常の精密医療に導入する実用的な方法を提供し、遺伝的設計図だけでなく患者ごとの“生きている”腫瘍に合わせた治療計画に近づく道を開きます。
引用: Stahl, A., Büringer, K., Missios, P. et al. Personalized signaling pathway analysis of gastrointestinal tumors for patient stratification and drug target evaluation using clinically derived core biopsies. npj Precis. Onc. 10, 124 (2026). https://doi.org/10.1038/s41698-026-01304-5
キーワード: 精密医療(プレシジョン・オンコロジー), 消化管がん, プロテオミクス, 生検プロファイリング, 標的療法