Clear Sky Science · ja
小児同種造血幹細胞移植後のアロ免疫性肺障害の危険因子
なぜ一部の子どもはがん治療後に呼吸が困難になるのか
骨髄移植を受けた子どもたちにとって、元の疾患を生き延びることは始まりに過ぎません。治療後数か月で、早期発見が難しく、一度発症すると治療が困難な深刻な肺障害を発症する例があります。本研究は、どの子どもがこうした肺障害のリスクが高いかを明らかにし、早期発見と長期的な障害を防ぐためのケアを最適化することを目指しています。
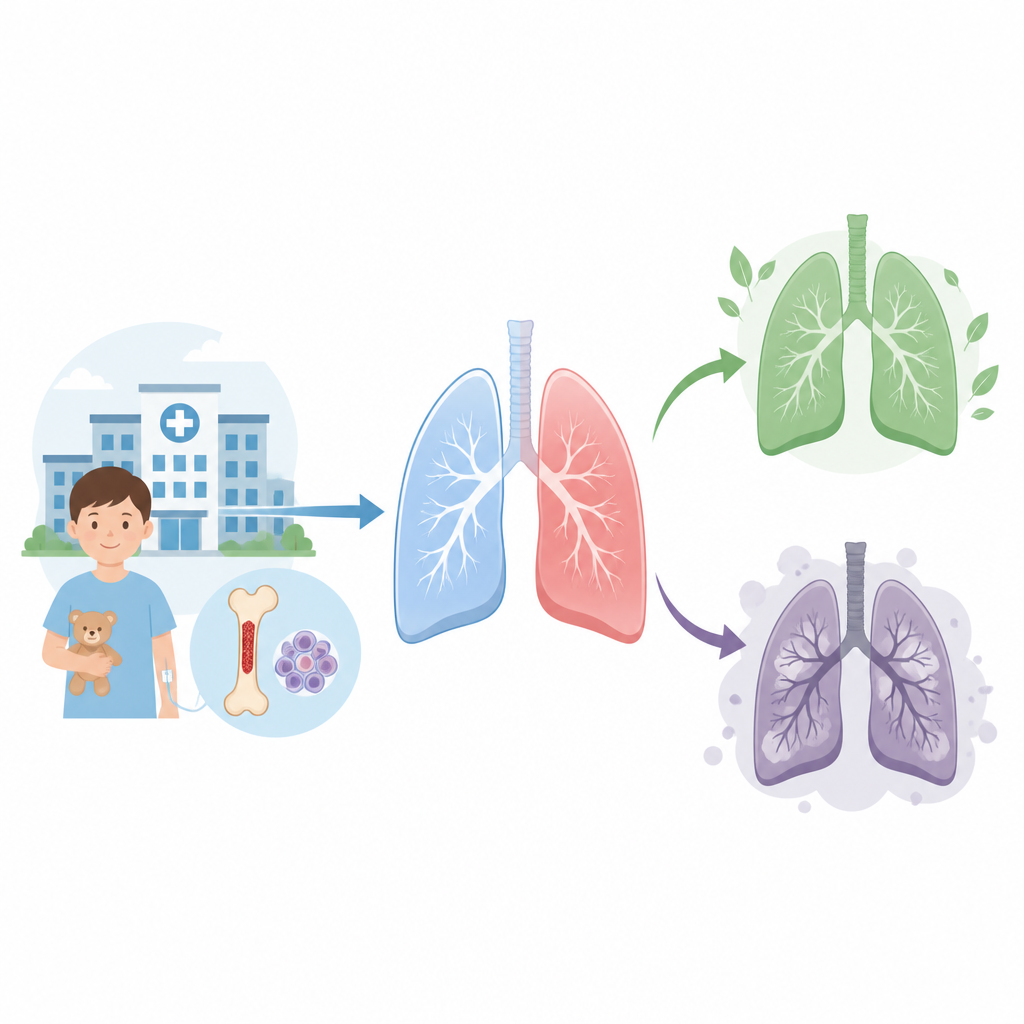
移植に関連する2種類の肺障害
研究者らは、ドナー由来の幹細胞移植後に現れる非感染性の肺症候群のうち二つに着目しました。ひとつ目は特発性肺炎症候群で、通常は移植後数か月以内に発症し、肺全体にわたる広範な炎症を伴います。もうひとつは閉塞性細気管支炎症候群で、通常はより後の時期に発症し、小さな気道を主に線維化させて徐々に気流を阻害します。どちらも新しい免疫系が肺に対して反応することに起因し、罹患した子どものかなりの割合で致命的になり得るため、予防と早期認識が不可欠です。
多くの若年患者を長期間追跡
チームは、オランダの2施設で過去20年間に初めてドナー幹細胞移植を受けた633名の小児・若年成人の記録を解析しました。半数以上はがん治療を目的とし、残りは免疫不全や遺伝性代謝疾患などの非悪性疾患が対象でした。研究では、基本的な臨床情報、移植前の治療詳細、ウイルス感染の履歴、および移植後数か月にわたる繰り返し採血の結果を統合しました。さらに、死亡や移植不成立の影響を考慮する統計手法を用いて、どの特徴が後の肺障害を予測するかを検討しました。
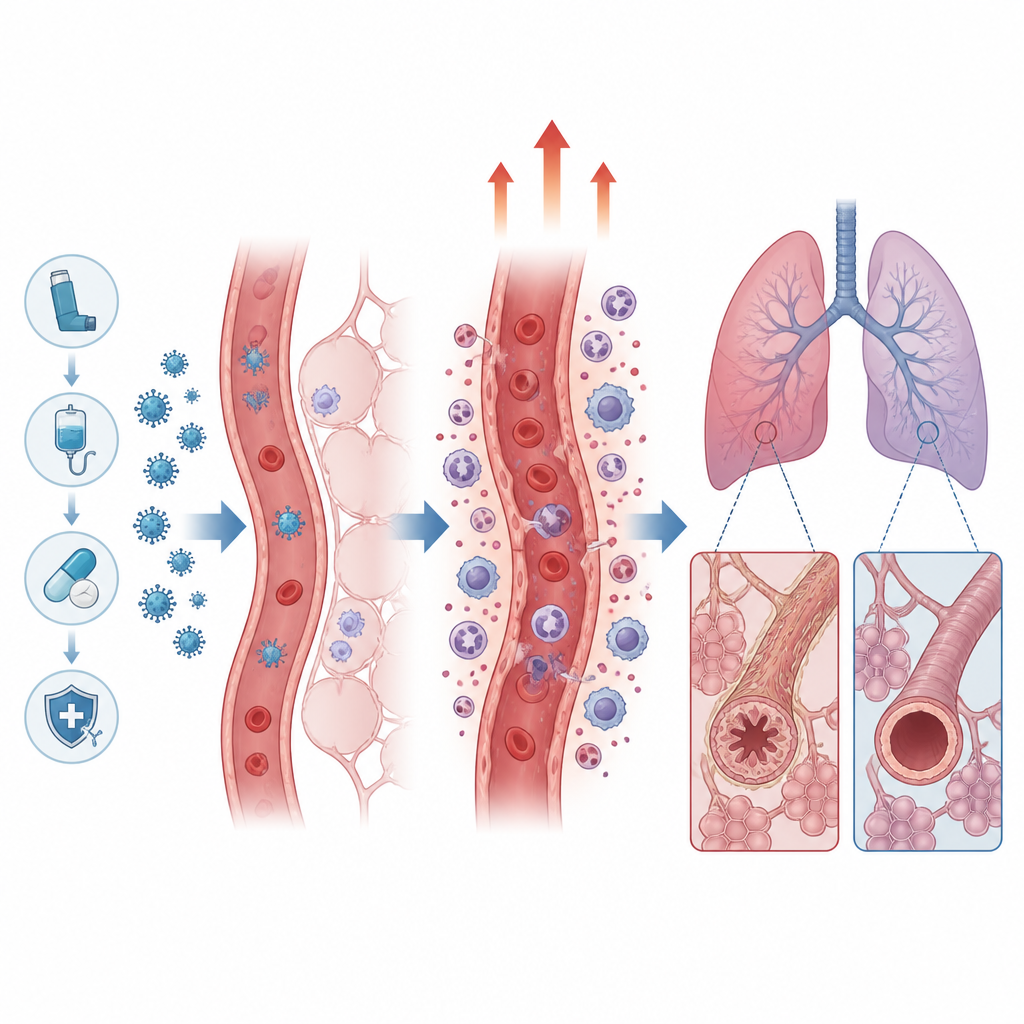
どの子どもが最もリスクが高かったか
およそ8人に1人がアロ免疫性肺症候群を発症し、早期の肺炎様型と後期の気道線維化型に分かれました。非悪性疾患を理由に移植を受けた子どもや、血中でアデノウイルスが再活性化した患者は、早期の肺炎様型を発症しやすい傾向がありました。移植前の特定の薬剤組み合わせも影響しました。ブスルファンとシクロホスファミドを含むレジメン(メルファランの有無を問わず)は、ブスルファン+フルダラビン、全身照射、または非集中的条件付けを用いるよりも、早期および後期の肺障害リスクがはるかに高いことと関連していました。
日常の血液検査に隠れた警告サイン
これらの基礎要因に加え、研究は移植後最初の3か月間の単純な血液マーカーが重要な手がかりを与えることを示しました。血管内皮細胞のストレスや損傷を反映する指標の高値は、後の肺障害と結びつき、血管内皮の損傷が疾病の引き金となることを支持しました。早期の肺炎様型を発症した子どもは、白血球数やリンパ球数が著しく高値であることが多く見られました。後に気道の線維化をきたした患者では、特定のヘルパーT細胞、特に活性化型や記憶型の増加が目立ち、肺を標的とする過剰な免疫反応が関与していることが示唆されました。
これらの知見がケアに意味すること
本研究は後ろ向き解析であり因果関係を証明するものではありませんが、幹細胞移植後に深刻な肺合併症に最も脆弱な患者像をより明確に描き出します。可能ならば毒性の低い条件付けレジメンを選択すること、アデノウイルスや呼吸器ウイルスなどのウイルス感染を注意深く管理すること、血管ストレスの簡便な指標や免疫細胞数に注目することが、追加の監視や早期介入を必要とする子どもを見つける助けになるかもしれません。臨床の現場では、この研究は命を救う移植の重大な後遺症を、予防可能あるいは少なくともより管理しやすいものに近づける一歩となります。
引用: Dekker, L., Versluys, B.A., de Koning, C.C.H. et al. Risk factors for alloimmune lung syndromes after allogeneic hematopoietic cell transplantation in children. Bone Marrow Transplant 61, 569–576 (2026). https://doi.org/10.1038/s41409-026-02829-w
キーワード: 小児の幹細胞移植, 肺合併症, 特発性肺炎症候群, 閉塞性細気管支炎, アデノウイルス再活性化