Clear Sky Science · ja
マウスにおけるMDMAによる立体選択的・性差依存的な5-HT2A受容体を介した皮質可塑性の調節
この研究が重要な理由
MDMA(一般にエクスタシーとして知られる)は、ナイトクラブの薬から臨床応用へと移行しつつあり、心的外傷後ストレス障害のような治療抵抗性の疾患で心理療法と併用して試験されています。しかし、この薬が脳をどのように再編成するのか、なぜ男女で効果が異なるのか、あるいは鏡像異性体のふるまいがどう違うのかは十分に解明されていません。本研究はマウスを用いてこれらの疑問に切り込み、MDMAの脳への影響が薬の正確な立体構造と生物学的な性の双方に依存することを明らかにし、安全で精密な治療を設計するうえで重要な示唆を与えます。
二つの鏡像薬とセロトニンの役割
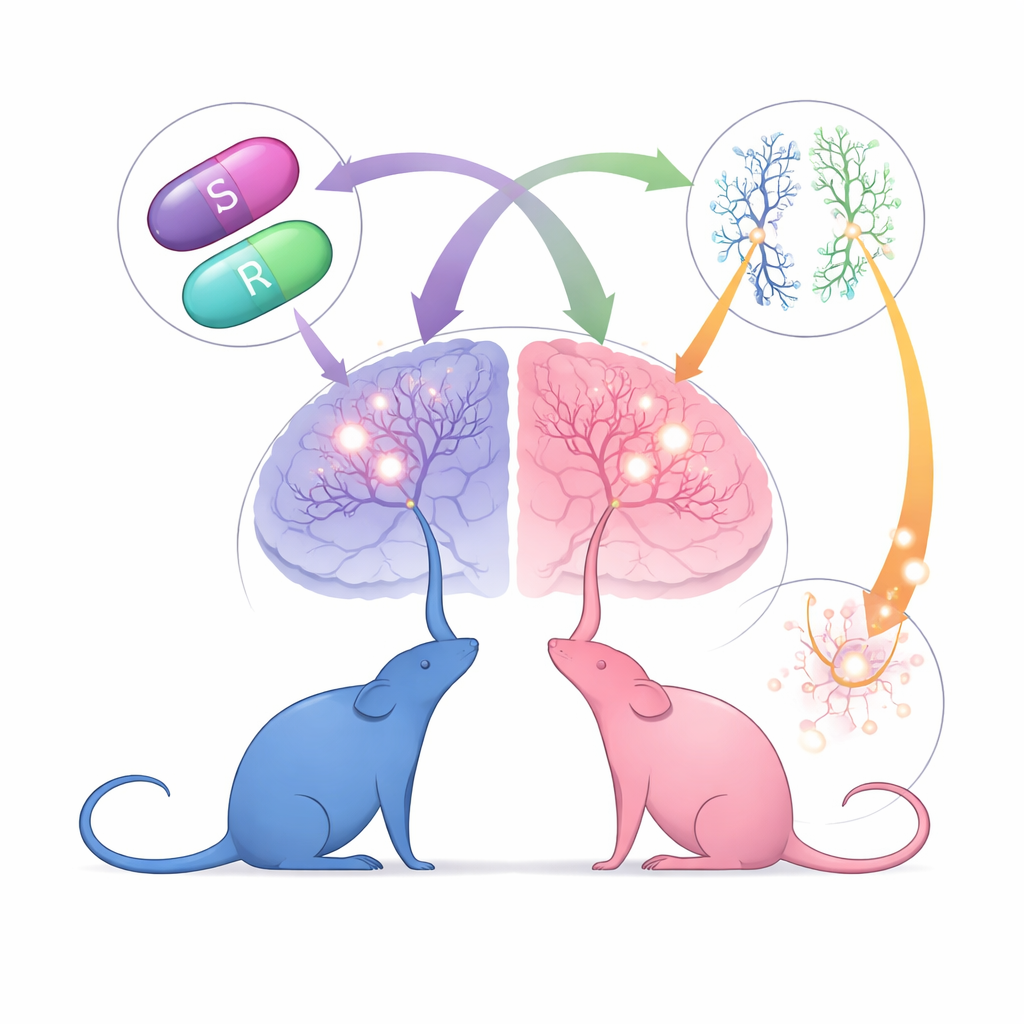
多くの薬は鏡像の二つの異性体(エナンチオマー)として存在し、体内で非常に異なる作用を示すことがあります。研究者たちは、標準的な50:50混合(ラセミ)であるMDMAと、その個別のS(+)およびR(–)形を比較しました。焦点は、古典的なサイケデリック薬や神経回路の変化に中心的に関わる脳内のセロトニン受容体5-HT2Aです。5-HT2Aを導入したヒト細胞では、ラセミとS(+)-MDMAは非常に弱い活性化作用を示し、R(–)-MDMAは受容体への結合はむしろ強いにもかかわらずほとんど活性化しませんでした。これは、生体内で観察される強力な効果が単純な受容体の直接刺激から生じているとは限らないことを示唆します。
サイケデリック様作用の行動指標
生体内でのMDMAのサイケデリック様作用を調べるために、研究チームはマウスの「ヘッドツイッチ反応」を用いました。これは5-HT2A受容体に強く依存する急速な左右振り動きで、人間のサイケデリック作用を反映します。S(+)-MDMAは雄雌の両方のマウスでこの行動を誘発しましたが、R(–)-MDMAは雌でのみ誘発しました。5-HT2A受容体を遮断するとこれらのヘッドツイッチは消失し、この受容体が必須であることが確認されました。さらに前頭皮質で受容体の主要なシグナル経路の活性化を反映する化学的指標(IP1)を測定すると、S(+)-MDMAは両性でこの信号を増強したのに対し、R(–)-MDMAはほとんど効果を示しませんでした。これらの結果は、MDMAの二つの鏡像体が5-HT2Aに結びつくシグナルの関与度で異なり、しかもその効果が性によって変換されることを示しています。
神経細胞の形を変える
持続的な治療効果は薬が神経回路をどのように再構築するかに依存する可能性があるため、研究者たちは樹状突起の小さな突起である樹状棘(シナプスの物理的部位で可塑性の指標)を調べました。前頭皮質ニューロンを蛍光標識し、単回投与後1日で棘の数を数えました。雄マウスではS(+)-MDMAが前頭皮質ニューロンの棘密度を増加させ、この変化は5-HT2A受容体欠損動物で部分的に減弱したが完全には消えませんでした。雄ではR(–)-MDMAに棘密度の検出可能な変化はなく、雌ではもともと基準値の棘密度が高かったため、どちらの異性体も棘を変化させませんでした。これらの知見は、特定の鏡像体が雄の前頭皮質で構造的再編成を促進し、5-HT2A受容体は寄与するが唯一の要因ではないことを示唆します。
隠れたスイッチとしてのセロトニントランスポーター
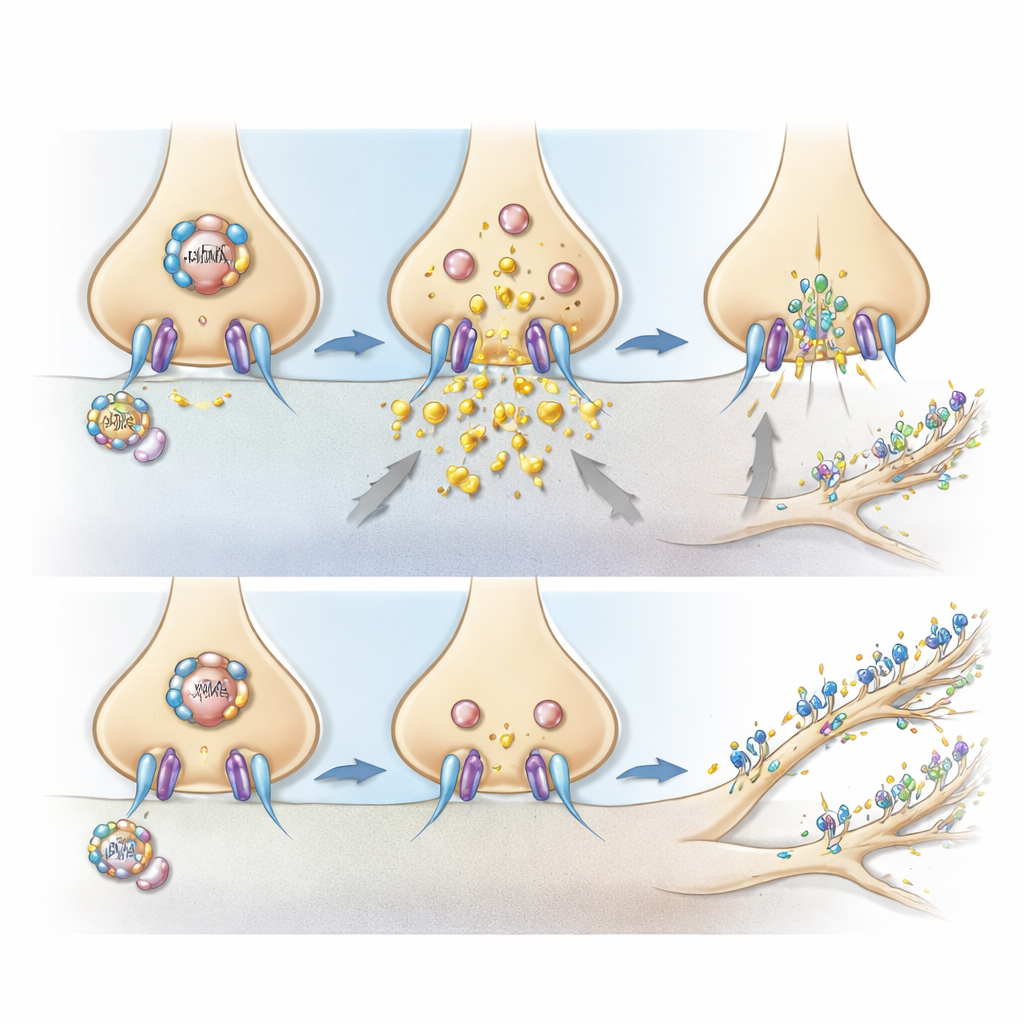
次に研究チームは、MDMAが脳内でどのようにして5-HT2A受容体を作動させるのかを問いました。MDMAはセロトニントランスポーター(SERT)の機能を逆転させ、神経終末からセロトニンを大量に放出させることで知られています。研究者らがMDMA投与前に抗うつ薬フルオキセチンでこのトランスポーターを阻害すると、S(+)-MDMAによるヘッドツイッチ行動とIP1シグナルの増強は、雄雌ともに消失しました。フルオキセチンは古典的な直接的5-HT2Aアゴニストの効果を鈍らせなかったため、この遮断はMDMAがセロトニン放出に依存していることに特異的であることを示しています。つまり、MDMAは脳内で主に5-HT2Aを直接刺激するのではなく、シナプスにセロトニンを放出してそれが受容体および下流の可塑性を性差・立体異性体依存的に活性化するのです。
今後のMDMA治療への示唆
平たく言えば、本研究はMDMAが前頭皮質回路を再編する能力が、薬の正確な3次元形状、セロトニン系、そして生物学的な性という三者の相互作用に依存することを示しています。S(+)体は雄マウスの皮質でセロトニン依存のシグナル伝達や構造変化を促進しやすく、R(–)体はより弱く性により異なる振る舞いを示します。臨床で用いられるMDMAが両方の異性体の混合であることを踏まえると、将来の治療を微調整するには適切な立体異性体、用量、あるいは性別特異的なプロトコルの選択が必要になる可能性があります。より広く見れば、MDMAや関連化合物の治療的可能性の一部は、単一受容体で古典的サイケデリックのように振る舞うことよりも、脳自身のセロトニンを動員して柔軟で再配線された神経ネットワークを促す仕組みに由来するのかもしれません。
引用: Gaines-Smith, M.C., Silverman, J.M., Fiorillo, M. et al. Stereoselective, sex-dependent 5-HT2A receptor modulation of cortical plasticity by MDMA in mice. Neuropsychopharmacol. 51, 1011–1022 (2026). https://doi.org/10.1038/s41386-025-02313-x
キーワード: MDMA, セロトニン, 皮質可塑性, 性差, 5-HT2A受容体