Clear Sky Science · it
Accuratezza diagnostica, equità e implementazione clinica dell'IA per lo screening del cancro al seno: risultati di studi multicentrici retrospettivi e prospettici di fattibilità tecnica
Screening più intelligenti per le donne di tutti i giorni
Lo screening per il cancro al seno salva vite, ma mette anche sotto pressione i sistemi sanitari e può perdere tumori o generare falsi allarmi stressanti. Questo studio pone una domanda semplice ma dalle grandi implicazioni: un programma di intelligenza artificiale (IA) può aiutare in sicurezza a leggere le mammografie nel programma nazionale di screening del Regno Unito, identificando più tumori pericolosi mentre riduce il carico di lavoro dei specialisti sovraccarichi — e facendolo in modo equo per donne di diversi contesti?
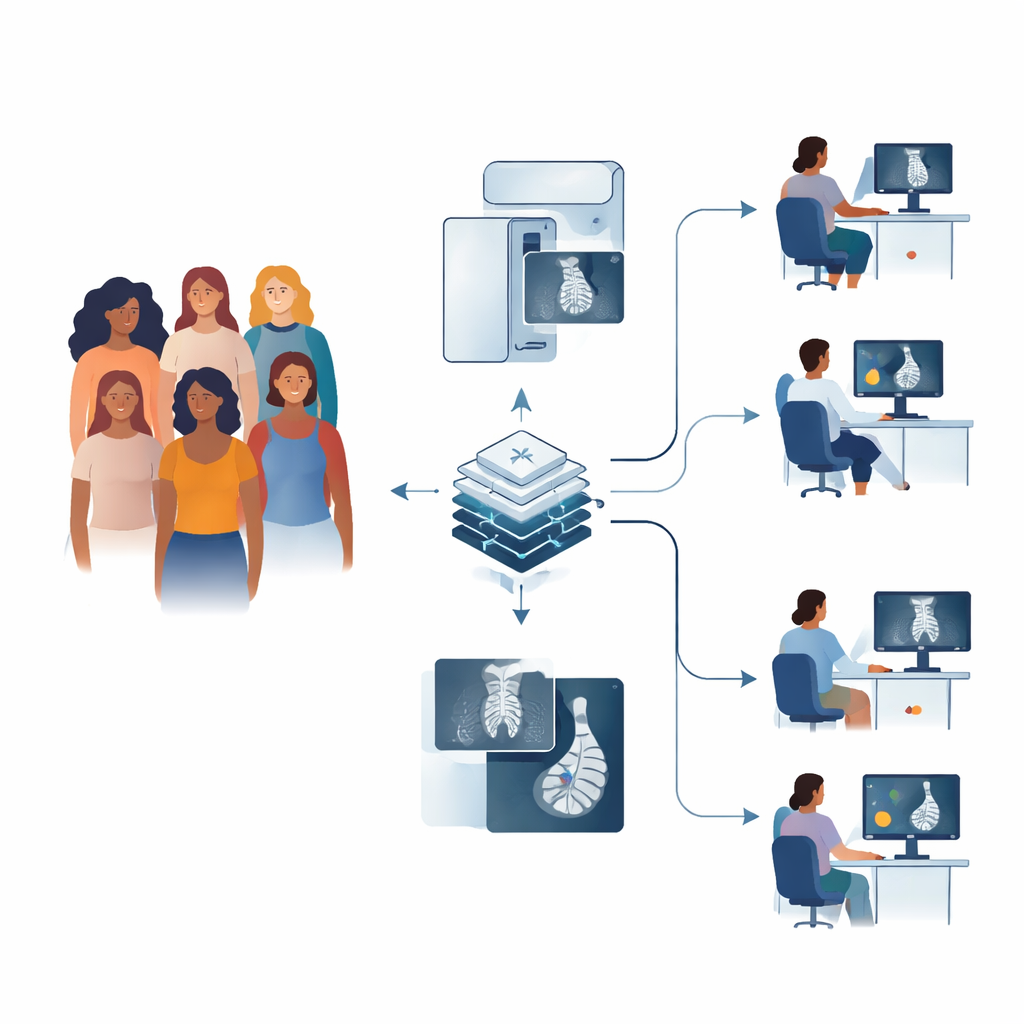
Come funziona oggi lo screening
In molti paesi, incluso il Regno Unito, alle donne di età compresa tra 50 e 70 anni viene offerta una mammografia periodica. Nel Regno Unito, ogni esame viene solitamente letto in modo indipendente da due esperti umani; se i lettori non concordano, il caso viene riesaminato da un pannello. Questo sistema a doppia lettura è pensato per essere sicuro, ma richiede tempo e dipende dalla disponibilità di lettori formati — una risorsa di cui molti sistemi sanitari scarseggiano. I primi strumenti informatici fornivano un aiuto limitato e a volte introducevano rumore anziché chiarezza, quindi le autorità sanitarie hanno richiesto solide prove prima di fidarsi dell’IA moderna all’interno dei programmi nazionali.
Mettere l’IA alla prova nelle cliniche reali
I ricercatori hanno valutato l’IA aggiornata per la mammografia di Google in due fasi principali nel Servizio Sanitario Nazionale del Regno Unito. Prima hanno eseguito il sistema su quasi 116.000 esami di screening passati provenienti da cinque diverse regioni, seguendo le donne per più di tre anni per verificare quali tumori effettivamente sono emersi. Hanno quindi confrontato le prestazioni dell’IA con quelle del primo lettore umano, del secondo lettore e della decisione finale del pannello. In una seconda fase, hanno installato silenziosamente l’IA in 12 siti di screening e l’hanno lasciata processare oltre 9.000 nuovi esami in tempo reale — senza influenzare le cure — per studiare come si comportasse nella pratica quotidiana e come fosse necessario tararne i parametri.
Cosa ha visto l’IA — e cosa ha individuato
Nel grande dataset retrospettivo, l’IA è risultata più sensibile del primo lettore umano: ha rilevato più tumori complessivamente mantenendo il tasso di falsi allarmi entro un margine di sicurezza predefinito. Se utilizzata come uno dei lettori nel flusso di lavoro a doppia lettura, il sistema avrebbe aumentato il tasso di rilevamento del cancro da circa 7,5 a 9,3 casi ogni 1.000 donne, e ha correttamente segnalato una donna su quattro con tumori che erano stati originariamente mancati e scoperti solo in seguito, o tra gli screening o alla successiva visita di routine. I guadagni sono stati particolarmente marcati nelle donne al primo screening — di solito il gruppo più difficile da interpretare perché non ci sono immagini pregresse. In queste visite iniziali, l’IA ha richiamato meno donne e al tempo stesso ha rilevato leggermente più tumori, in particolare tumori invasivi che rappresentano la minaccia maggiore.
Equità, carico di lavoro e ostacoli nel mondo reale
Il team ha esaminato con attenzione se l’IA trattasse in modo equo diversi gruppi di donne. Per età, densità mammaria, stato socioeconomico e i limitati dati di etnia disponibili, non hanno osservato segni coerenti di bias dannoso: sensibilità e specificità sono rimaste entro margini ristretti rispetto ai lettori umani, anche se alcuni sottogruppi molto piccoli presentavano ampia incertezza. Hanno anche modellato come l’uso dell’IA come secondo lettore riorganizzerebbe il lavoro. Il numero di letture umane prima della revisione del pannello potrebbe diminuire di quasi la metà, riducendo il tempo dei lettori di circa un terzo, anche se più casi verrebbero portati al pannello. Nella fase di fattibilità in vivo, l’IA ha fornito risultati in pochi minuti — molto più rapidamente della lettura umana di routine — ma il team ha scoperto una variazione nell’aspetto delle immagini recenti rispetto ai dati di addestramento più vecchi. Una soglia operativa iniziale si è rivelata troppo sensibile, provocando tassi di richiamo più elevati, e ha dovuto essere ricalibrata al ribasso usando dati locali aggiornati.
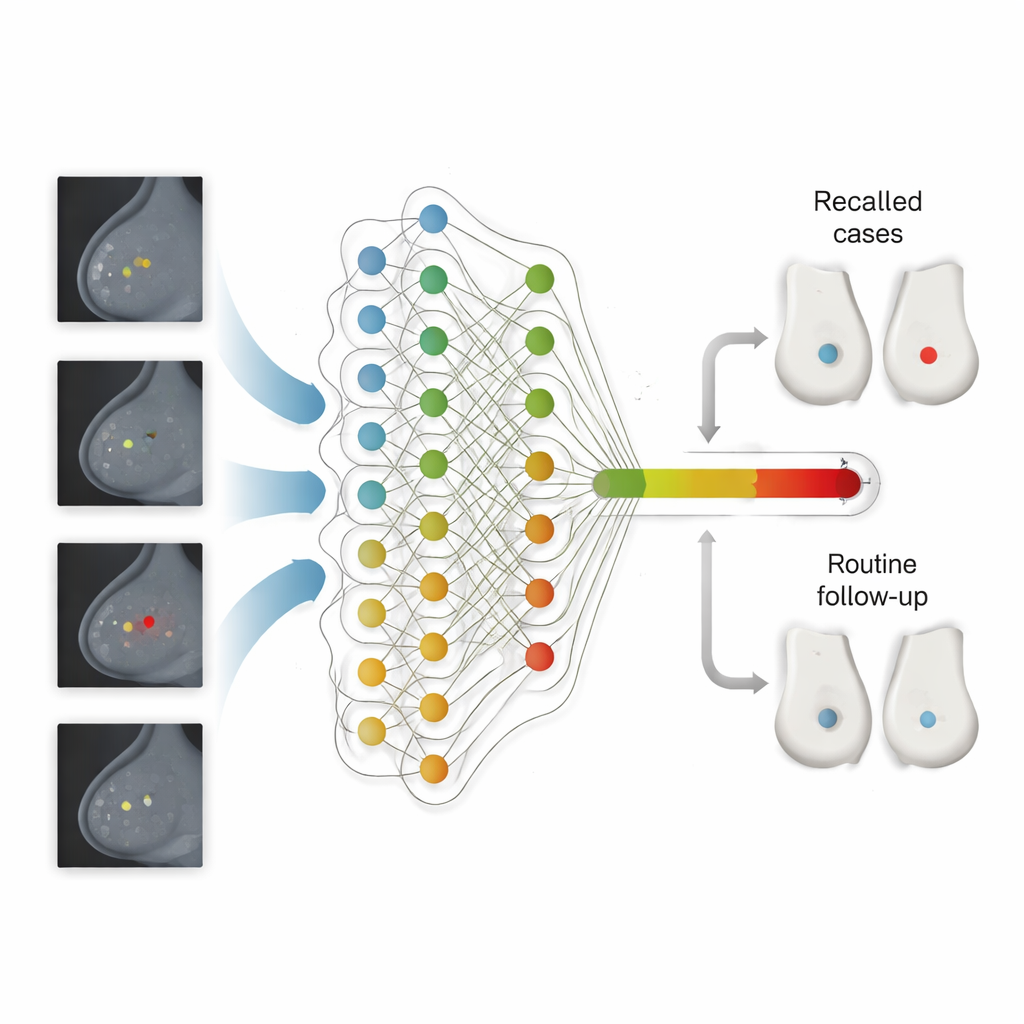
Costruire un sistema di screening pronto per l’IA
Oltre all’accuratezza, lo studio ha messo in luce barriere pratiche a un’implementazione sicura. Molti centri di screening dipendono ancora da moduli cartacei e software legacy che non possono memorizzare automaticamente i risultati dell’IA o spiegare perché un esame è stato richiamato — funzionalità di cui regolatori e clinici hanno bisogno. Gli autori sostengono che flussi di lavoro completamente digitali, standardizzati e una migliore raccolta dei dati demografici saranno cruciali per monitorare nel tempo prestazioni ed equità. Sottolineano inoltre che le soglie dell’IA non possono essere “impostate e dimenticate”: apparecchiature d’imaging, comportamento dei lettori e composizione della popolazione cambiano, perciò il sistema deve essere controllato e aggiustato continuamente, con regole nazionali chiare e supporto tecnico.
Cosa significa per le pazienti
I risultati suggeriscono che un sistema IA distribuito con attenzione potrebbe aiutare i programmi nazionali di screening a individuare più precocemente i tumori più gravi, soprattutto nelle donne al primo esame, riducendo al contempo il carico di lavoro degli specialisti sovraccarichi. Tuttavia gli autori rimarcano che il successo dipende da più di un algoritmo accurato. I servizi sanitari avranno bisogno di calibrazione continua, monitoraggio rigoroso per deriva e bias, infrastrutture IT aggiornate e un’integrazione ponderata nei flussi di lavoro umani esistenti. Con queste salvaguardie in atto, l’IA potrebbe diventare un lettore aggiuntivo di fiducia che migliora sia l’efficienza sia l’equità dello screening del cancro al seno, anziché una scatola nera che introduce nuovi rischi.
Citazione: Kelly, C.J., Wilson, M., Warren, L.M. et al. Diagnostic accuracy, fairness and clinical implementation of AI for breast cancer screening: results of multicenter retrospective and prospective technical feasibility studies. Nat Cancer 7, 494–506 (2026). https://doi.org/10.1038/s43018-026-01127-0
Parole chiave: screening del cancro al seno, intelligenza artificiale medica, mammografia, equità nell’assistenza sanitaria, implementazione clinica