Clear Sky Science · it
Analisi personalizzata delle vie di segnalazione nei tumori gastrointestinali per la stratificazione dei pazienti e la valutazione dei target farmacologici usando biopsie core derivate clinicamente
Perché questa ricerca è importante per i pazienti
I medici oncologi cercano sempre più spesso di abbinare i trattamenti alla biologia unica del tumore di ciascuna persona. Per i tumori del sistema digerente — come quelli del pancreas, del colon, del fegato o delle vie biliari — questo è particolarmente urgente, perché sono frequenti, spesso diagnosticati in stadio avanzato e difficili da trattare. Questo studio esplora un nuovo metodo di laboratorio in grado di leggere l’attività di molte proteine correlate al cancro a partire da minuscoli campioni di biopsia, con l’obiettivo di aiutare i medici a scegliere terapie più precise per singoli pazienti.
Dalle liste di DNA ai segnali vivi
Oggi la maggior parte delle cure “personalizzate” per il cancro si basa sulla lettura delle alterazioni del DNA nel tumore. Pur essendo potente, il DNA da solo non mostra quali segnali all’interno della cellula sono effettivamente attivi e guidano la crescita. Questi segnali sono veicolati dalle proteine, molte delle quali possono essere bersagliate direttamente dai farmaci. I ricercatori hanno utilizzato una tecnica ad alto rendimento chiamata DigiWest, una versione moderna del classico Western blot, per misurare contemporaneamente circa 130–200 proteine e le loro forme attivate. È importante che questo metodo richieda solo una quantità di materiale paragonabile a quella di una singola biopsia con ago, rendendolo adatto all’uso clinico di routine.
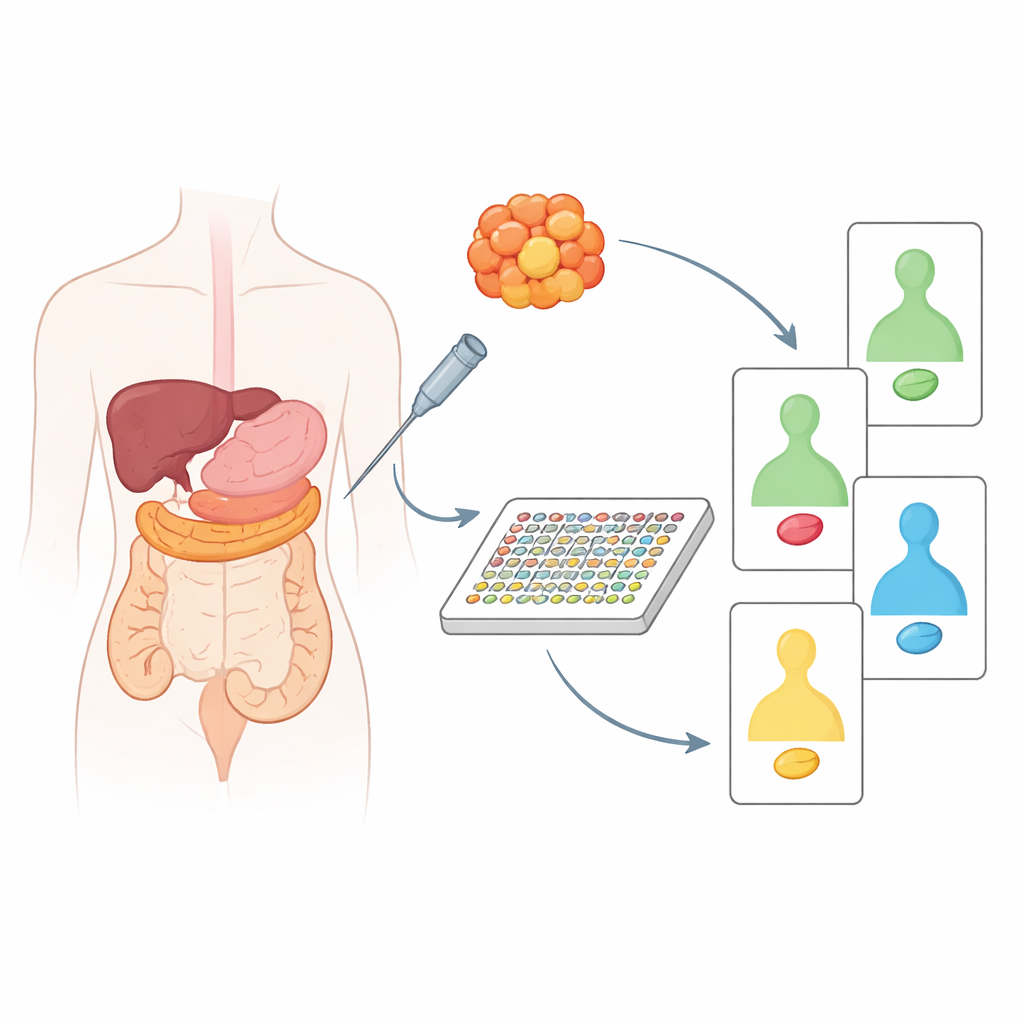
Confrontare il tessuto tumorale con il tessuto sano vicino
Il gruppo ha prima analizzato tessuti conservati provenienti da 20 pazienti con tumore pancreatico o colorettale, sempre accoppiati al tessuto non canceroso vicino della stessa persona. Confrontando i tumori con i loro corrispondenti sani, hanno potuto vedere quali proteine erano realmente alterate dal cancro piuttosto che riflettere semplici differenze fisiologiche tra organi. Ciò ha rivelato contrasti netti nel comportamento di noti guardiani e driver del cancro, come p53, Ras, PTEN e altri. I tumori pancreatici, ad esempio, tendevano a mostrare segnali pro‑crescita potenziati e perdita di proteine protettive, mentre i tumori del colon avevano un loro pattern distinto di vie alterate. Quando i ricercatori hanno raggruppato i campioni in base a questi cambiamenti proteici, sono riusciti a dividere i tumori pancreatici in due gruppi biologicamente differenti e a rilevare differenze significative tra i tumori del colon correlate all’età dei pazienti e alla posizione della neoplasia nell’intestino.
“Codici a barre” individuali dell’attività di segnalazione
Andando oltre le medie di gruppo, gli scienziati hanno costruito un profilo proteico dettagliato per ciascun tumore. Questi profili hanno evidenziato quali rotte di segnalazione — come quelle che coinvolgono mTOR, MAPK/Erk, Wnt o fattori legati al sistema immunitario — erano particolarmente attive o spente. Molte delle proteine misurate sono bersagli diretti di farmaci esistenti, o si trovano subito a valle di tali bersagli, permettendo al team di inferire quali medicinali potrebbero interferire con i principali motori di crescita di un tumore. In tre quarti dei casi retrospettivi, sono riusciti a indicare una o più vie che probabilmente alimentavano la progressione tumorale. Hanno anche individuato tumori ricchi di marcatori delle cellule immunitarie, suggerendo tumori “caldi” che potrebbero rispondere all’immunoterapia, e casi inusuali con firme particolarmente distintive.
Applicare il metodo a pazienti reali
Per testarene l’utilità a livello clinico, i ricercatori hanno poi applicato DigiWest a biopsie fresche con ago provenienti da 14 pazienti con vari tumori gastrointestinali i cui casi erano in esame da parte di un Molecular Tumor Board. Questi pazienti avevano storie cliniche complesse e, spesso, trattamenti pregressi. Poiché non era disponibile tessuto sano abbinato, i livelli proteici di ciascun tumore sono stati confrontati con il livello mediano del gruppo per definire cosa considerare anormalmente alto o basso. Anche con questo approccio più restrittivo, 12 dei 14 tumori hanno mostrato pattern chiari e rilevanti per il trattamento. In due esempi dettagliati, i dati proteici hanno confermato un’amplificazione a livello di DNA del gene FGFR2 in un tumore del colon e la perdita di un freno su mTOR in un tumore del fegato, supportando con forza la considerazione da parte del Board di farmaci inibitori di FGFR o di mTOR. Nel complesso, i risultati DigiWest concordavano con i principali driver genetici e suggerivano target farmacologici nella maggior parte dei casi valutabili.
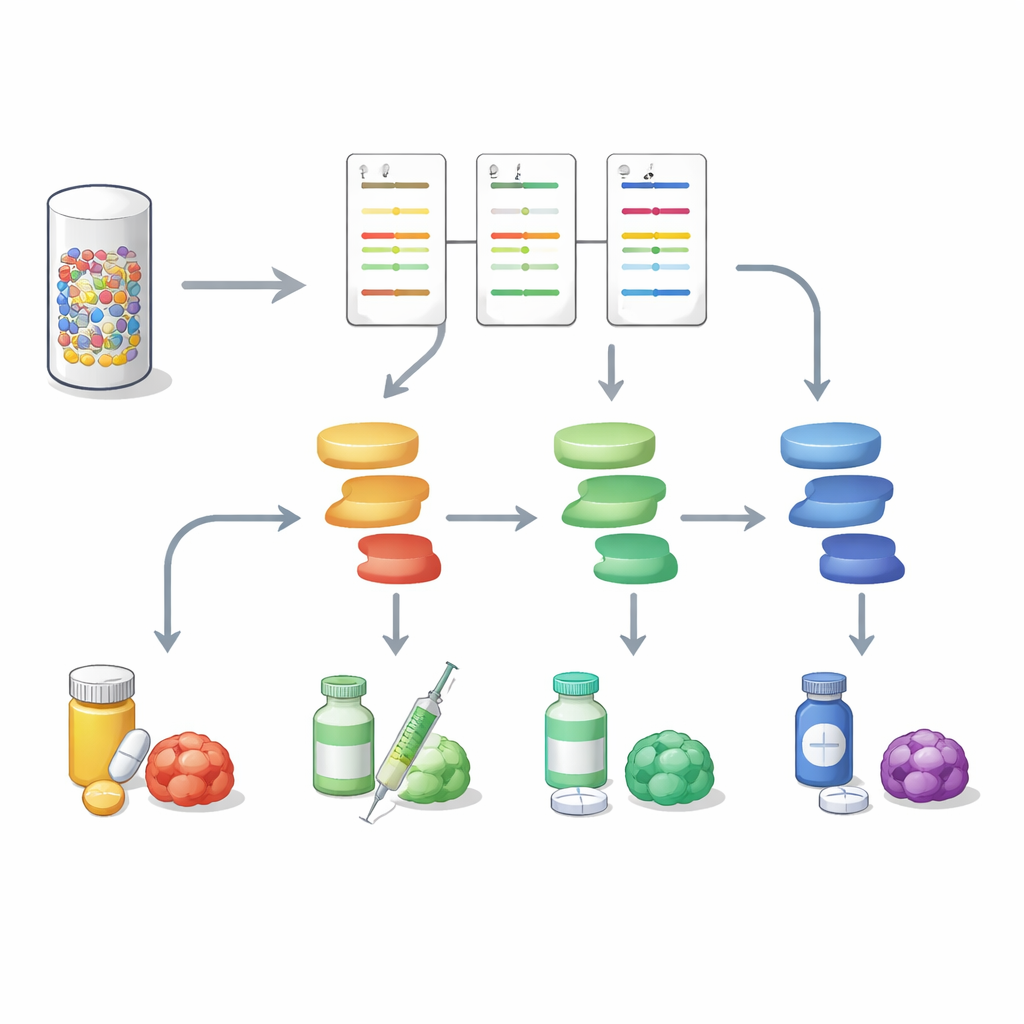
Verso ritratti tumorali più completi
Questo lavoro dimostra che analizzare la segnalazione proteica in parallelo al sequenziamento del DNA può fornire un quadro più ricco e utilizzabile dei tumori gastrointestinali. Trasformando una piccola biopsia in una mappa di attività multivie, DigiWest aiuta a distinguere quali interruttori molecolari sono effettivamente attivi in un dato cancro e quali farmaci potrebbero colpirli al meglio, e può anche segnalare vie di resistenza emergenti. Pur richiedendo ulteriori studi su scala più ampia, l’approccio offre un modo praticabile per portare la profilazione proteica ad alto contenuto nella oncologia di precisione di tutti i giorni e avvicinarsi a piani terapeutici tarati sul tumore vivente di ciascun paziente, non solo sul suo schema genetico.
Citazione: Stahl, A., Büringer, K., Missios, P. et al. Personalized signaling pathway analysis of gastrointestinal tumors for patient stratification and drug target evaluation using clinically derived core biopsies. npj Precis. Onc. 10, 124 (2026). https://doi.org/10.1038/s41698-026-01304-5
Parole chiave: oncologia di precisione, cancro gastrointestinale, proteomica, profilazione delle biopsie, terapia mirata