Clear Sky Science · it
Strategie antimicrobiche di nanoparticelle e agenti chelanti per ridurre la contaminazione da Staphylococcus spp. sulle superfici dei macelli
Perché la pulizia degli impianti di lavorazione della carne riguarda tutti
Dietro ogni bistecca o petto di pollo nel supermercato c’è una rete di tubi, tavoli, scarichi e ganci nei grandi macelli. Su queste superfici, microrganismi tenaci possono insediarsi in strati vischiosi molto difficili da rimuovere. Alcuni di questi batteri non solo possono deteriorare gli alimenti e causare malattie, ma trasportano anche geni che li aiutano a sopravvivere agli antibiotici. Questo studio esplora un nuovo modo per pulire quegli angoli nascosti usando particelle metalliche minuscole combinate con sostanze ausiliarie, con l’obiettivo di fermare sia i germi sia i tratti di resistenza ai farmaci che essi diffondono.
Germi nascosti sulle superfici di lavoro
I ricercatori si sono concentrati sugli stafilococchi, un gruppo di batteri che può causare infezioni cutanee, setticemia e intossicazioni alimentari nell’uomo. Hanno raccolto campioni da diverse aree di un macello—sale di taglio, celle frigorifere, aree di macellazione e servizi igienici—e hanno identificato diversi ceppi di Staphylococcus, incluso il noto Staphylococcus aureus. Quattro dei sei ceppi principali si sono rivelati multidrug-resistenti, cioè in grado di resistere a molti antibiotici usati in clinica. Ancora più preoccupante è che questi batteri formavano biofilm: comunità sottili e appiccicose aderenti a acciaio e plastica che proteggono i microrganismi da saponi, disinfettanti e farmaci.
Piccoli metalli e collaboratori intelligenti fanno squadra
Per affrontare questi microrganismi ostinati, il team ha testato quattro tipi di nanoparticelle metalliche—oro, argento, ossido di zinco e ossido di rame—insieme a EDTA, un comune composto chelante che lega i metalli, e a una miscela disinfettante domestica chiamata HLE a base di perossido di idrogeno, acido lattico ed EDTA. Da soli, questi agenti hanno mostrato risultati variabili, con alcune nanoparticelle che richiedevano dosi relativamente elevate per fermare la crescita batterica. Tuttavia, quando le nanoparticelle sono state combinate con EDTA o HLE, il quadro è cambiato. Diverse combinazioni, in particolare oro più EDTA, argento più HLE e ossido di zinco più EDTA, hanno funzionato molto meglio di ciascun componente preso singolarmente. Queste miscele sono state in grado di inibire le cellule libere nuotanti e di attaccare anche i batteri già insediati nei biofilm aderenti alle superfici.
Smantellare i biofilm e pulizia profonda
I ricercatori hanno poi approfondito lo studio su tre dei ceppi più resistenti per valutare come i trattamenti agissero sui biofilm, sia durante la loro formazione sia dopo che erano stabiliti. Gli agenti singoli hanno avuto qualche effetto: per esempio, le nanoparticelle di ossido di zinco e l’HLE potevano rallentare parzialmente la crescita del biofilm, e alcune nanoparticelle o l’EDTA da soli potevano erodere i biofilm maturi. Ma i risultati più significativi sono emersi dalle combinazioni. Nanoparticelle d’oro o d’argento abbinate a EDTA o HLE hanno ridotto il numero di cellule vive nei biofilm preformati fino a quasi otto ordini di grandezza. In termini pratici, queste miscele hanno fatto molto più che assottigliare lo strato di limo: hanno quasi annientato le comunità protette attaccate alle superfici.
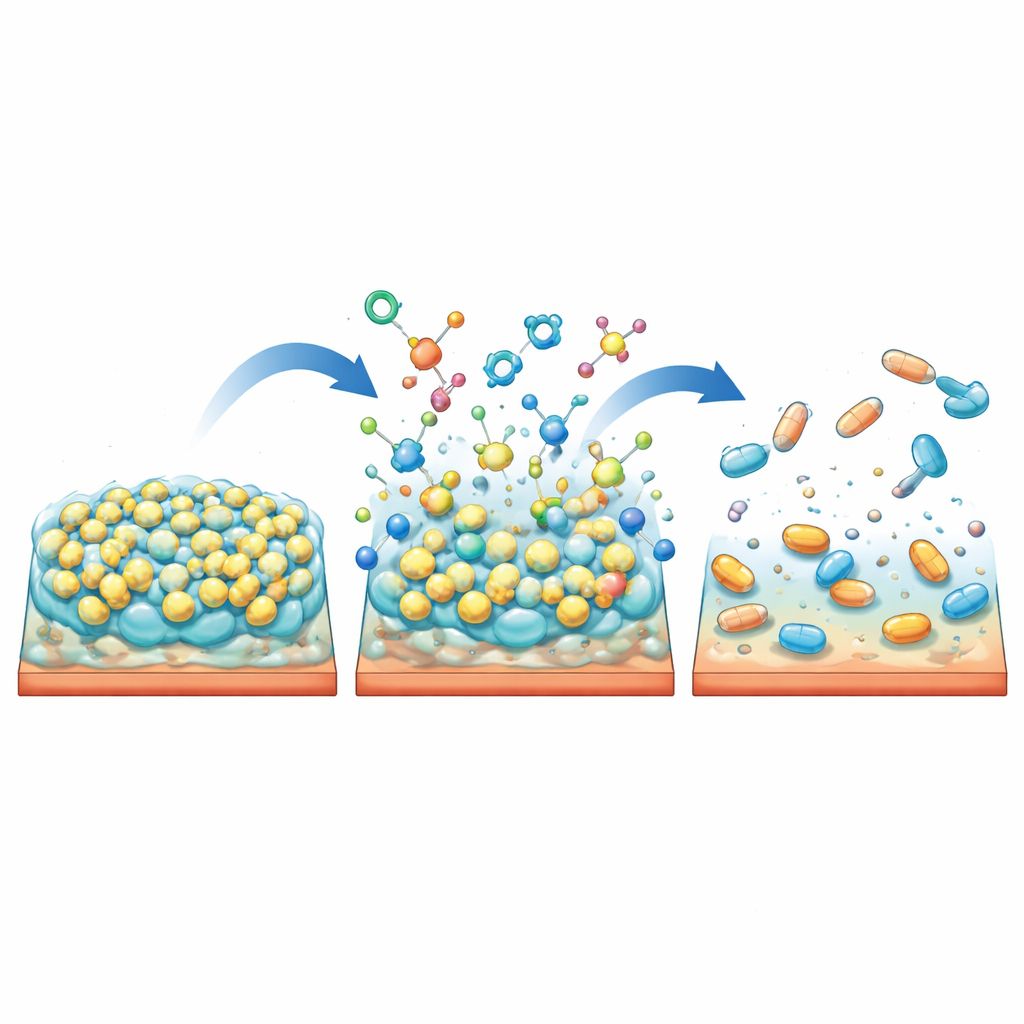
Quando l’adattamento rende i batteri meno pericolosi
L’uso di antimicrobici potenti solleva una preoccupazione importante: i batteri si adatteranno e diventeranno ancora più difficili da uccidere? Per indagare questo aspetto, il team ha esposto ripetutamente i ceppi più resistenti a dosi subletali di nanoparticelle, quindi ha riesaminato la loro risposta agli antibiotici standard. Sorprendentemente, invece di diventare più robusti, molti dei batteri adattati sono risultati più facili da trattare. Le loro concentrazioni minime inibitorie per antibiotici chiave sono diminuite, in alcuni casi passando da resistenti a chiaramente suscettibili. I test genetici hanno mostrato che diversi geni di resistenza noti, inclusi quelli collegati a macrolidi, sulfonamidi, cloramfenicolo e pompe di efflusso multidroga, risultavano meno attivi dopo l’adattamento alle nanoparticelle. Osservazioni microscopiche e lavori precedenti suggeriscono che le nanoparticelle possano danneggiare gli involucri cellulari e la fisiologia complessiva delle cellule in modi che rendono il mantenimento dei tratti di resistenza più oneroso per i batteri.
Cosa significa per una filiera alimentare più sicura
Complessivamente, lo studio dimostra che nanoparticelle metalliche combinate con agenti chelanti come l’EDTA o con il disinfettante HLE possono svolgere una doppia funzione nei macelli. Innanzitutto agiscono come detergenti potenti che penetrano e distruggono i biofilm, riducendo notevolmente il numero di stafilococchi multiresistenti sulle superfici di lavoro. In secondo luogo, l’adattamento a lungo termine a queste nanoparticelle può spingere alcuni batteri a ridurre o addirittura perdere la loro resistenza agli antibiotici, anziché accentuarla. Sebbene l’implementazione sul campo richiederà attente valutazioni di sicurezza e ambientali, queste formulazioni offrono uno strumento promettente per mantenere la filiera alimentare e gli ambienti circostanti più liberi da “superbatteri” difficili da trattare.
Citazione: Naim, W., Caballero Gómez, N., González Romero, S. et al. Antimicrobial strategies of nanoparticles and chelating agents for mitigating Staphylococcus spp. contamination on slaughterhouse surfaces. Sci Rep 16, 11804 (2026). https://doi.org/10.1038/s41598-026-41026-z
Parole chiave: resistenza antimicrobica, nanoparticelle, sicurezza alimentare, biofilm, igiene dei macelli