Clear Sky Science · it
Tofacitinib ripara l'infiammazione e la disfunzione mitocondriale nei macrofagi della RA riprogrammati da GM-CSF
Perché è importante per le persone con artrite
L'artrite reumatoide non riguarda solo le articolazioni doloranti: è sostenuta da cellule immunitarie iperattive che risiedono nella membrana sinoviale. Questo studio mostra che una pillola comune per l'artrite reumatoide, il tofacitinib, può calmare un gruppo particolarmente ostinato di queste cellule correggendo sia il loro comportamento infiammatorio sia i loro “impianti di energia” danneggiati, i mitocondri. Comprendere questo riprogrammarsi cellulare nascosto aiuta a spiegare perché alcuni trattamenti falliscono e indica strategie più intelligenti per controllare il danno articolare e il dolore.
I guardiani dell'articolazione che creano problemi
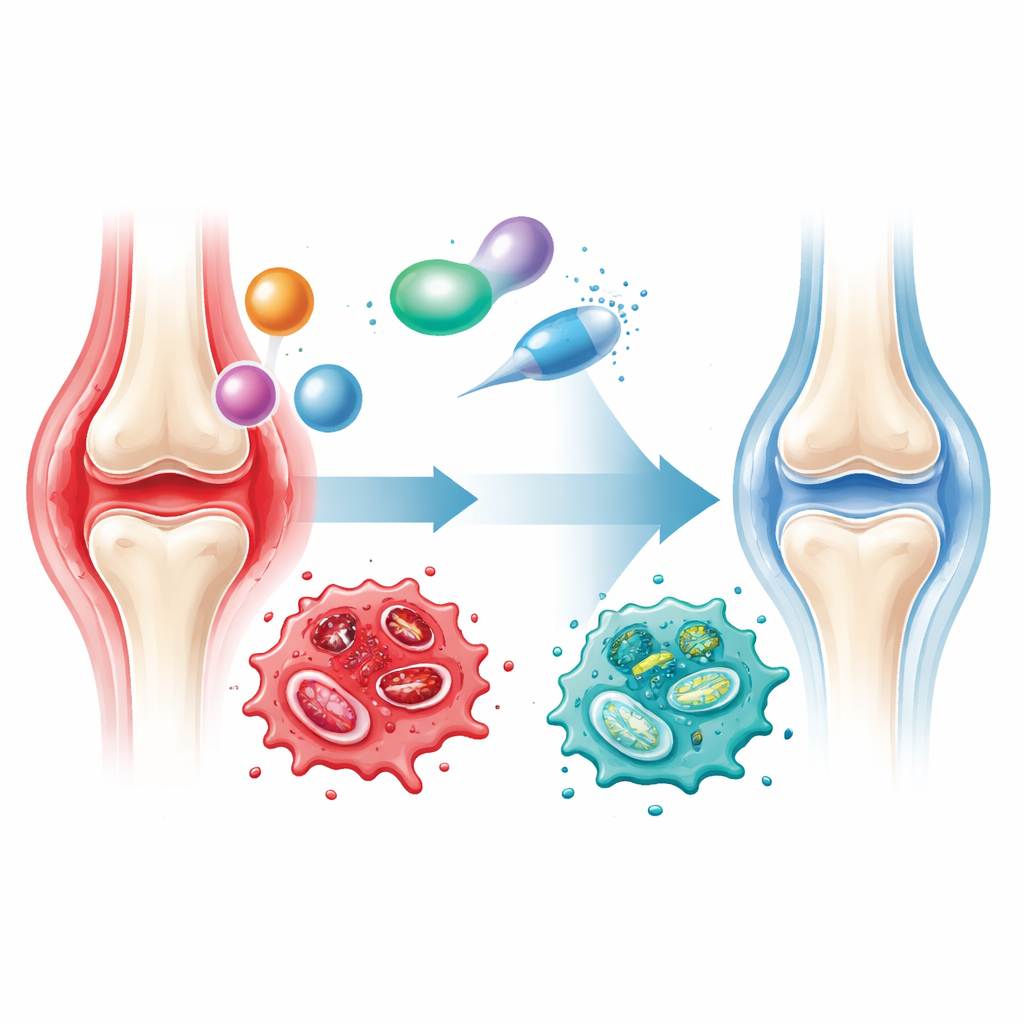
Nelle articolazioni sane, un tipo di globulo bianco chiamato macrofago pulisce discretamente i detriti e favorisce la riparazione. Nell'artrite reumatoide, queste cellule si accumulano nella membrana articolare e diventano potenti promotrici dell'infiammazione. I ricercatori si sono concentrati su un segnale chiamato GM-CSF, presente in alte concentrazioni nelle articolazioni e nel sangue dei pazienti con RA. I macrofagi che ricevono questo segnale tramite il recettore corrispondente si bloccano in uno stato dannoso: rilasciano molecole infiammatorie come IL-1 beta e proteine S100 e perdono l'espressione di geni che normalmente limitano l'infiammazione. Le analisi dei campioni articolari dei pazienti hanno mostrato che questo programma di risposta a GM-CSF compare precocemente nella malattia, persiste nella artrite a lungo termine e si associa alle misure di attività della malattia.
Quando le centrali energetiche cellulari perdono l'equilibrio
Questi macrofagi plasmati da GM-CSF non sono solo arrabbiati; sono riorganizzati metabolicamente. Invece di utilizzare principalmente i mitocondri per produrre energia in modo efficiente, si spostano verso una rapida combustione degli zuccheri (glicolisi). Enzimi chiave del ciclo energetico cellulare vengono soppressi, portando all'accumulo di prodotti intermedi come citrato e succinato e all'attivazione del fattore sensibile all'ossigeno HIF-1α. All'interno delle cellule, i mitocondri diventano frammentati e più numerosi, un segno strutturale di stress. Le misurazioni hanno confermato che la maggior parte dell'ATP cellulare — l'energia chimica — deriva ora dalla glicolisi piuttosto che dalle vie mitocondriali, e i tessuti articolari dei pazienti mostrano lo stesso orientamento verso la rottura mitocondriale.
Perché molti farmaci standard non bastano
Il gruppo ha poi valutato se le terapie attuali possano correggere questo stato alterato. I farmaci che bloccano TNF o il recettore dell'IL-6 — pilastri del trattamento dell'artrite reumatoide — così come i tradizionali farmaci modificanti la malattia, hanno avuto scarso effetto sui livelli di GM-CSF o sul suo recettore nella membrana articolare. Rallentare direttamente l'ingresso degli zuccheri nelle cellule o bloccare parzialmente la respirazione mitocondriale ha attenuato alcuni aspetti dello spostamento metabolico e ha ripristinato alcuni geni legati alla riparazione, ma il programma infiammatorio centrale e la struttura mitocondriale danneggiata sono rimasti in gran parte intatti. In altre parole, semplicemente tagliare la fonte di carburante non ha riportato questi macrofagi a uno stato sano e bilanciato.
Una pillola che ripristina le cellule infiammate
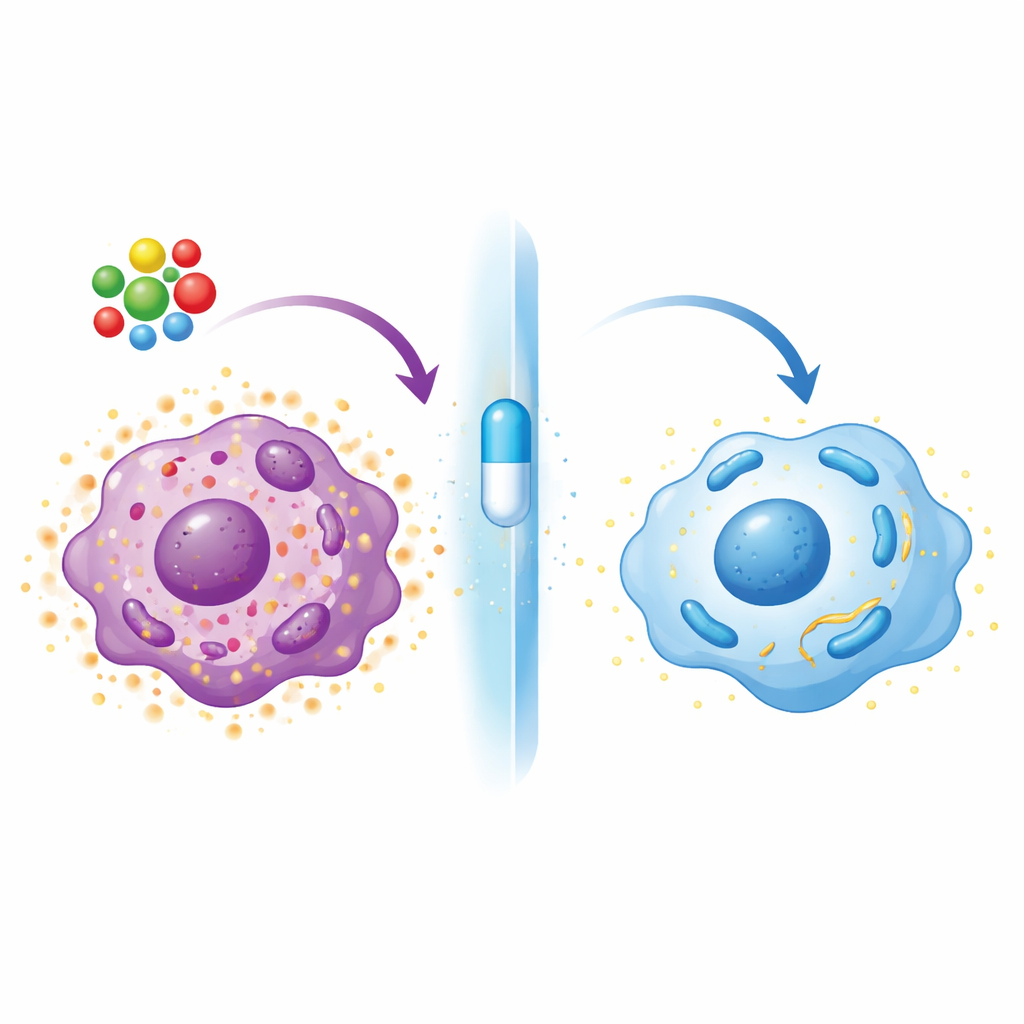
Il tofacitinib, un farmaco orale che blocca la via JAK-STAT, ha raccontato una storia diversa. Sia nei macrofagi derivati dal sangue sia in frammenti di tessuto articolare di pazienti coltivati in laboratorio, il tofacitinib ha ridotto il recettore di GM-CSF, spento la via STAT5 e spostato le cellule lontano dal profilo ricco di IL-1 beta e S100 verso uno più regolatorio, caratterizzato da IL-10 e altri geni calmanti. La produzione energetica è stata riallineata verso i mitocondri: gli enzimi chiave del ciclo energetico si sono ripristinati, sono diminuiti i livelli di specie reattive dell'ossigeno e di lattato e si è ridotta la frammentazione mitocondriale. Cambiamenti simili sono emersi in un modello murino in cui un eccesso di GM-CSF è stato iniettato nelle articolazioni per scatenare l'artrite: il tofacitinib ha ridotto il gonfiore, i marker infiammatori, gli enzimi glicolitici e i segni di stress mitocondriale nei macrofagi articolari.
Cosa significa per le persone che vivono con RA
Per chi convive con l'artrite reumatoide, questi risultati suggeriscono che non tutti i farmaci agiscono sui driver più profondi dell'infiammazione articolare. Segnali come GM-CSF possono spingere i macrofagi in uno stato autosufficiente, ad alto consumo di zuccheri e ad alto stress, che molti trattamenti standard non riescono a invertire completamente. Il tofacitinib, spegnendo un interruttore chiave all'interno di queste cellule (STAT5), sembra in grado sia di attenuare la tempesta infiammatoria sia di riparare i sistemi energetici interni delle cellule. Questa azione doppia può contribuire a spiegare i suoi benefici clinici e sottolinea il valore di terapie che affrontano contemporaneamente i segnali immunitari e il metabolismo cellulare per proteggere meglio le articolazioni.
Citazione: Satoeya, N., Zack, S.R., Zoubi, O.A. et al. Tofacitinib repairs inflammation and mitochondrial dysregulation in GM-CSF-reprogrammed RA macrophages. Cell Mol Immunol 23, 417–431 (2026). https://doi.org/10.1038/s41423-026-01395-x
Parole chiave: artrite reumatoide, macrofagi, GM-CSF, tofacitinib, metabolismo cellulare