Clear Sky Science · it
Mirare alle vie che guidano la resistenza a ibrutinib tramite miR-28 in ABC-DLBCL
Fermare la ricomparsa del cancro
Molti farmaci antitumorali moderni funzionano bene all’inizio, ma perdono efficacia man mano che i tumori evolvono strategie di fuga. Questo studio esamina una forma ostinata di cancro del sangue chiamata linfoma diffuso a grandi cellule B, concentrandosi su un sottotipo difficile da trattare e su un farmaco ampiamente usato, l’ibrutinib. I ricercatori pongono una domanda semplice ma urgente: invece di inseguire la resistenza solo dopo che è comparsa, possiamo prevenire l’emergere di cellule tumorali resistenti fin dall’inizio usando una piccola molecola di RNA chiamata miR-28?
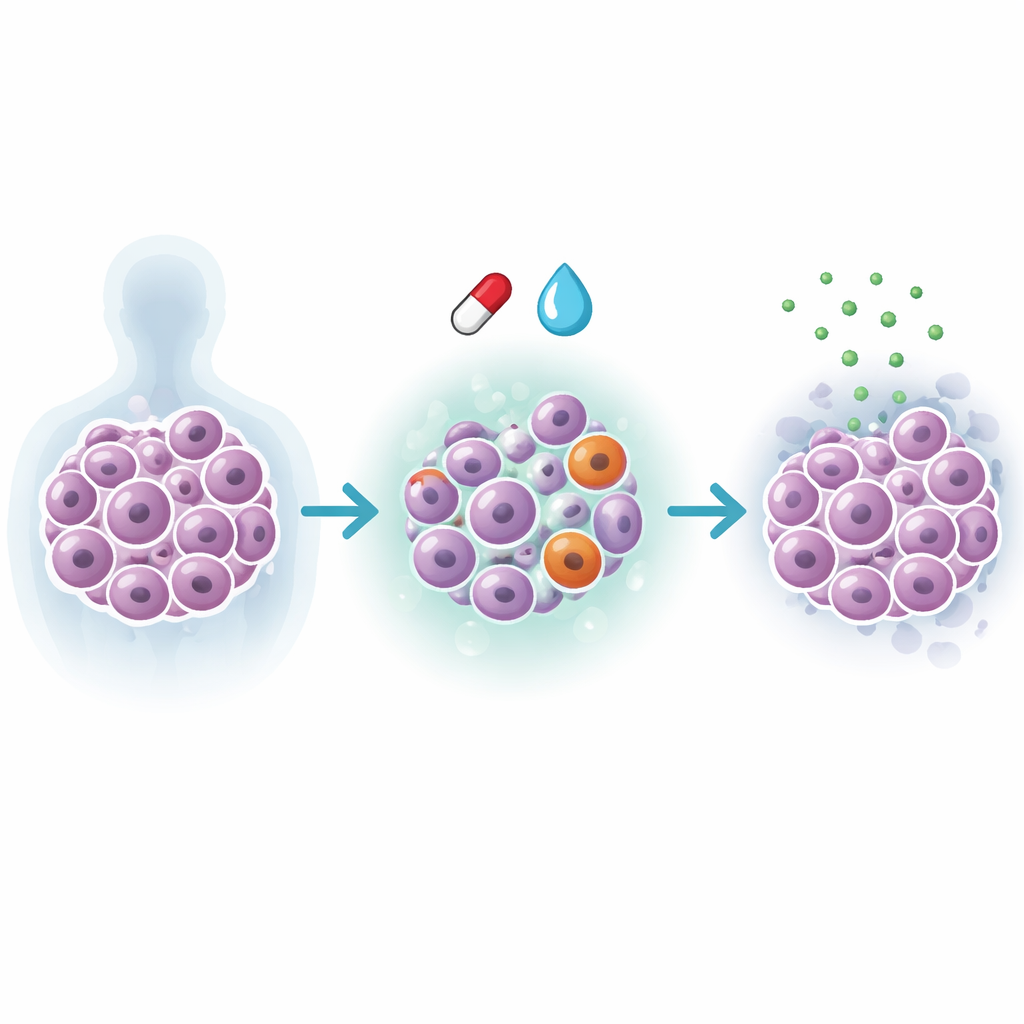
Un linfoma difficile e un farmaco che perde efficacia
Il linfoma diffuso a grandi cellule B è il linfoma aggressivo più comune. La chemioterapia immunologica standard guarisce molti pazienti, ma chi ha tumori appartenenti al sottotipo activated B‑cell (ABC) spesso va incontro a recidiva. Per questi pazienti l’ibrutinib, una compressa che blocca un interruttore di sopravvivenza chiave nelle cellule B, è stato un progresso importante. Tuttavia i suoi benefici sono spesso temporanei: col tempo, gruppi di cellule linfomatose si adattano, sopravvivono al farmaco e guidano la ricomparsa del cancro. Queste vie di fuga possono coinvolgere mutazioni del DNA, ma anche una riorganizzazione più sottile dei circuiti di controllo e del metabolismo cellulare che i test standard possono non rilevare.
Un piccolo RNA con grande influenza
I microRNA sono brevi filamenti di RNA che regolano finemente l’uso di centinaia di geni all’interno delle cellule. Non codificano proteine, ma agiscono più come dimmer sui programmi esistenti. Il miR‑28 è una di queste molecole, che normalmente contribuisce a tenere sotto controllo le cellule B. Spesso è ridotto nei linfomi delle cellule B e lavori precedenti hanno dimostrato che ristabilirne i livelli può rallentare la crescita tumorale e rendere le cellule linfomatose più vulnerabili all’ibrutinib. In questo studio gli autori hanno chiesto se un’attività costante di miR‑28 possa effettivamente bloccare la comparsa di cloni resistenti all’ibrutinib nel linfoma di tipo ABC.
Osservare la competizione tra cloni tumorali
Per seguire come emerge la resistenza, il gruppo ha mischiato cellule linfomatose in grado di attivare miR‑28 con cellule di controllo e le ha coltivate insieme sotto dosi di ibrutinib aumentate lentamente. Utilizzando marcatori fluorescenti colorati e citometria a flusso, hanno tracciato come diversi cloni aumentavano o diminuivano nell’arco di diverse settimane. Nelle colture di controllo, una piccola frazione di cellule si adattava ai livelli crescenti di farmaco, si espandeva e finiva per dominare — una riproduzione in laboratorio della recidiva clinica. Quando miR‑28 veniva attivato, questa presa da parte dei cloni era attenuata: i cloni con caratteristiche di resistenza comparivano meno spesso e la diversità complessiva della popolazione rimaneva più alta, mostrando che miR‑28 interferiva attivamente con la selezione dei vincitori tolleranti al farmaco.
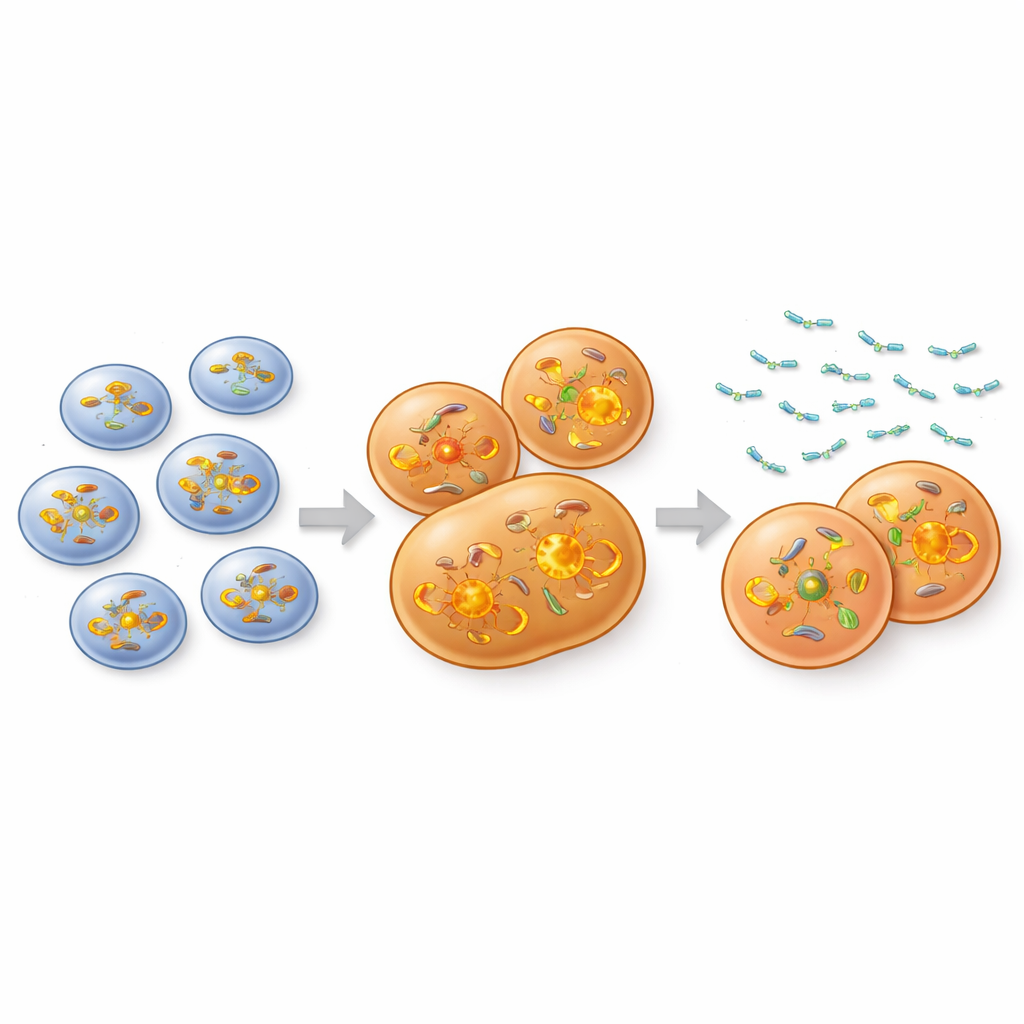
Interrompere i circuiti energetici e di crescita del tumore
Per capire come miR‑28 eserciti questo effetto, i ricercatori hanno confrontato l’attività genica in cellule sensibili, in cellule che stavano diventando resistenti e in cellule che esprimevano miR‑28, tutte raccolte a metà del processo di sviluppo della resistenza. Le cellule sulla via della resistenza avevano attivato programmi collegati ai mitocondri — le centrali energetiche della cellula — e alla via mTOR, un controllore centrale della crescita e della sintesi proteica. miR‑28 ha agito in direzione opposta su questi stessi programmi, abbassando l’espressione di molti dei geni e delle vie di cui le cellule resistenti dipendono. Misurazioni dirette hanno confermato che le cellule che esprimevano miR‑28 avevano meno mitocondri, producevano meno energia mitocondriale e mostravano un’attività mTOR ridotta. Nei dati dei pazienti dello studio clinico PHOENIX, i tumori i cui profili genici somigliavano a questo stato indotto da miR‑28 erano associati a una sopravvivenza migliore negli anziani trattati con ibrutinib, suggerendo che la stessa circuiteria è rilevante nei tumori reali.
Trasformare miR‑28 in una medicina mirata
Infine, il gruppo ha testato se somministrare miR‑28 dall’esterno potesse rallentare tumori già resistenti all’ibrutinib cresciuti nei topi. Iniezioni dirette di miR‑28 sintetico nei linfomi resistenti hanno ridotto le dimensioni dei tumori, con effetti più marcati nelle cellule resistenti rispetto alle loro controparti naive al farmaco. Per avvicinarsi a una terapia pratica, hanno legato i mimetici di miR‑28 a piccole nanoparticelle d’oro decorate con aptameri — brevi filamenti simili al DNA che riconoscono marcatori di superficie delle cellule linfomatose. Queste particelle mirate, somministrate sia direttamente nel tumore sia per via sistemica, si sono dirette verso i tumori resistenti e ne hanno frenato la crescita in diversi modelli di linfoma, mentre le particelle di controllo hanno avuto scarso effetto.
Cosa potrebbe significare per i pazienti
In termini chiari, questo lavoro mostra che miR‑28 può sia prevenire sia colpire il linfoma resistente all’ibrutinib interrompendo i programmi energetici e di crescita di cui le cellule resistenti dipendono. Invece di aspettare che il cancro si adatti e poi cercare di colpire ogni nuova via di fuga, miR‑28 agisce in modo più ampio, modulando molti geni contemporaneamente per rendere più difficile l’instaurarsi della resistenza. Abbinato a vettori di somministrazione intelligenti come nanoparticelle guidate da aptameri, miR‑28 o strategie simili basate su microRNA potrebbero un giorno essere aggiunte ai trattamenti esistenti per mantenere più a lungo l’efficacia di farmaci potenti come l’ibrutinib nei pazienti con linfomi ad alto rischio.
Citazione: Álvarez-Corrales, E., Moreno-Palomares, R., Gómez-Escolar, C. et al. Targeting of ibrutinib resistance–driving pathways by miR-28 in ABC-DLBCL. Leukemia 40, 894–905 (2026). https://doi.org/10.1038/s41375-026-02948-9
Parole chiave: linfoma diffuso a grandi cellule B, resistenza ai farmaci, ibrutinib, microRNA-28, nanoparticelle mirate