Clear Sky Science · he
ניתוח מותאם אישית של מסלולי איתות בגידולי מערכת העיכול למטרות סיווג מטופלים והערכת מטרות תרופתיות באמצעות דגימות ליבה קליניות
מדוע המחקר הזה חשוב עבור מטופלים
רופאי הסרטן מנסים יותר ויותר להתאים טיפולים לביולוגיה הייחודית של הגידול אצל כל מטופל. בסרטנים של מערכת העיכול — כגון סרטני הלבלב, המעי הגס, הכבד או צינורות המרה — הדבר דחוף במיוחד, שכן הם שכיחים, מאובחנים לעתים קרובות מאוחר וקשים לטיפול. עבודה זו בוחנת שיטה מעבדתית חדשה שיכולה לקרוא את הפעילות של חלבונים רבים הקשורים לסרטן מתוך דגימות ביופסיה זעירות, במטרה לסייע לרופאים לבחור טיפולים מדויקים יותר עבור כל מטופל.
מרשימות DNA לאיתותים חיים
כיום רוב הטיפול ה"ממותג" בסרטן מסתמך על קריאת שינויים ב‑DNA של הגידול. למרות היותה חזקה, ה‑DNA לבדו לא מראה אילו מסלולים בתוך התא באמת דלוקים ומניעים גדילה. אותות אלה נישאים על ידי חלבונים, רבים מהם ניתנים למיקוד ישיר בעזרת תרופות. החוקרים השתמשו בטכניקה מהירה הנקראת DigiWest, גרסה מודרנית של Western blot הקלאסי, כדי למדוד בו‑זמנית כ‑130–200 חלבונים וצורותיהם המופעלות. משמעותי ששיטה זו דורשת רק כמות חומר השווה בערך לביופסיה מחט יחידה, מה שהופך אותה לשימושית במצבי קליני שגרתיים.
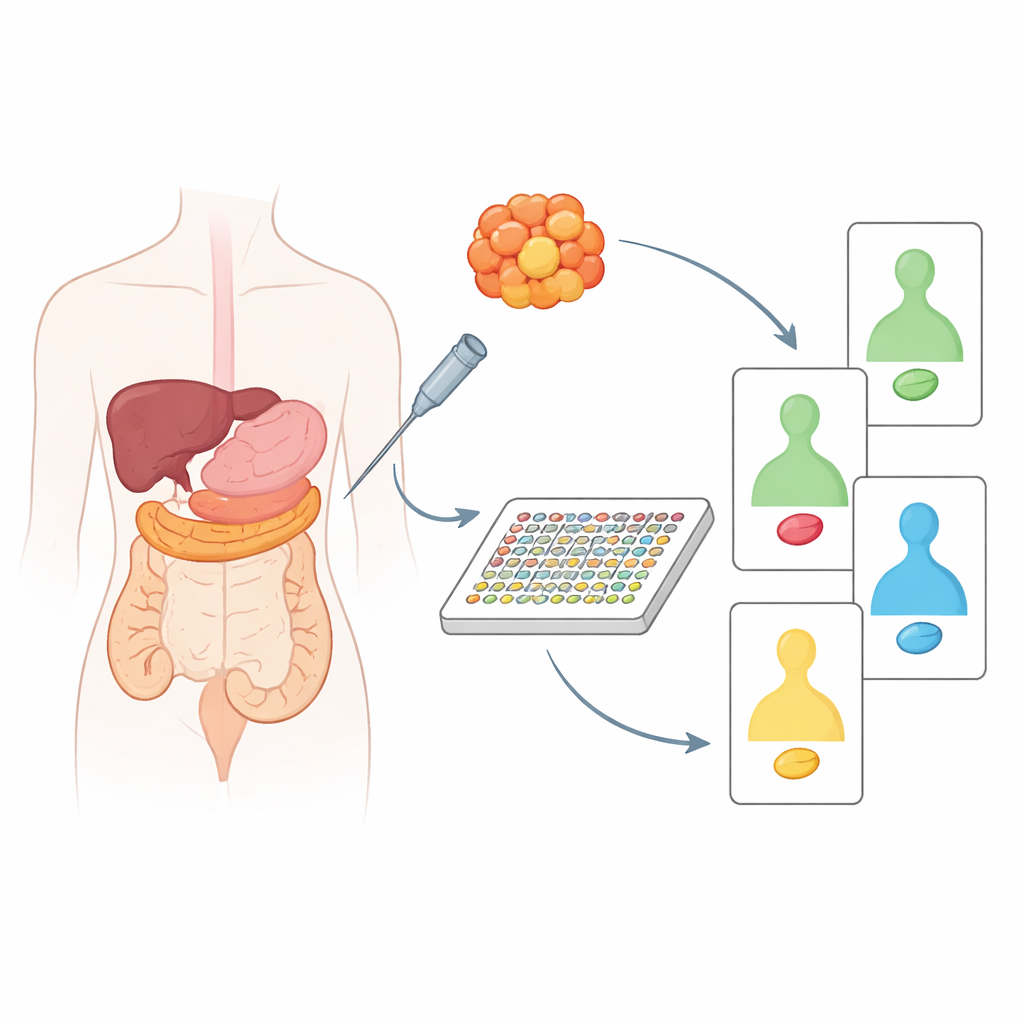
השוואת רקמת הגידול לשכנתה התקינה
הצוות ניתח תחילה רקמות מאוחסנות של 20 מטופלים עם סרטן הלבלב או המעי הגס, תמיד בזוגות לצד רקמה סמוכה שאינה סרטנית מאותו אדם. על‑ידי השוואת הגידולים אל המקבילים התקינים שלהם, יכלו החוקרים לזהות אילו חלבונים השתנו באמת בעקבות הסרטן ולא רק משקפים הבדלים נורמליים בין איברים. התגלה ניגוד ברור בהתנהגותם של שומרי ומניעי סרטן ידועים, כגון p53, Ras, PTEN ואחרים. למשל, גידולי לבלב נטו להראות חיזוק איתותים המקדמי‑צמיחה ואובדן חלבונים מגן, בעוד שלגידולי המעי הגס היה דפוס שונה של מסלולים מופרעים. כאשר קיבצו החוקרים את הדגימות על בסיס שינויים אלה בחלבונים, יכלו לחלק את סרטןי הלבלב לשתי קבוצות ביולוגיות נבדלות ולגלות הבדלים מהותיים בין גידולי המעי הגס הקשורים לגיל המטופל ומיקומו במעי.
"ברקודים" אישיים של פעילות איתות בגידול
מעבר לממוצעים קבוצתיים, הבנו החוקרים פרופיל חלבונים מפורט לכל גידול. פרופילים אלה הדגישו אילו מסלולי איתות — כגון מעגלי mTOR, MAPK/Erk, Wnt או גורמים הקשורים למערכת החיסון — היו פעילים במיוחד או כבויים. רבים מהחלבונים הנמדדים הם מטרות ישירות של תרופות קיימות, או נמצאים ממש מתחת למטרות אלה, מה שאיפשר לצוות להסיק אילו תרופות עשויות להפריע למנועי הצמיחה העיקריים של הגידול. בשלושה רבעים מהמקרים הרטרוספקטיביים הם זיהו מסלול או יותר שסביר שהיה דוחף את התקדמות הגידול. הם גם בלטו גידולים עשירים בסמנים של תאים חיסוניים, שמרמזים על סרטנים "חמים" שעשויים להגיב לאימונותרפיה, ומקרים חריגים עם חתימות ייחודיות בולטות.
יישום השיטה בחולים אמיתיים
כדי לבדוק את השימושיות המעשית שלה בצידו של המיטה, החלו החוקרים להפעיל את DigiWest על ביופסיות מחט טריות מ‑14 מטופלים עם סוגים שונים של סרטן מערכת העיכול שמקרים שלהם נבחנו על‑ידי ועדת גידולים מולקולרית. למטופלים אלה היו היסטוריות מחלה מורכבות ולעתים טיפולים קודמים. מאחר שלא הייתה זמינה רקמה בריאה מתאימה להשוואה, השוו את רמות החלבון של כל גידול לערך החציון בקבוצה כדי להגדיר מה נחשב גבוה או נמוך על־פי תקן. אפילו תחת מסגרת מחמירה זו, ב‑12 מתוך 14 הגידולים נצפו דפוסי פעילות מסלולים ברורים ורלוונטיים לטיפול. בשני דוגמאות מפורטות, נתוני החלבונים איששו הגברה ברמת DNA של גן FGFR2 בסרטן המעי ואובדן של מעצור mTOR בסרטן הכבד, מה שחיזק באופן משמעותי את בחינת הוועדה שתרופות החוסמות FGFR או mTOR יילקחו בחשבון. באופן כללי, ממצאי DigiWest תאמו למניעים גנטיים מרכזיים והציעו מטרות תרופתיות ברוב המקרים שניתנו להערכה.
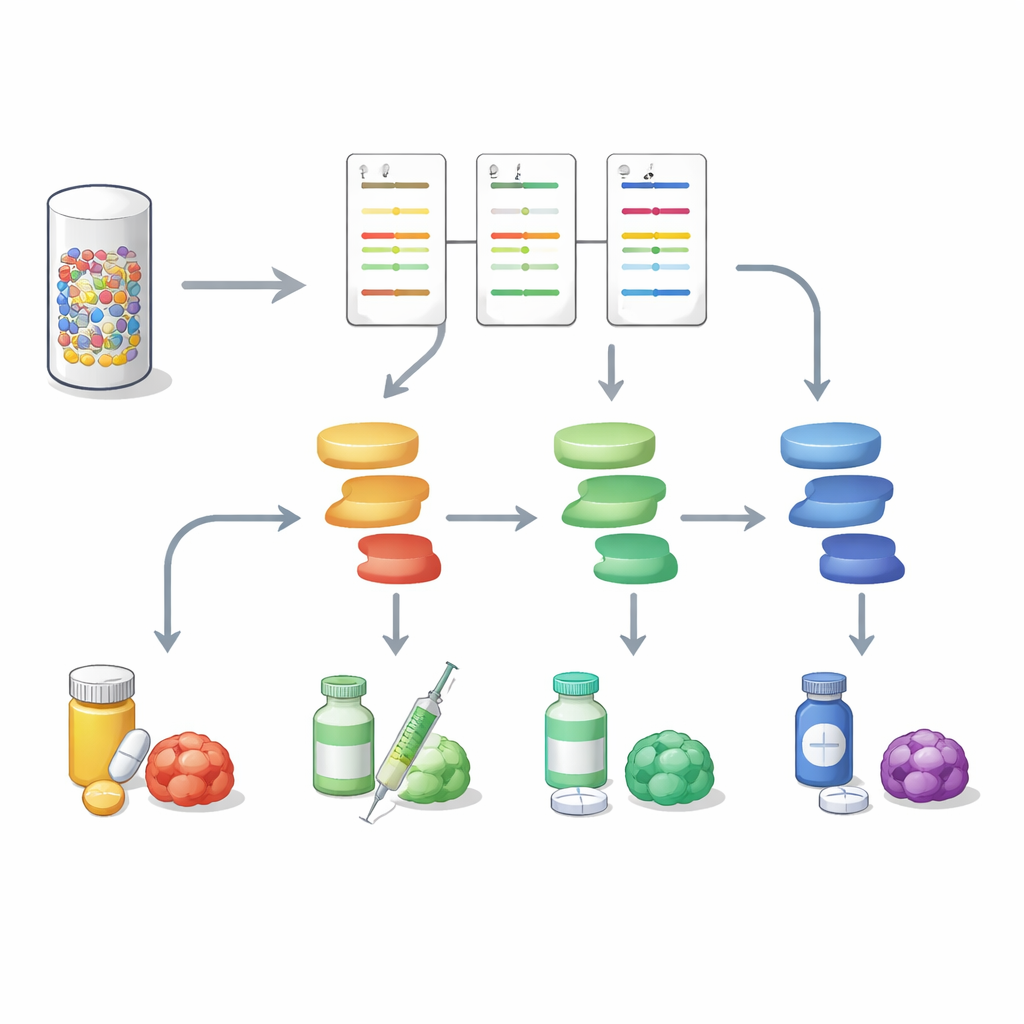
לקראת דיוקן גידול שלם יותר
עבודה זו ממחישה שניתוח איתות חלבוני במקביל לריצוף DNA יכול לספק תמונה עשירה ויותר ישימה של גידולי מערכת העיכול. על‑ידי הפיכת ביופסיה זעירה למפת פעילות רב‑מסלולית, DigiWest מסייע להבחין אילו מתגי מולקולה באמת דלוקים בגידול נתון ואילו תרופות עשויות לפגוע בהם בצורה הטובה ביותר, וייתכן שגם יסמן נתיבי עמידות מתפתחים. למרות שנדרשים מחקרים נרחבים נוספים, הגישה מציעה דרך פרקטית להכניס פרופילינג חלבוני עשיר לתוך האונקולוגיה הפרסונלית היומיומית ולהתקדם לעבר תכניות טיפול המותאמות לגידול החי של כל מטופל, לא רק לתוכנית הגנטית שלו.
ציטוט: Stahl, A., Büringer, K., Missios, P. et al. Personalized signaling pathway analysis of gastrointestinal tumors for patient stratification and drug target evaluation using clinically derived core biopsies. npj Precis. Onc. 10, 124 (2026). https://doi.org/10.1038/s41698-026-01304-5
מילות מפתח: אונקולוגיה מותאמת, סרטן דרכי עיכול, פרוטאומיקה, אפיון ביופסיות, טיפול ממוקד