Clear Sky Science · fr
Apprentissage multimodal multi‑instance pour prédire la performance au test d’effort cardiopulmonaire
Pourquoi cela compte pour les personnes dont le cœur est affaibli
Pour les personnes vivant avec une insuffisance cardiaque, l’une des questions majeures est « Combien de temps me reste‑t‑il, et que peuvent encore faire les médecins pour moi ? ». Le meilleur examen médical pour répondre aujourd’hui à cette question est un test d’effort exigeant sur tapis roulant ou vélo qui mesure la quantité d’oxygène que le corps peut utiliser lors d’un exercice intense. Mais ce test est difficile à organiser et n’est pas disponible dans de nombreux hôpitaux. Cette étude montre comment les médecins pourraient, à la place, utiliser des échographies cardiaques courantes et des informations déjà présentes dans le dossier médical, combinées à l’intelligence artificielle moderne, pour estimer la même valeur cruciale et repérer les patients qui pourraient nécessiter des thérapies avancées potentiellement salvatrices.
Le défi de repérer tôt les situations dangereuses
L’insuffisance cardiaque touche des millions d’Américains et réduit souvent l’espérance de vie de plus d’une décennie. À son stade le plus avancé, la survie peut être pire que pour de nombreux cancers, pourtant seule une petite fraction des patients reçoit à temps des traitements comme la transplantation cardiaque ou les dispositifs mécaniques. Un outil clé pour décider qui doit être orienté vers ces thérapies est le test d’effort cardiopulmonaire, qui mesure le « VO₂ max », la quantité maximale d’oxygène que le corps peut utiliser pendant l’effort. Un VO₂ max faible est un fort signal d’alerte, mais le test exige du matériel spécialisé, du personnel formé et de l’espace, de sorte que de nombreux centres—en particulier les hôpitaux plus petits ou ruraux—ne peuvent pas le proposer. En revanche, les échographies cardiaques standard (échocardiographie transthoracique, ou TTE) et les dossiers médicaux électroniques (DME) sont largement disponibles mais, isolément, n’ont pas été très performants pour prédire quels patients présentent le risque le plus élevé.
Apprendre aux ordinateurs à lire plusieurs examens
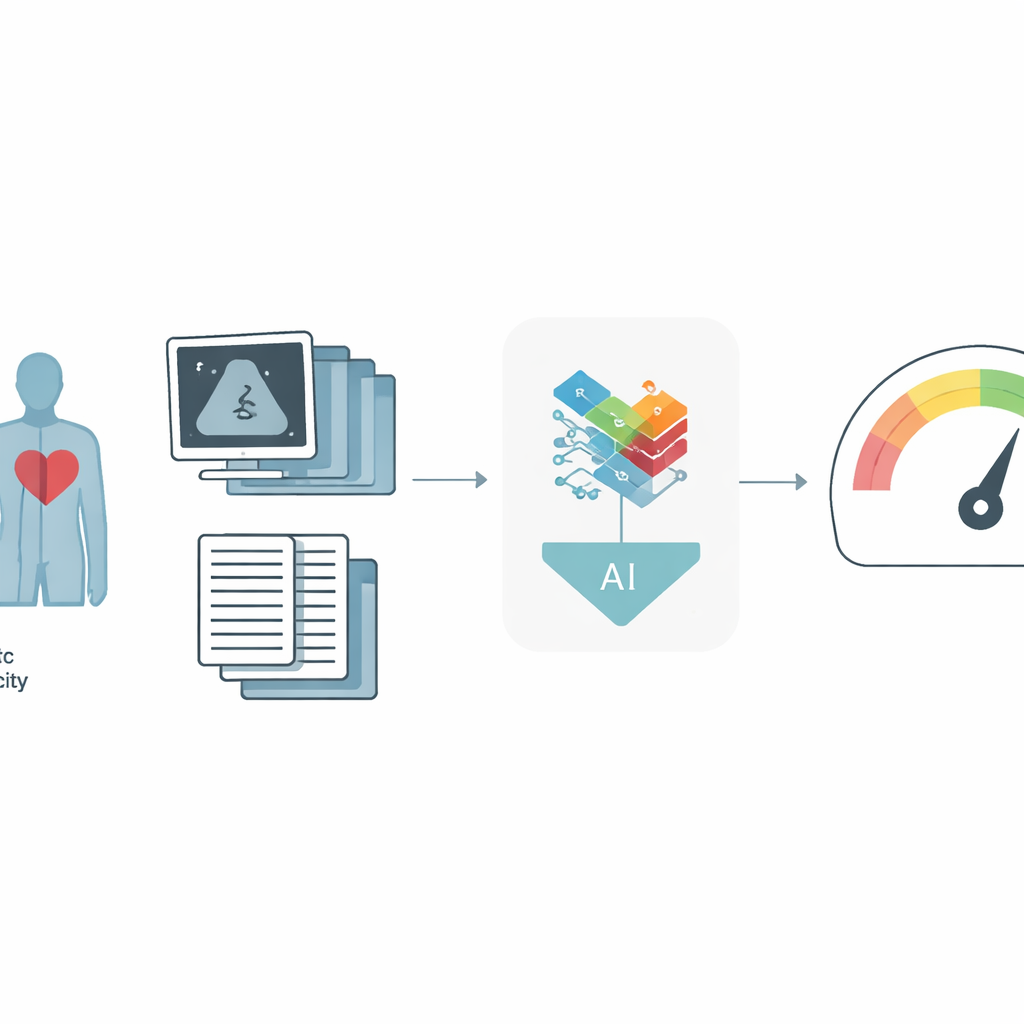
Les chercheurs ont conçu un nouveau système d’intelligence artificielle qui apprend à partir de deux grandes sources d’information : des images échographiques cardiaques animées et des données détaillées du DME, comme l’âge, le poids, les médicaments et les mesures cardiaques standard. Chaque examen échographique contient de nombreux clips et vues spécialisées, donc plutôt que de traiter chaque image séparément, le modèle passe en revue l’ensemble, de manière plus proche de la manière dont travaillerait un clinicien. Il utilise une stratégie « multi‑instance » : d’abord, chaque image ou clip est converti en une description compacte, puis ceux‑ci sont combinés avec un mécanisme d’attention qui permet au modèle de se concentrer sur les parties les plus informatives. En parallèle, un réseau de neurones spécialisé, entraîné sur de nombreux types de données tabulaires médicales, convertit les informations du DME en son propre résumé. Une étape finale de fusion mélange les résumés échographiques et DME en un portrait unique du patient, à partir duquel le système prédit le VO₂ max et si la personne se situe en dessous d’un seuil critique de sécurité.
Performances du système
L’équipe a entraîné et testé son approche sur des données provenant de quatre grands hôpitaux du réseau New York–Presbyterian, en utilisant 1 000 patients pour le développement et 127 patients issus de sites distincts pour la validation externe. Comparé à un modèle d’IA antérieur et plus simple qui considérait les données échographiques et du DME de façon plus indépendante, le nouveau cadre s’est montré sensiblement plus précis. Il expliquait environ 60 % de la variation du VO₂ max dans le groupe de test principal, contre environ 53 % auparavant, et son erreur typique a diminué d’environ un demi‑équivalent métabolique, une amélioration cliniquement significative. Lorsque l’objectif était simplement d’identifier les patients à haut risque—ceux dont la capacité d’effort est particulièrement faible—le système a atteint une aire sous la courbe (AUC) de 0,85 dans le groupe de développement et de 0,87 dans les hôpitaux externes, surpassant tous les modèles qui n’utilisaient que l’échographie ou que les données du DME. En termes pratiques, pour un compromis fixe et cliniquement raisonnable entre cas manqués et fausses alertes, un plus grand nombre de patients réellement à haut risque ont été correctement signalés.
Regarder à l’intérieur de la boîte noire
Pour vérifier que le modèle se focalisait sur des caractéristiques sensées, les auteurs ont créé des cartes visuelles sur les images échographiques montrant quelles régions influençaient le plus les prédictions. Les cartes avaient tendance à mettre en évidence les cavités cardiaques, leurs mouvements et les formes d’onde du flux sanguin—des caractéristiques sur lesquelles les cardiologues s’appuient déjà—suggérant que le système apprend des motifs signifiants plutôt que du bruit. Dans les données du DME, des mesures comme l’âge, l’indice de masse corporelle et la force de contraction du ventricule gauche se sont révélées particulièrement importantes, ce qui correspond là encore aux attentes cliniques. Les chercheurs ont également examiné les performances du modèle dans différents sous‑groupes. La performance était similaire chez les hommes et les femmes et entre patients blancs et non‑blancs pour la prédiction de la valeur exacte du VO₂ max, bien que des écarts soient apparus chez les personnes âgées et dans la classification des haut‑risques selon les races, soulignant la nécessité de données plus diversifiées et d’un affinage axé sur l’équité.
De la recherche à la prise en charge clinique
Parce que le système utilise des informations déjà collectées dans les soins de routine—échocardiogrammes standards et données DME existantes—il pourrait, en principe, être intégré directement aux logiciels hospitaliers. Après la lecture d’un examen, l’IA pourrait estimer discrètement le VO₂ max et signaler les patients dont la capacité d’effort prédite est dangereusement faible, incitant les médecins à ordonner un test d’effort formel ou à les orienter vers des spécialistes de l’insuffisance cardiaque avancée. Les résultats de l’étude, y compris la bonne performance dans des hôpitaux non utilisés pour l’entraînement, suggèrent qu’un tel outil pourrait aider à détecter davantage de patients en détresse qui, autrement, seraient négligés. Bien que des essais prospectifs et des tests plus larges soient encore nécessaires, ce travail indique un avenir où des examens puissants mais rares seraient complétés par des systèmes d’IA utilisant de manière plus intelligente les données dont la plupart des hôpitaux disposent déjà.
Citation: Huang, Z., Pan, W., Alishetti, S. et al. Multimodal multi-instance learning for cardiopulmonary exercise testing performance prediction. npj Digit. Med. 9, 304 (2026). https://doi.org/10.1038/s41746-026-02493-w
Mots-clés: insuffisance cardiaque, test d’effort cardiopulmonaire, échocardiographie, intelligence artificielle, prévision du risque