Clear Sky Science · fr
xGNN4MI : explicabilité des réseaux de neurones graphiques en électrocardiographie 12 dérivations pour la classification des maladies cardiovasculaires
Pourquoi cela compte pour la santé cardiaque
Les infarctus et autres maladies cardiaques restent des causes majeures de mortalité dans le monde, et le test standard pour repérer les problèmes est la ligne ondulée familière de l’électrocardiogramme, ou ECG. Les médecins se tournent de plus en plus vers l’intelligence artificielle pour aider à lire ces signaux, mais de nombreux outils d’IA fonctionnent comme des boîtes noires opaques, donnant un verdict sans montrer leur raisonnement. Cette étude présente une nouvelle approche nommée xGNN4MI qui vise à conserver la puissance de l’IA moderne tout en rendant son raisonnement visible et vérifiable pour les cliniciens.
Des battements cardiaques aux signaux connectés
Un ECG ne provient pas d’un seul point de vue : douze dérivations placées sur le thorax et les membres offrent des perspectives légèrement différentes de l’activité électrique du cœur. Chacune est sensible à une région différente du muscle cardiaque et de son irrigation sanguine. Les auteurs transforment cet enregistrement multi‑dérivations en réseau, où chaque nœud représente une dérivation et les connexions capturent la façon dont ces signaux se rapportent les uns aux autres au fil du temps. En découpant l’ECG de dix secondes en courtes tranches et en reliant la même dérivation à travers les tranches, ils construisent une structure qui reflète à la fois la position des électrodes sur le corps et le déroulement du battement de cœur pas à pas. Ce réseau devient l’entrée d’un réseau de neurones graphiques, un type d’IA conçu pour fonctionner sur des toiles de données connectées plutôt que sur des grilles ou listes simples. 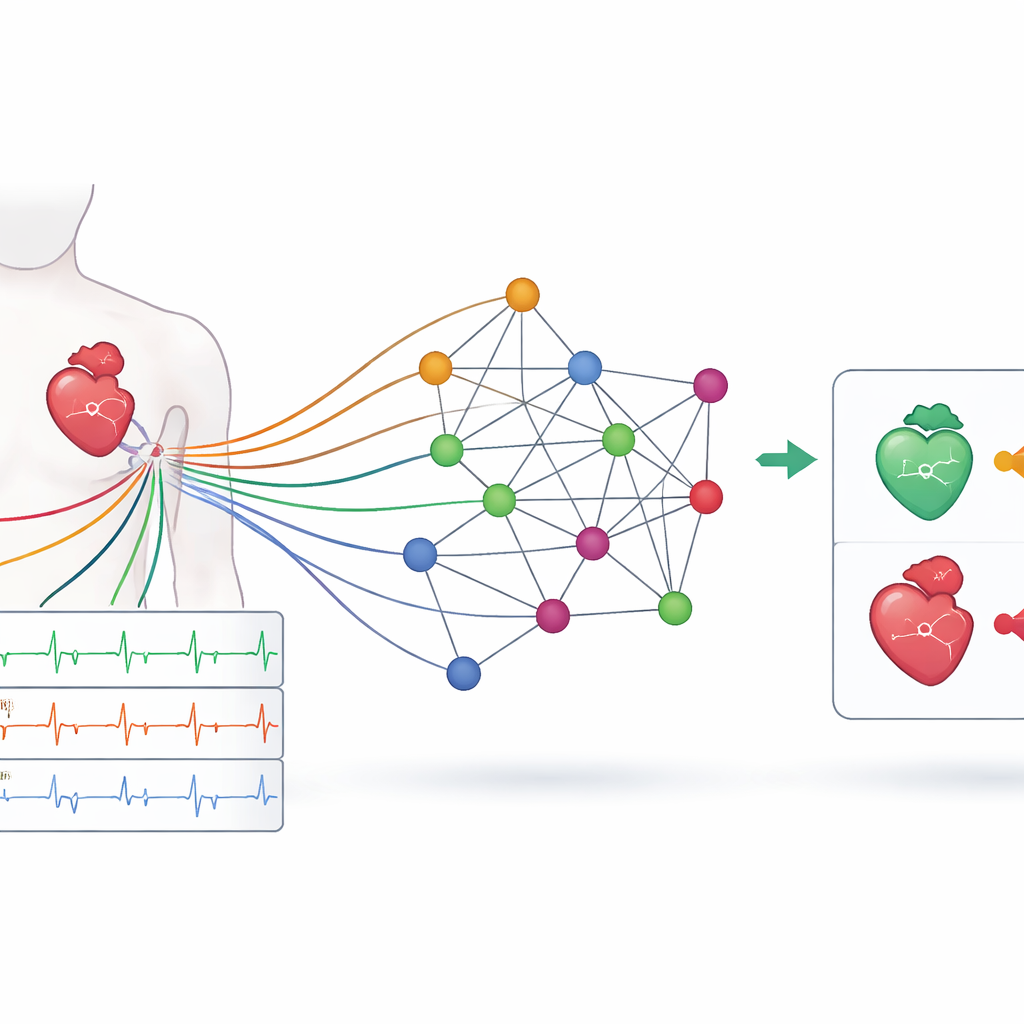
Un nouveau pipeline pour lire et localiser les infarctus
En utilisant cette vue en réseau de l’ECG, l’équipe a conçu une chaîne logicielle open source qu’elle appelle xGNN4MI. Elle prend en charge l’ensemble du parcours depuis le signal brut jusqu’au diagnostic : construction du graphe ECG, entraînement du réseau de neurones graphique, puis explication de la manière dont le modèle produit ses prédictions. Ils ont testé le système sur deux tâches exigeantes. D’abord, il devait classer les ECG en cinq grands groupes diagnostiques, tels que rythme normal, infarctus, ou troubles de conduction. Ensuite, il devait aller plus loin et identifier où dans le cœur un infarctus s’était produit, en distinguant notamment une lésion de la paroi antérieure (antéroséptale) d’une lésion de la paroi inférieure (inférieure) du muscle cardiaque. Le modèle a été entraîné sur une grande collection publique d’ECG puis évalué sur une étude populationnelle distincte pour mesurer sa capacité à se généraliser à de nouveaux patients.
Performance du système
Sur la tâche de classification large, le modèle a atteint une précision d’environ sept ECG sur dix, avec des performances particulièrement solides pour reconnaître les enregistrements normaux et les infarctus nets. Certaines catégories plus hétérogènes, comme l’épaississement du muscle cardiaque ou les perturbations de conduction, étaient plus difficiles à séparer clairement, probablement parce qu’elles recouvrent plusieurs problèmes sous‑jacents différents. Pour la tâche plus fine de localisation de l’infarctus, la performance s’est améliorée : le système distinguait correctement les principaux sous‑types d’infarctus avec un score F1 pondéré proche de 0,8 sur le jeu de données principal et montrait une bonne capacité de généralisation à la cohorte externe. Il reconnaissait de manière particulièrement fiable les patrons classiques inférieurs et antéroséptaux. En revanche, il éprouvait davantage de difficultés à identifier de véritables cœurs sains dans l’étude externe, signe que des différences subtiles entre jeux de données — comme des durées de QRS légèrement plus longues, une mesure du temps d’activation d’un battement — peuvent perturber même des modèles bien entraînés. 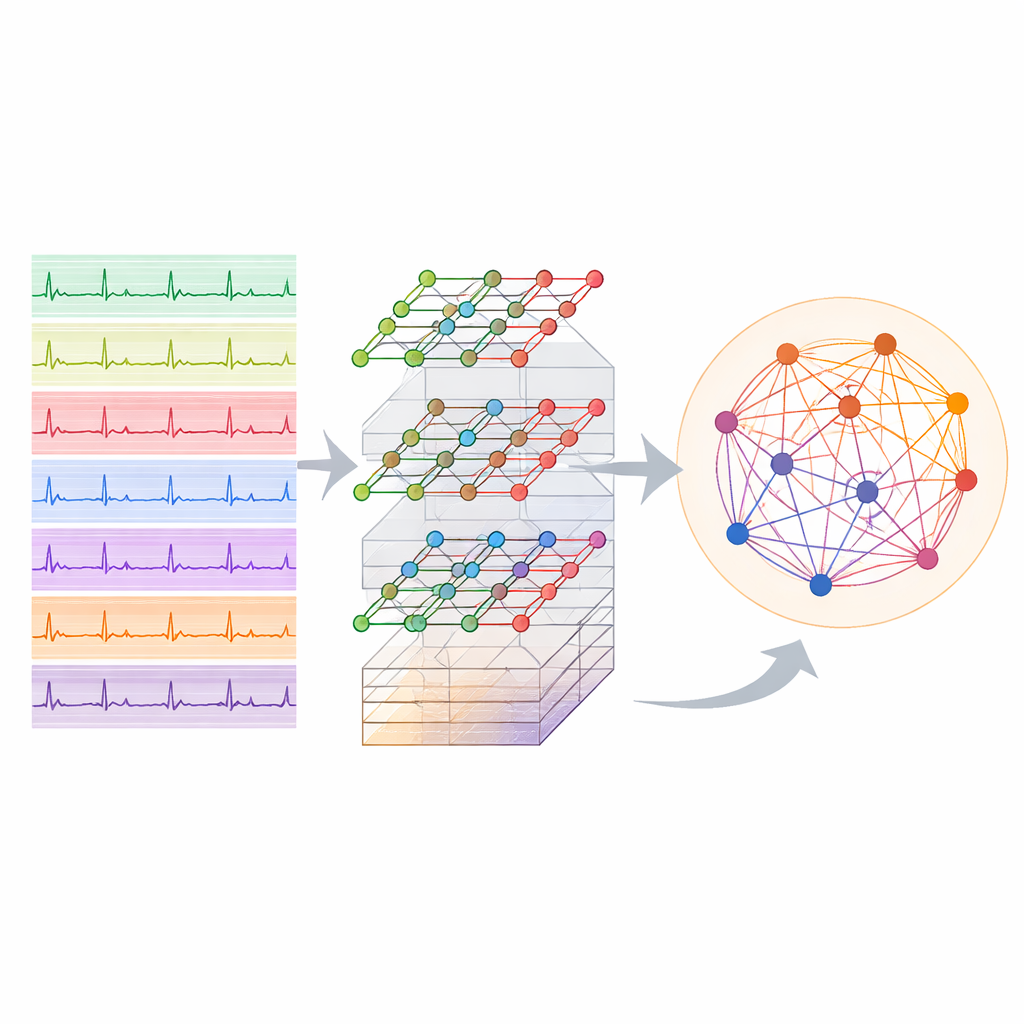
Voir ce que l’IA « regarde »
Une promesse centrale de xGNN4MI est qu’il ne se contente pas de fournir une réponse, mais montre aussi quelles parties du graphe ECG ont le plus compté. Les auteurs ont utilisé une méthode appelée GNNExplainer pour mettre en évidence les dérivations et connexions les plus influentes pour chaque prédiction. Quand le modèle a étiqueté un ECG comme un infarctus antéroséptal, les nœuds les plus importants étaient les dérivations thoraciques V1 à V3, ce qui correspond à l’enseignement classique selon lequel ces dérivations surveillent la paroi antérieure du cœur. Pour les infarctus inférieurs, le modèle s’est focalisé sur les dérivations II, III et aVF, reproduisant encore une fois les critères traditionnels. Fait intéressant, une dérivation des membres (aVR), souvent négligée en lecture routinière, est apparue comme inhabituellement importante dans certains cas inférieurs, faisant écho à des rapports cliniques plus récents liant des modifications dans cette dérivation à des complications plus sévères. Les ECG normaux, en revanche, montraient une répartition plus homogène de l’importance entre les dérivations, cohérente avec l’absence d’une région endommagée unique.
Limites et voies futures
Si les explications concordaient bien avec les connaissances cardiologiques établies, elles ont aussi mis en évidence des limites actuelles. La méthode d’explicabilité tend à se concentrer sur des grappes de dérivations connectées et ne capture pas complètement les relations à distance ni le détail temporel fin, alors que ceux‑ci peuvent être pertinents cliniquement. Le modèle fonctionne aussi avec des étiquettes dominantes uniques et ne reflète pas encore le mélange de conditions souvent présent chez les patients réels. Les auteurs suggèrent que des travaux futurs pourraient utiliser des outils d’explication plus avancés mieux adaptés au temps, intégrer des diagnostics multi‑étiquettes et adapter la structure du graphe à des maladies cardiaques spécifiques. Néanmoins, en partageant ouvertement le code, en documentant chaque choix de conception et en montrant que leur modèle se concentre sur des régions ECG cliniquement sensées, xGNN4MI offre une étape concrète vers des outils d’IA que les médecins peuvent à la fois utiliser et vérifier.
Ce que cela signifie pour les patients et les cliniciens
En termes simples, ce travail montre qu’il est possible de construire un assistant IA pour l’interprétation des ECG qui non seulement repère les infarctus et suggère leur localisation, mais indique aussi les mêmes dérivations sur lesquelles les experts humains s’appuient. Bien qu’il ne soit pas encore prêt à remplacer un cardiologue, le cadre démontre que des IA puissantes basées sur les graphes peuvent être rendues plus transparentes et confrontées aux connaissances médicales. Si elles sont affinées et validées, de tels outils pourraient aider des cliniciens moins expérimentés dans des environnements chargés ou à ressources limitées, en signalant rapidement les infarctus à haut risque tout en fournissant une trace visuelle du cheminement de la décision.
Citation: Maurer, M.C., Hempel, P., Steinhaus, K.E. et al. xGNN4MI: explainability of graph neural networks in 12-lead electrocardiography for cardiovascular disease classification. npj Digit. Med. 9, 256 (2026). https://doi.org/10.1038/s41746-026-02367-1
Mots-clés: IA électrocardiogramme, réseaux de neurones graphiques, infarctus du myocarde, intelligence artificielle explicable, diagnostic cardiovasculaire