Clear Sky Science · fr
Analyse personnalisée des voies de signalisation des tumeurs gastro-intestinales pour la stratification des patients et l’évaluation des cibles médicamenteuses à partir de biopsies centrales cliniquement obtenues
Pourquoi cette recherche compte pour les patients
Les oncologues cherchent de plus en plus à adapter les traitements à la biologie propre à chaque tumeur. Pour les cancers du système digestif — comme ceux du pancréas, du côlon, du foie ou des voies biliaires — cet objectif est particulièrement urgent, car ils sont fréquents, souvent diagnostiqués tard et difficiles à traiter. Cette étude explore une nouvelle méthode de laboratoire capable de lire l’activité de nombreux protéines liées au cancer à partir de prélèvements minimes, dans le but d’aider les médecins à choisir des thérapies plus précises pour chaque patient.
Des listes d’ADN aux signaux vivants
Aujourd’hui, la plupart des prises en charge « personnalisées » du cancer reposent sur l’analyse des altérations de l’ADN tumoral. Bien que puissante, l’ADN seul n’indique pas quels signaux intracellulaires sont effectivement activés et conduisent la croissance. Ces signaux sont portés par des protéines, dont beaucoup peuvent être ciblées directement par des médicaments. Les chercheurs ont utilisé une technique à haut débit appelée DigiWest, une version moderne du Western blot classique, pour mesurer environ 130 à 200 protéines et leurs formes activées simultanément. Fait important, cette méthode nécessite seulement la quantité de matériel d’une biopsie à l’aiguille, ce qui la rend adaptée à un usage clinique réel.
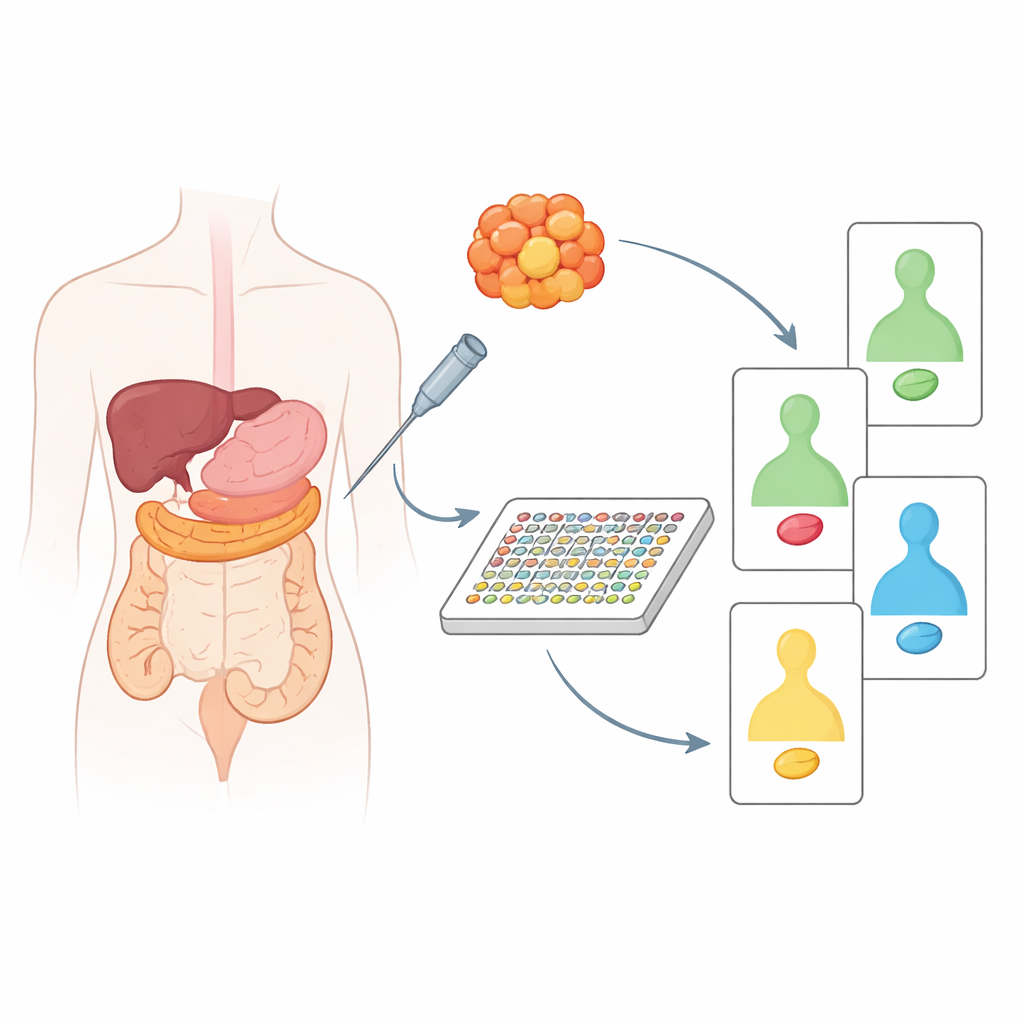
Comparer le tissu tumoral à son voisin sain
L’équipe a d’abord analysé des échantillons conservés de 20 patients atteints de cancer pancréatique ou colorectal, toujours appariés avec un tissu non cancéreux adjacent provenant de la même personne. En comparant les tumeurs à leurs homologues sains, ils ont pu identifier les protéines véritablement altérées par le cancer plutôt que reflétant de simples différences normales entre organes. Cela a révélé des contrastes nets dans le comportement de gardiens et d’activateurs tumoraux bien connus, tels que p53, Ras, PTEN et d’autres. Les tumeurs pancréatiques, par exemple, montraient une tendance à l’activation accrue des signaux promoteurs de croissance et à la perte de protéines protectrices, tandis que les tumeurs coliques présentaient leur propre profil distinct de voies perturbées. Lorsqu’ils ont regroupé les échantillons selon ces changements protéiques, ils ont pu diviser les cancers du pancréas en deux groupes biologiquement différents et détecter des différences significatives parmi les cancers du côlon liées à l’âge des patients et à la localisation tumorale dans l’intestin.
“Codes-barres” individuels d’activité de signalisation
Au-delà des moyennes de groupe, les scientifiques ont construit un profil protéique détaillé pour chaque tumeur. Ces profils ont mis en évidence quelles voies de signalisation — par exemple celles impliquant mTOR, MAPK/Erk, Wnt ou des facteurs liés à l’immunité — étaient particulièrement actives ou inhibées. De nombreuses protéines mesurées sont des cibles directes de médicaments existants, ou se situent juste en aval de telles cibles, permettant à l’équipe de déduire quels médicaments pourraient perturber les principaux moteurs de croissance d’une tumeur. Dans les trois quarts des cas rétrospectifs, ils ont pu identifier une ou plusieurs voies vraisemblablement responsables de la progression tumorale. Ils ont également repéré des tumeurs riches en marqueurs de cellules immunitaires, suggérant des cancers « chauds » susceptibles de répondre à l’immunothérapie, ainsi que des cas atypiques présentant des signatures particulièrement uniques.
Mettre la méthode en pratique chez de vrais patients
Pour tester son utilité au chevet, les chercheurs ont ensuite appliqué DigiWest à des biopsies à l’aiguille fraîches de 14 patients atteints de divers cancers gastro-intestinaux dont les dossiers étaient examinés par un Comité moléculaire des tumeurs. Ces patients avaient des histoires de maladie complexes et souvent des traitements antérieurs. Faute de tissu sain apparié, les niveaux protéiques de chaque tumeur ont été comparés à la médiane du groupe pour définir ce qui devait être considéré comme anormalement élevé ou bas. Même avec ce cadre plus strict, 12 des 14 tumeurs ont montré des profils d’activité des voies clairs et pertinents pour le traitement. Dans deux exemples détaillés, les données protéiques ont confirmé une amplification au niveau de l’ADN du gène FGFR2 dans un cancer du côlon et la perte d’un frein mTOR dans un cancer du foie, soutenant fortement l’examen par le Comité de l’utilisation d’inhibiteurs de FGFR ou de mTOR. Globalement, les résultats DigiWest concordaient avec des altérations génétiques clés et suggéraient des cibles médicamenteuses dans la plupart des cas évaluables.
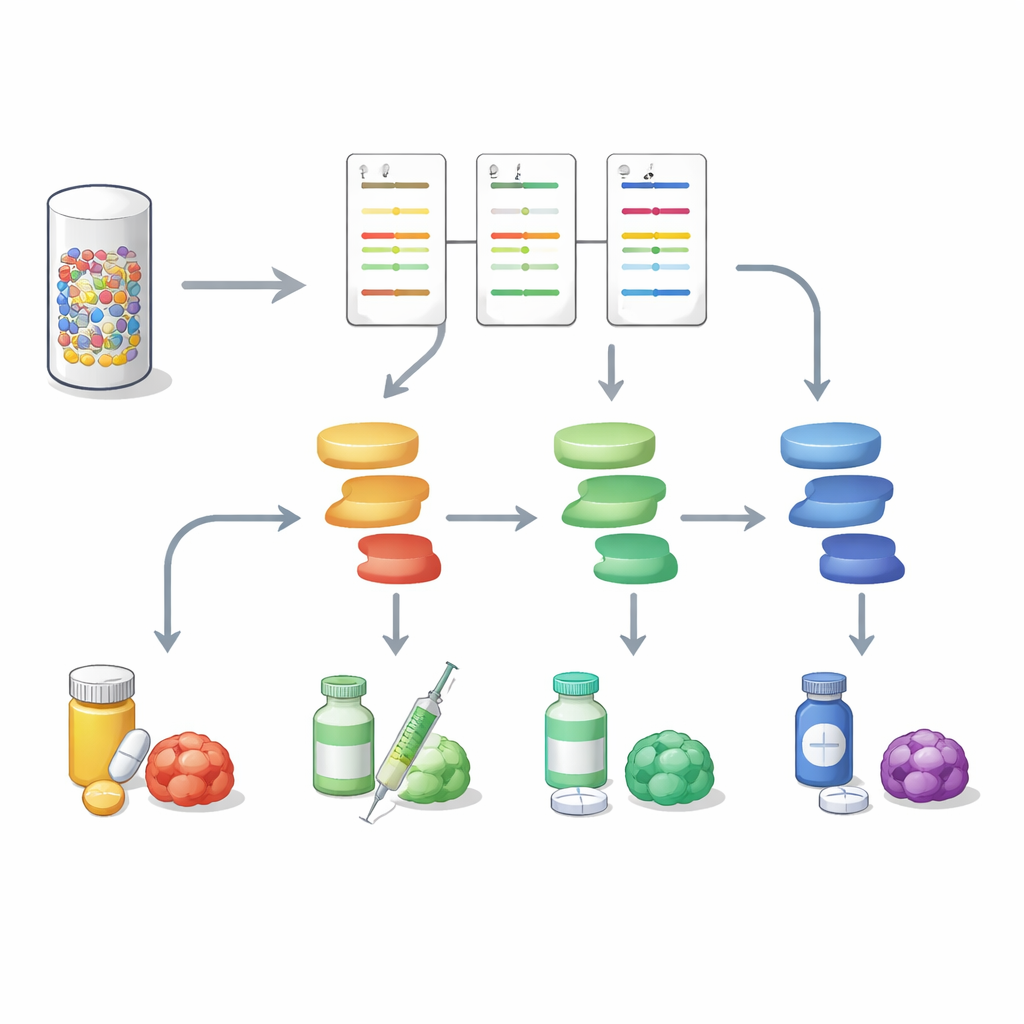
Vers des portraits tumoraux plus complets
Ce travail montre que l’analyse de la signalisation protéique en parallèle du séquençage de l’ADN peut fournir une image plus riche et plus exploitable des tumeurs gastro-intestinales. En transformant une biopsie minime en une carte d’activité multi‑voies, DigiWest aide à distinguer quels interrupteurs moléculaires sont réellement activés dans un cancer donné et quels traitements sont les mieux placés pour les cibler, et peut aussi signaler des routes émergentes de résistance. Bien que des études de plus grande ampleur soient encore nécessaires, l’approche offre une manière pratique d’introduire le profilage protéique haute‑contenu dans l’oncologie de précision quotidienne et de se rapprocher de plans de traitement adaptés à la tumeur vivante de chaque patient, et pas seulement à son plan génétique.
Citation: Stahl, A., Büringer, K., Missios, P. et al. Personalized signaling pathway analysis of gastrointestinal tumors for patient stratification and drug target evaluation using clinically derived core biopsies. npj Precis. Onc. 10, 124 (2026). https://doi.org/10.1038/s41698-026-01304-5
Mots-clés: oncologie de précision, cancer gastro-intestinal, protéomique, profilage de biopsie, thérapie ciblée