Clear Sky Science · fr
Atténuation écologique de la corrosion du cuivre lors du décapage acide en dessalement grâce à un extrait végétal
Pourquoi il est important de protéger le cuivre
L’eau douce issue de la mer repose sur de vastes usines de dessalement équipées de tuyaux en cuivre qui transmettent la chaleur rapidement et efficacement. Pour maintenir ces systèmes, les exploitants nettoient périodiquement les tuyaux avec des acides concentrés pour dissoudre les dépôts minéraux. Or, ces mêmes acides peuvent attaquer le cuivre lui‑même, réduire la durée de vie des équipements et risquer la contamination de l’approvisionnement en eau. Cette étude examine si un extrait naturel de l’Acacia farnesiana peut agir comme une protection douce et écologique pour le cuivre pendant ces étapes de nettoyage agressives.
Des nettoyages courants aux coûts cachés
Dans une usine de dessalement, les tubes en cuivre baignent dans une eau chaude et salée et accumulent progressivement des dépôts minéraux crustacés, comme le carbonate de calcium. Pour éliminer ces dépôts, les techniciens font circuler de l’acide chlorhydrique dans les conduites. Efficace pour le nettoyage, cet acide arrache aussi des atomes de cuivre de la surface métallique, en particulier en présence d’ions chlorure provenant de l’eau de mer, ce qui provoque piqûres et parois de tuyau rugueuses et fragilisées. Les additifs chimiques classiques peuvent ralentir ce dommage, mais beaucoup sont synthétiques, toxiques ou persistants dans l’environnement. Trouver une alternative d’origine végétale pouvant être rejetée sans nuire aux personnes ou à la vie marine constituerait une avancée majeure vers des traitements d’eau plus verts.

Un bouclier d’origine végétale pour le métal
Les chercheurs se sont concentrés sur un extrait commercial d’Acacia farnesiana, un arbrisseau connu sous le nom d’acacia doux. L’extrait, dissous dans l’eau et dans l’acide, contient un mélange d’acides gras naturels. Lorsqu’ils ont ajouté de petites quantités de cet extrait à une solution d’acide chlorhydrique 1 molaire — du type utilisé pour le nettoyage — ils ont mesuré la perte de masse des échantillons de cuivre, la facilité de passage du courant électrique à l’interface métal‑acide, et les courants de corrosion. Avec les trois méthodes, l’extrait a réduit la corrosion de plus de 94 % à la concentration maximale testée, avec une performance atteignant environ 97 %. Ces résultats signifient que dans des conditions de nettoyage typiques, seule une infime fraction de la perte de cuivre habituelle se produirait en présence de l’extrait végétal.
Comment le revêtement naturel se forme
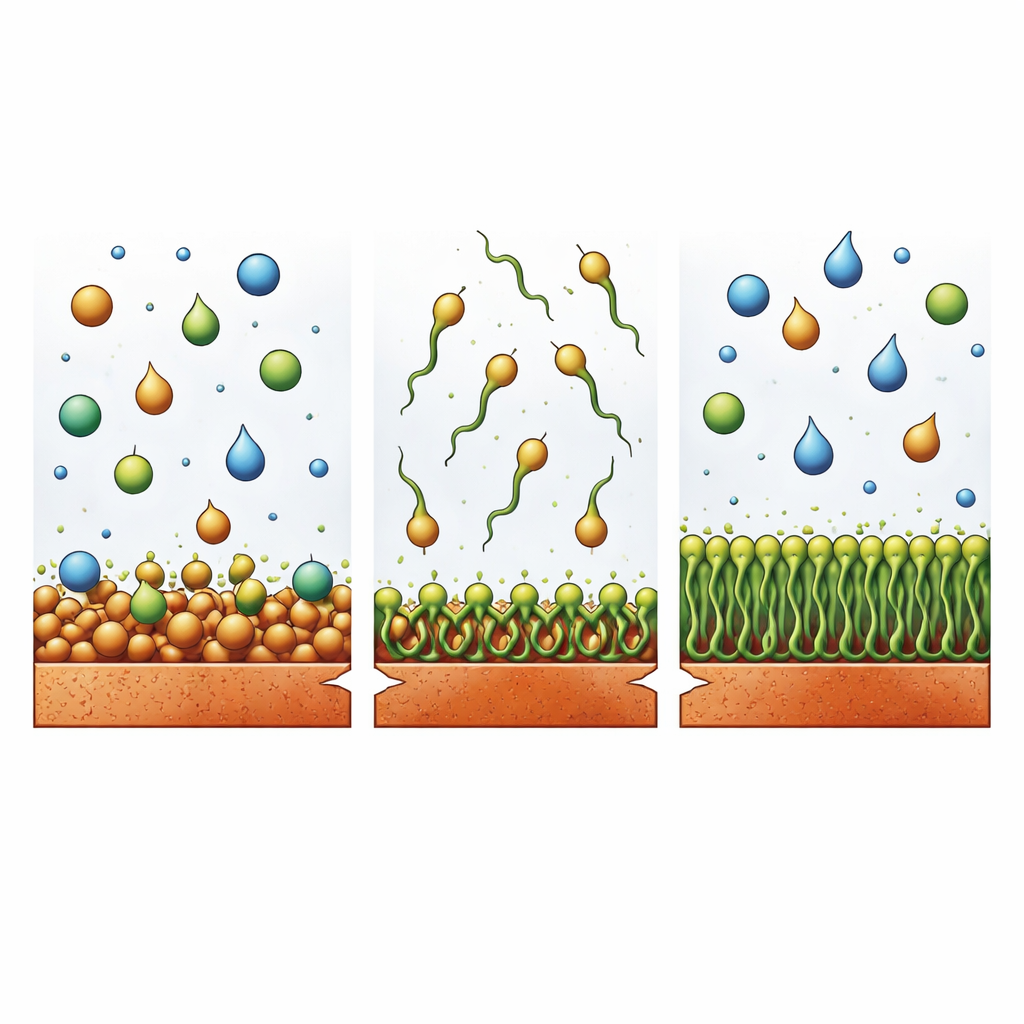
Pour comprendre pourquoi l’extrait fonctionne si bien, l’équipe a analysé ses composants et observé leur comportement à la surface du métal. La chromatographie liquide haute performance a révélé que deux acides gras insaturés à longue chaîne, l’acide linoléique et l’acide oléique, dominent le mélange. Chaque molécule possède un groupe « tête » réactif qui peut s’accrocher au cuivre et une longue « queue » huileuse qui n’aime pas l’eau. Les images microscopiques ont montré que, sans l’extrait, les surfaces de cuivre en milieu acide deviennent rugueuses et couvertes de cristaux chlorure corrosifs, tandis qu’avec l’extrait elles apparaissent lisses et intactes. La spectroscopie a confirmé que les acides gras se lient effectivement au cuivre, modifiant leur signature chimique lors de la liaison. Ensemble, ces indices indiquent que les molécules s’ancrent d’abord au cuivre via leurs groupes têtes et des liaisons riches en électrons, puis s’alignent côte à côte pour que leurs queues forment un film compact et hydrophobe qui empêche l’acide et les chlorures d’atteindre le métal.
Protection stable dans des conditions réelles
L’équipe a également testé la robustesse de ce film naturel au fil du temps et à différentes températures, reflétant les exigences du nettoyage industriel. Sur trois heures — la durée typique d’un lavage acide — l’effet protecteur est resté très élevé. Même après 72 heures d’exposition, l’efficacité est restée supérieure à 90 %, suggérant une marge de sécurité confortable en cas de retards imprévus. À des températures plus élevées, la corrosion augmentait quelque peu et la protection diminuait légèrement, ce qui correspond à un modèle où certaines molécules sont physiquement adsorbées et peuvent se désorber lorsque le système se réchauffe. Néanmoins, le film est resté suffisamment efficace pour être pratique lors d’opérations de nettoyage à chaud. Des calculs informatiques ont appuyé cette double action, montrant que les acides gras clés sont bien adaptés pour donner des électrons au cuivre et construire une barrière mixte, physique et chimique.
De l’eau plus propre grâce à une chimie plus verte
En termes simples, cette étude montre qu’un liquide dérivé d’Acacia farnesiana peut envelopper le cuivre d’un manteau auto‑assemblé, semblable à de l’huile, qui tient l’essentiel de l’acide à distance. En réduisant la perte de cuivre de plus de 95 %, l’extrait pourrait prolonger la durée de vie des échangeurs de chaleur coûteux, diminuer les coûts de maintenance et réduire le risque de contamination métallique de l’eau dessalée. Comme les molécules actives sont des acides gras naturels — proches des composants des huiles végétales — elles sont beaucoup moins susceptibles que les inhibiteurs traditionnels de présenter des risques environnementaux ou sanitaires à long terme. Alors que le dessalement devient de plus en plus crucial pour approvisionner en eau douce des populations croissantes, ces protecteurs de corrosion d’origine végétale offrent une voie prometteuse pour rendre le processus à la fois fiable et respectueux de l’environnement.
Citation: Thabet, H.K., Alshammari, O.A.O., Ashmawy, A.M. et al. Eco-friendly corrosion mitigation for copper in desalination acid cleaning using plant extract. Sci Rep 16, 9845 (2026). https://doi.org/10.1038/s41598-026-44764-2
Mots-clés: dessalement, corrosion du cuivre, inhibiteurs écologiques, extraits végétaux, décapage acide