Clear Sky Science · fr
Étude moléculaire du dysbiose de l’intestin grêle liée à l’anémie ferriprive
Pourquoi l’intestin est important dans le sang pauvre en fer
L’anémie ferriprive est surtout connue pour provoquer fatigue et faiblesse, mais cette étude montre que le problème peut débuter bien plus tôt dans le tube digestif que ce que la plupart imaginent. Les chercheurs ont examiné de près l’intestin grêle — la principale porte d’entrée des nutriments — pour voir comment un manque de fer modifie la communauté microbienne qui y vit. Leurs résultats suggèrent que la carence en fer elle‑même peut préparer le terrain à une forme de prolifération microbienne qui, à son tour, rend encore plus difficile l’absorption du fer par l’organisme, créant un cercle vicieux.
Un problème sanguin courant aux racines cachées
L’anémie ferriprive touche environ une personne sur trois dans le monde, en particulier les enfants, les femmes et les personnes âgées. Les médecins savent que le microbiome intestinal — les milliards de microbes qui peuplent notre système digestif — peut influencer l’efficacité de l’absorption du fer, et que certains patients présentant une prolifération bactérienne de l’intestin grêle ont des difficultés à capter ce minéral. Ce qui restait flou, c’est si l’inverse peut aussi se produire : une absence de fer peut‑elle modifier à ce point les microbes de l’intestin grêle qu’ils en viennent à ressembler à ceux observés dans la prolifération bactérienne de l’intestin grêle (SIBO), une affection associée à ballonnements, douleurs et mauvaise absorption des nutriments ?
Tester la réponse de l’intestin à la carence en fer
Pour répondre à cette question, les scientifiques ont utilisé un modèle de rat bien établi d’anémie ferriprive. Un groupe d’animaux a reçu une alimentation standard, tandis qu’un autre a été nourri pendant 40 jours avec une nourriture délibérément dépourvue de fer. Des analyses sanguines ont confirmé que le second groupe développait une anémie nette, avec des taux de globules rouges bas, une hémoglobine réduite et des réserves en fer épuisées. L’équipe a ensuite prélevé des échantillons de trois segments de l’intestin grêle — le duodénum, le jéjunum et l’iléon — et a utilisé des méthodes basées sur l’ADN pour quantifier les bactéries, identifier les types présents et prédire les activités métaboliques de ces microbes.
Quand l’intestin grêle commence à ressembler au côlon
La première observation marquante fut que le nombre total de bactéries augmentait fortement dans tout l’intestin grêle des animaux anémiques, atteignant des niveaux que des travaux antérieurs ont associés à la SIBO. La diversité des espèces microbiennes a également augmenté, en particulier vers l’extrémité distale de l’intestin grêle. Au lieu de la communauté clairsemée et de faible densité qui y vit normalement, les animaux anémiques présentaient un enrichissement en bactéries plus typiques du côlon, telles que Clostridium et Escherichia‑Shigella, ainsi que des groupes fermentaires comme Lactobacillus. Ce schéma était le plus prononcé dans l’iléon, suggérant que des microbes du gros intestin peuvent remonter en amont lorsque le fer se raréfie.
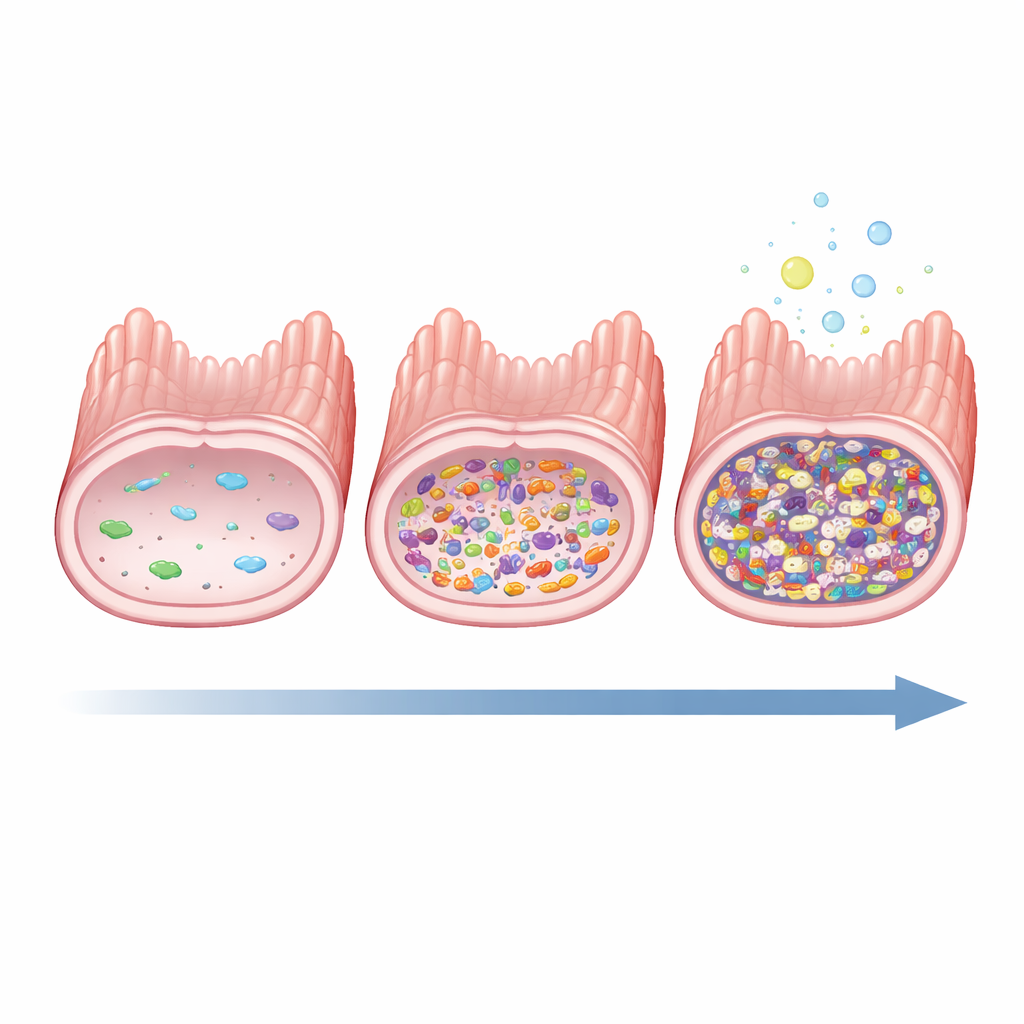
Activités microbiennes qui provoquent gaz et inconfort
Au‑delà de l’identification des espèces, les chercheurs ont cherché à savoir ce que ces microbes faisaient probablement. À l’aide d’outils informatiques, ils ont inféré les voies métaboliques codées dans l’ADN microbien. Dans les trois régions de l’intestin grêle, les animaux anémiques présentaient davantage d’activité dans les voies qui dégradent les sucres et les acides aminés et produisent des gaz et des acides gras à chaîne courte, notamment le propionate et le butyrate, ainsi que de l’hydrogène. Ce sont des signatures classiques d’une prolifération fermentaire et elles sont étroitement liées aux gaz, ballonnements et inconfort abdominal souvent observés dans la SIBO. Les changements fonctionnels correspondaient nettement aux modifications taxonomiques, renforçant l’idée que la carence en fer pousse l’écosystème de l’intestin grêle vers un état proche de la SIBO.
Un cercle vicieux entre microbes et carence en fer
Globalement, l’étude suggère que la carence en fer fait plus que réduire les réserves de fer de l’organisme : elle peut aussi remodeler le paysage microbien de l’intestin grêle de manière à favoriser la prolifération bactérienne et une fermentation excessive. Cela peut, en retour, endommager la muqueuse intestinale et entrer en compétition avec l’hôte pour les nutriments, compliquant la correction de l’anémie. Pour les patients, le message est que des carences en fer persistantes ou récurrentes peuvent parfois refléter non seulement l’alimentation ou des pertes sanguines, mais aussi des déséquilibres microbiaux sous‑jacents dans l’intestin grêle. À l’avenir, des traitements combinant la supplémentation en fer et des stratégies pour prévenir ou corriger les modifications bactériennes de type SIBO pourraient améliorer la récupération et réduire les symptômes digestifs inconfortables.
Citation: Soriano-Lerma, A., Soriano-Suárez, J.S., Garcia-Rodriguez, M. et al. Molecular study of the small intestine dysbiosis derived from iron deficiency anaemia. Sci Rep 16, 14298 (2026). https://doi.org/10.1038/s41598-026-44373-z
Mots-clés: anémie ferriprive, microbiome de l’intestin grêle, prolifération bactérienne, dysbiose intestinale, absorption des nutriments