Clear Sky Science · fr
L’impact de la malbouffe sur la fertilité masculine chez la souris : interventions thérapeutiques ciblant les produits terminaux de glycation avancée et le stress oxydatif
Pourquoi cette étude compte dans la vie de tous les jours
La plupart des gens savent que la malbouffe peut augmenter le tour de taille et faire monter la glycémie, mais peu imaginent qu’elle puisse aussi saper silencieusement la fertilité. Cette étude chez la souris explore comment un régime moderne riche en graisses et fortement transformé nuit à la santé reproductive masculine et teste si deux traitements différents peuvent inverser les effets. Ce travail intéresse non seulement les couples qui cherchent à concevoir, mais aussi toute personne soucieuse de savoir comment l’environnement alimentaire actuel peut affecter la santé des générations futures.
De la restauration rapide à des spermatozoïdes fragiles
Les chercheurs se sont concentrés sur un groupe de molécules problématiques appelées produits terminaux de glycation avancée, ou PTGA (AGEs en anglais). Elles se forment quand des sucres réagissent avec des protéines et des lipides, en particulier lors de cuissons à haute température comme la friture et le grillage. Les aliments industriels et ultra-transformés en sont riches ; ces composés s’accumulent dans l’organisme et favorisent une inflammation de bas grade et une usure chimique. Dans des tissus particulièrement sensibles à l’équilibre chimique — comme les testicules — cela peut être particulièrement délétère. Pour modéliser un mode de vie typique « malbouffe », des souris mâles ont reçu un régime riche en graisses et en PTGA pendant plusieurs semaines, puis ont été évaluées pour leur santé métabolique, la qualité du sperme et le succès reproductif réel.
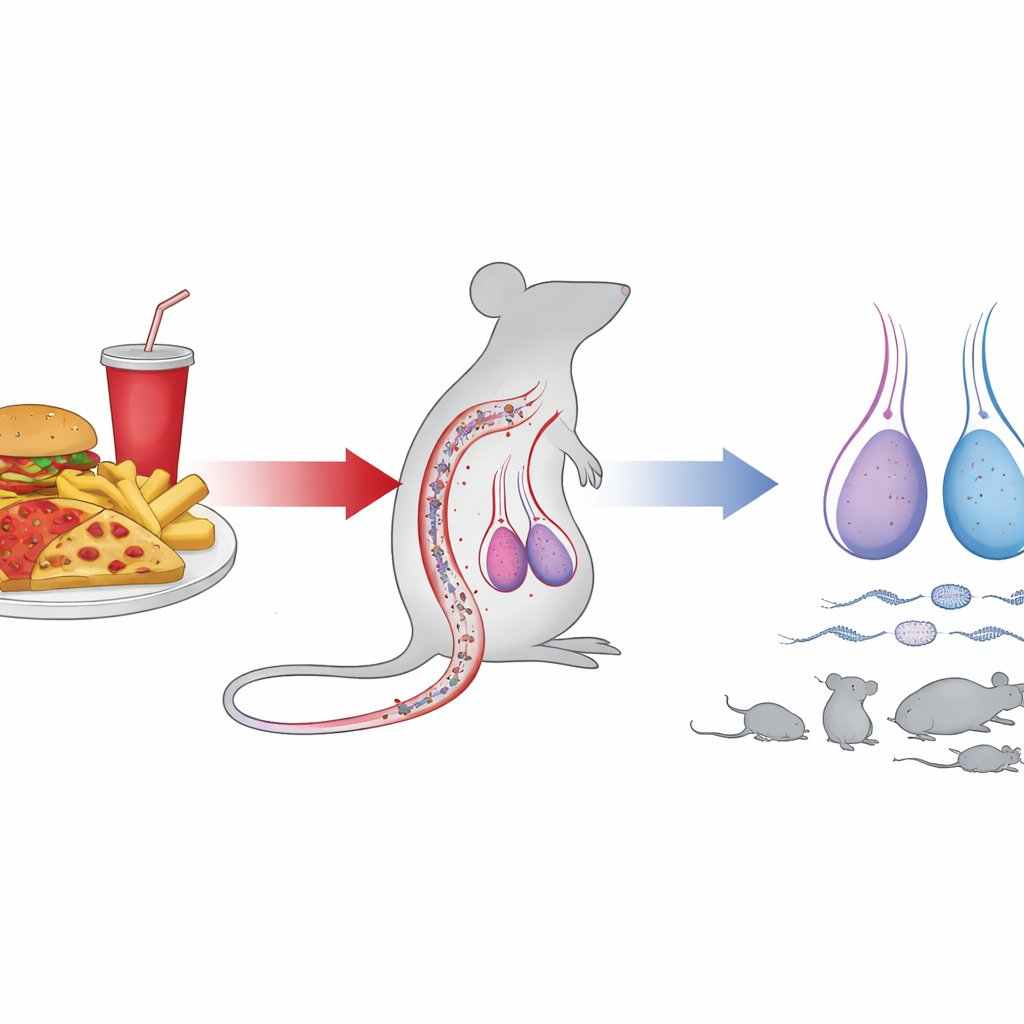
Ce que la malbouffe a fait aux souris mâles
Les souris soumises au régime de type malbouffe ont développé une signature biochimique claire d’excès de PTGA : des marqueurs clés dans le sang et les testicules ont augmenté, le cholestérol et la glycémie à jeun ont monté, et leur organisme a accumulé davantage de graisse. À l’intérieur des testicules, les indicateurs chimiques du stress oxydatif — un déséquilibre entre les molécules réactives nocives et les défenses de l’organisme — se sont aggravés. Cet environnement hostile a perturbé la production normale de spermatozoïdes. Les concentrations de spermatozoïdes ont diminué, leur motilité a chuté et un plus grand nombre de cellules présentaient des têtes et des flagelles déformés. Même l’emballage de l’ADN à l’intérieur des noyaux spermatiques était perturbé, laissant le matériel génétique moins compact et plus susceptible de se casser. Comme prévu, le sperme de ces animaux présentait plus de dommages à l’ADN et des signes d’atteinte membranaire.
De spermatozoïdes altérés à des grossesses fragilisées
Ces changements microscopiques ont eu des conséquences réelles. Lorsqu’on a accouplé les mâles avec des femelles saines, les couples impliquant des mâles nourris à la malbouffe avaient moins de chances d’aboutir à une grossesse. Quand des grossesses survenaient, elles étaient plus fragiles : les fausses couches étaient plus fréquentes, les portées étaient plus petites et les fœtus et les nouveau-nés tendaient à être plus légers. Autrement dit, le régime n’a pas seulement réduit les chiffres du sperme sur une lecture de laboratoire ; il a modifié toute la trajectoire reproductive, des taux de conception au développement précoce. Cela renforce l’idée émergente selon laquelle l’alimentation paternelle avant la conception peut influencer la santé des enfants, non seulement via les gènes mais aussi via des marques chimiques et des lésions portées par le sperme.
Tester deux moyens de lutter contre les dégâts
L’équipe a ensuite cherché à savoir si les dommages pouvaient être inversés. Ils ont comparé deux interventions. La première était l’Alagebrium (ALT-711), un médicament conçu pour rompre les liaisons croisées liées aux PTGA dans les tissus. La seconde était Fertilix®, un mélange d’antioxydants et de micronutriments tels que des vitamines, du sélénium, du zinc et du CoQ10, visant à restaurer la capacité de l’organisme à neutraliser les molécules réactives nocives. Les deux approches ont amélioré de nombreux signes chimiques et cellulaires de stress chez les souris nourries à la malbouffe. Le niveau de dommages oxydatifs dans les testicules a diminué, la capacité antioxydante a rebondi et plusieurs mesures de la qualité du sperme — y compris la motilité, l’intégrité structurale et la stabilité de l’ADN — se sont rapprochées de la normale.
Pourquoi les nutriments ont surpassé le médicament briseur d’AGE
Malgré des améliorations similaires sur de nombreux paramètres de laboratoire, les deux traitements ont divergé là où cela comptait le plus : la fertilité effective. Le mélange d’antioxydants et de micronutriments a presque complètement restauré les taux de grossesse, réduit les fausses couches et ramené la taille des portées et la croissance des petits au niveau des témoins sains. En revanche, le médicament briseur de PTGA a amélioré certains marqueurs liés au sperme mais n’a pas réussi à sauver les issues reproductives chez les souris nourries à la malbouffe et a même aggravé certaines mesures de grossesse chez des animaux autrement sains. Les auteurs suggèrent que cela s’explique par le fait que les régimes de type malbouffe ne se contentent pas de générer des PTGA : ils appauvrissent aussi l’organisme en nutriments protecteurs essentiels. Reconstituer ces éléments constitutifs peut être crucial pour rétablir un équilibre chimique sain dans les testicules et soutenir le développement normal du sperme, tandis que se concentrer uniquement sur la rupture des liaisons PTGA n’aborde pas complètement le déficit nutritionnel sous-jacent.
Ce que cela signifie pour les humains
En termes simples, l’étude montre qu’un régime régulier d’aliments denses en énergie et fortement transformés peut compromettre la fertilité masculine chez la souris en surchargeant l’organisme de composés nocifs dérivés du sucre et en vidant ses défenses naturelles. Réparer ces dommages semble possible, mais toutes les stratégies ne se valent pas : restaurer les micronutriments manquants et la capacité antioxydante s’est avéré bien plus efficace qu’un médicament qui n’attaque qu’un seul type de cicatrice moléculaire. Bien que les souris ne soient pas des humains et que des essais cliniques restent nécessaires et difficiles, ces résultats renforcent l’argument en faveur d’une réduction de la malbouffe et d’un régime riche en nutriments pour aider à protéger la fertilité masculine et les perspectives de santé de la génération suivante.
Citation: Darmishonnejad, Z., Hassan Zadeh, V., Tavalaee, M. et al. The impact of junk food on male fertility in mice: therapeutic interventions targeting advanced glycation end-products and oxidative stress. Sci Rep 16, 13874 (2026). https://doi.org/10.1038/s41598-026-42820-5
Mots-clés: malbouffe, fertilité masculine, produits terminaux de glycation avancée, stress oxydatif, compléments antioxydants