Clear Sky Science · fr
Analyse de modèles CNN hybrides optimisés par des algorithmes méta‑heuristiques pour la détection du mélanome
Pourquoi des dépistages du cancer de la peau plus intelligents sont importants
Le mélanome est une forme de cancer de la peau dangereuse qui peut se propager rapidement si elle n’est pas détectée tôt. Les dermatologues utilisent désormais des caméras et des logiciels en complément de l’examen à l’œil nu, mais concevoir des systèmes d’intelligence artificielle (IA) fiables pour ces images reste un défi. Cette étude explore une nouvelle manière de construire de tels systèmes en laissant des stratégies de recherche inspirées de la nature concevoir et régler automatiquement un modèle d’apprentissage profond, dans le but de détecter davantage de mélanomes tout en maîtrisant les faux positifs.
Apprendre aux ordinateurs à voir la peau en difficulté
Les chercheurs se concentrent sur les images dermoscopiques — des clichés rapprochés et agrandis de lésions cutanées pris avec un appareil spécialisé. Ces images contiennent des motifs subtils de couleur, de texture et de forme qui peuvent indiquer un cancer. Les réseaux de neurones convolutionnels (CNN) sont un type d’IA particulièrement efficace pour reconnaître de tels motifs visuels, mais ils sont délicats : leurs performances dépendent de nombreux choix de conception, comme le nombre de couches, la taille des filtres et la vitesse d’apprentissage. Traditionnellement, les experts estiment ou règlent manuellement ces paramètres, ou réutilisent des architectures issues de tâches non liées, ce qui peut limiter l’adaptation des modèles aux images de cancer de la peau.
Laisser une recherche inspirée par la nature concevoir le modèle
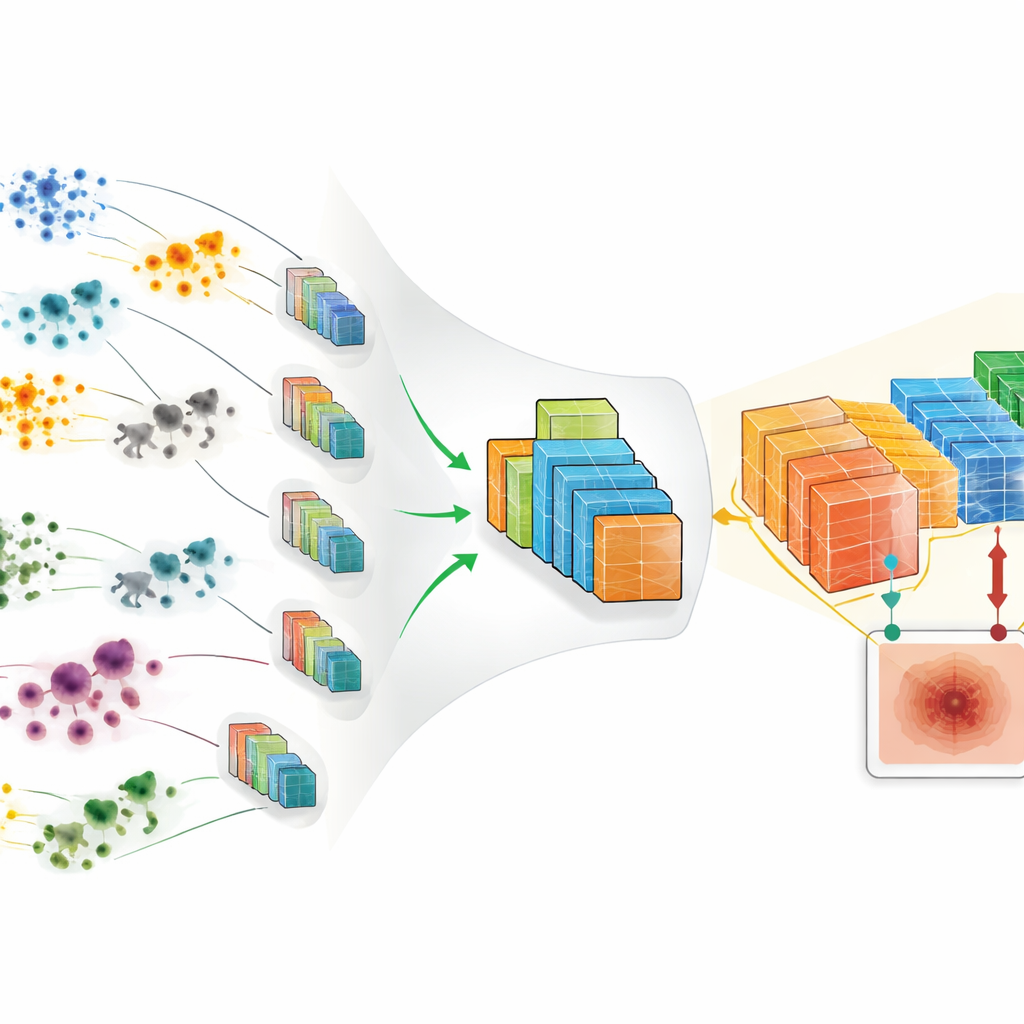
Plutôt que de fixer un CNN à l’avance, les auteurs transforment l’ensemble de la conception en un problème de recherche. Ils combinent le CNN avec six algorithmes dits méta‑heuristiques — des stratégies de recherche inspirées de comportements naturels tels que les coucous pondant dans le nid d’autres oiseaux, les loups chassant en meute ou les oiseaux se déplaçant en essaim. Dans ce cadre, chaque méta‑heuristique considère une conception complète de CNN, y compris ses principaux paramètres d’entraînement, comme une solution candidate. Elle génère ensuite de nombreux candidats, teste chacun en entraînant et validant effectivement un CNN sur des images de peau, et oriente progressivement la population vers des conceptions meilleures en fonction de leur capacité à distinguer précisément le mélanome des lésions bénignes.
Nettoyer et enrichir d’abord les images
Avant qu’un apprentissage puisse avoir lieu, les images doivent être préparées avec soin. L’équipe utilise la collection largement adoptée HAM10000, contenant plus de onze mille images dermoscopiques réparties en sept types de lésions cutanées, y compris le mélanome. Ils redimensionnent toutes les images à une taille standard, uniformisent les différences de luminosité et retirent les artefacts distrayants tels que les poils et les marques qui pourraient perturber le modèle. Pour aider le CNN à faire face à la variété rencontrée en clinique réelle, ils créent ensuite de nouvelles versions légèrement modifiées de chaque image de mélanome en les retournant, en les faisant pivoter, en zoomant, en recadrant et en ajustant la luminosité. Cela sert aussi à équilibrer le nombre d’exemples de mélanome et de non‑mélanome, évitant que le modèle n’apprenne simplement à privilégier la classe la plus fréquente.
Mettre six stratégies de recherche à l’épreuve
Au sein de cet ensemble de données nettoyé et enrichi, les six méta‑heuristiques — Cuckoo Search, Firefly Algorithm, Whale Optimization Algorithm, Particle Swarm Optimization, Grey Wolf Optimizer et Crow Search Algorithm — recherchent chacune des configurations CNN performantes. Elles explorent des choix tels que le nombre de couches convolutionnelles, le nombre de filtres par couche, l’application ou non d’une technique de stabilisation appelée batch normalization, la taille des lots d’entraînement et le taux d’apprentissage qui contrôle la vitesse de mise à jour des paramètres du modèle. Pour chaque conception proposée, un CNN est construit, entraîné et évalué sur un ensemble de validation séparé, et son exactitude est renvoyée à l’algorithme de recherche comme score pour guider la génération des candidats suivants. Ce cycle se répète selon plusieurs schémas expérimentaux qui font varier les tailles de population et le nombre d’itérations pour chaque optimiseur.
Quelles stratégies ont le mieux fonctionné
Les six approches ont toutes produit des CNN surpassant un réseau de référence soigneusement conçu et réglé manuellement. Le référentiel plafonnait autour de 84 % de classifications correctes, tandis que les meilleurs modèles guidés par des méta‑heuristiques atteignaient environ 91 % de précision. Deux algorithmes se distinguent. Cuckoo Search a fourni la meilleure précision globale et la meilleure sensibilité — ce qui signifie qu’il excellait particulièrement à détecter les mélanomes et à réduire le risque de cancers manqués. Grey Wolf Optimizer a offert une précision comparable tout en obtenant la meilleure capacité à reconnaître correctement les lésions bénignes, diminuant ainsi les faux positifs. D’autres méthodes, comme Firefly Algorithm, étaient compétitives mais avec plus de variabilité, tandis que Particle Swarm et Crow Search avaient tendance à se fixer prématurément sur des régions moins optimales de l’espace de conception.
Regarder à l’intérieur du « raisonnement » du modèle
Parce que l’IA médicale doit inspirer confiance aux cliniciens, les auteurs examinent aussi comment les CNN optimisés prennent leurs décisions. En utilisant une technique de visualisation appelée Grad‑CAM++, ils génèrent des cartes de chaleur colorées superposées aux images d’entrée montrant où le réseau « regarde » lorsqu’il classe une lésion comme maligne ou bénigne. Dans les cas réussis, ces cartes se focalisent sur la lésion elle‑même plutôt que sur la peau environnante ou des artefacts résiduels, et mettent en évidence des structures irrégulières concordant avec ce que les dermatologues considèrent comme suspect. Quand le système se trompe, il a souvent des difficultés avec des lésions visuellement ambiguës même pour les spécialistes, comme des taches bénignes à texture rugueuse ou des mélanomes précoces à contraste très subtil.
Ce que cela signifie pour les futurs dépistages de la peau
Pour un non‑spécialiste, le message principal est que l’étude montre que laisser des stratégies de recherche inspirées de la nature concevoir les mécanismes internes d’un modèle d’apprentissage profond peut rendre la détection automatisée du mélanome à la fois plus précise et plus fiable que le seul réglage manuel par des experts. En comparant systématiquement plusieurs de ces stratégies sur le même grand jeu de données public, les auteurs identifient Cuckoo Search et Grey Wolf Optimizer comme des outils particulièrement prometteurs pour construire de futurs systèmes d’aide à la décision clinique. Bien que ces systèmes ne soient pas destinés à remplacer les dermatologues, ils pourraient devenir des seconds lecteurs précieux, aidant à réduire le risque de passer à côté de lésions dangereuses et à diminuer l’angoisse et les procédures inutiles liées aux taches bénignes.
Citation: Hermosilla, P., Soto, R., Monfroy, E. et al. Analysis of hybrid CNN models optimized with metaheuristic algorithms for melanoma detection. Sci Rep 16, 13075 (2026). https://doi.org/10.1038/s41598-026-42711-9
Mots-clés: détection du mélanome, imagerie dermoscopique, réseaux de neurones convolutionnels, optimisation méta‑heuristique, intelligence artificielle médicale