Clear Sky Science · fr
Efficacité d’un nouveau bactériophage pour contrôler Escherichia coli associé aux environnements d’élevages porcins et son potentiel de disruption des biofilms
Pourquoi les élevages porcins et les microbes nous concernent tous
Ce qui se passe dans une porcherie peut sembler loin de la vie quotidienne, mais les bactéries qui s’y développent peuvent se propager par la viande, l’eau et l’environnement au sens large pour atteindre les humains. À mesure que les antibiotiques perdent de leur efficacité contre ces microbes, les scientifiques recherchent urgemment de nouvelles méthodes pour maintenir la santé des animaux et la sécurité alimentaire. Cette étude explore si un virus d’origine naturelle, qui s’attaque aux bactéries, peut aider à contrôler une souche problématique d’Escherichia coli dans les élevages porcins, en particulier lorsque les bactéries se regroupent en couches protectrices tenaces appelées biofilms.
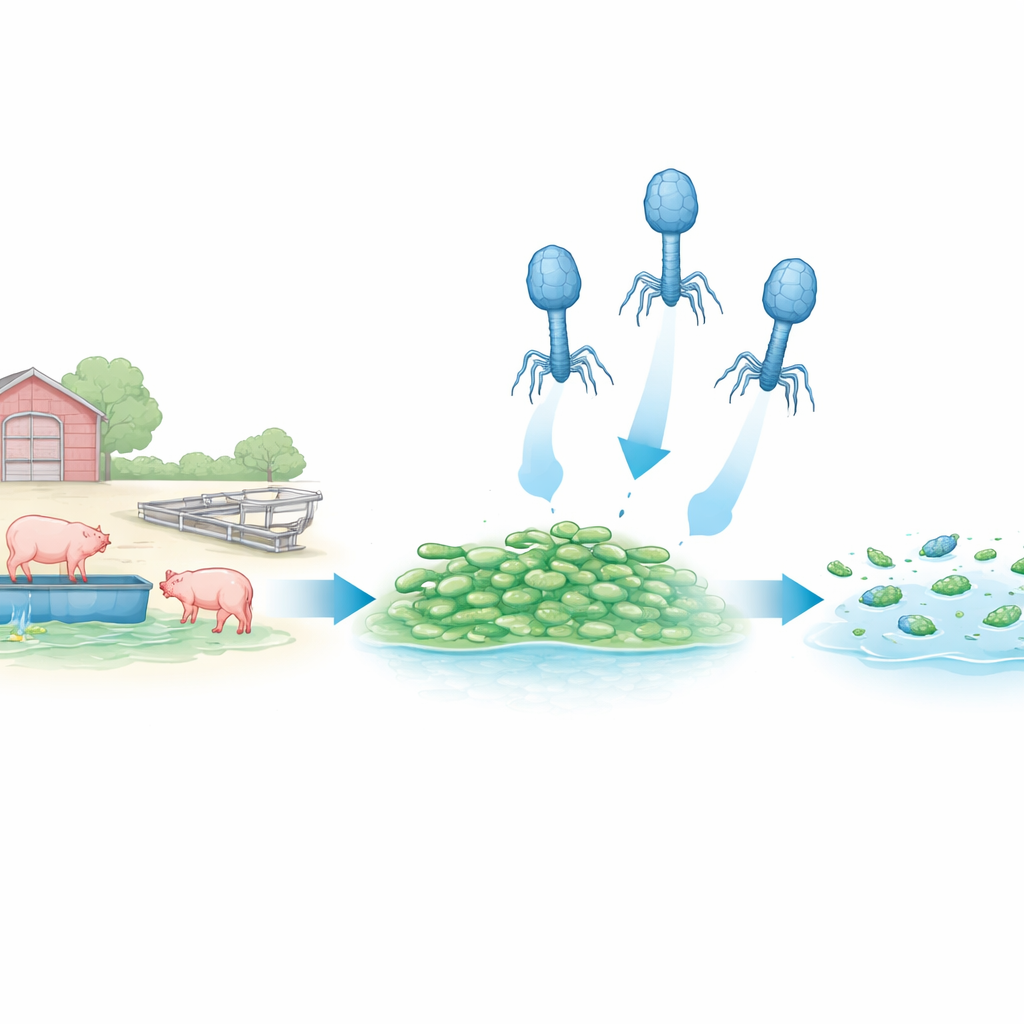
Un petit chasseur trouvé dans l’eau de rivière
Les chercheurs ont commencé par prélever de l’eau dans le fleuve Chao Phraya à Bangkok et à y chercher des virus ciblant spécifiquement des E. coli multirésistantes issues des eaux usées d’élevages porcins. Ils en ont isolé un candidat prometteur qu’ils ont nommé vECPPW9. Au microscope électronique, ce virus présente une forme classique de « module d’atterrissage spatial », avec une tête polyédrique et une queue contractile qui lui permet de s’accrocher aux cellules bactériennes. En laboratoire, vECPPW9 a tué environ 40 % des souches résistantes d’E. coli examinées, lui conférant une portée raisonnablement large parmi les bactéries problématiques trouvées dans ces environnements d’élevage.
Attaque rapide, fort impact et résistance au stress
Pour évaluer les performances de vECPPW9 en tant que prédateur bactérien, l’équipe a suivi la rapidité avec laquelle il se fixe à ses cibles et se multiplie. À température corporelle, plus de 90 % des particules virales se sont attachées aux cellules d’E. coli en moins de dix minutes. Une fois à l’intérieur, le virus a eu besoin d’environ 20 minutes de préparation discrète avant de libérer des centaines de descendants par cellule infectée, provoquant la lyse des bactéries. Même lorsque les scientifiques ont ajouté relativement peu de particules virales par rapport au nombre de bactéries, la croissance d’E. coli a été fortement supprimée en moins d’une heure, et le nombre de bactéries est resté bien inférieur à celui des cultures non traitées pendant 24 heures. Le phage est également resté stable à des températures typiques de stockage et des bâtiments d’élevage et sur une assez large plage d’acidité, des caractéristiques importantes s’il doit être utilisé dans de véritables porcheries et systèmes d’eau.
Un plan génétique sûr doté d’outils puissants
L’équipe a séquencé l’ensemble du matériel génétique de vECPPW9 pour en vérifier l’identité et la sûreté. Le virus porte un grand génome d’ADN double brin contenant des centaines de gènes qui construisent sa structure, répliquent son ADN et provoquent la lyse des cellules hôtes. De façon cruciale, les chercheurs n’ont trouvé aucun gène lié à des toxines bactériennes, à la résistance aux antibiotiques ou à la capacité de s’intégrer silencieusement dans les chromosomes bactériens. À la place, ils ont identifié des enzymes capables de perforer les parois bactériennes et probablement d’autres qui dégradent les sucres visqueux formant les biofilms. Des comparaisons avec des virus connus ont montré que vECPPW9 appartient à un groupe appelé Phapecoctavirus, mais qu’il est suffisamment distinct pour être considéré comme une nouvelle espèce au sein de cette famille de phages strictement lytique.
Démanteler des communautés bactériennes tenaces
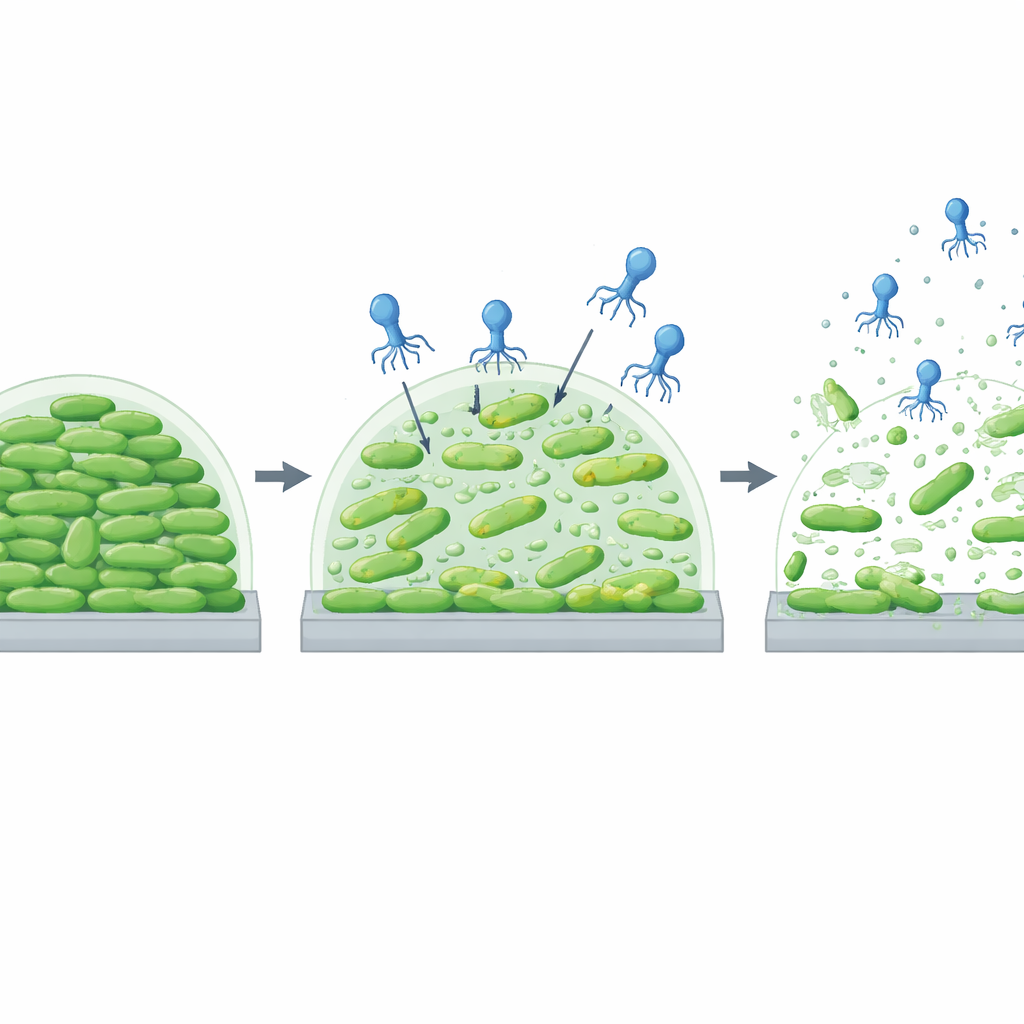
Étant donné que de nombreuses bactéries d’élevage vivent en biofilms sur des surfaces plastiques, caoutchoutées et métalliques, les scientifiques ont testé si vECPPW9 pouvait empêcher ces communautés de se former ou les dégrader une fois établies. Dans des puits plastiques simples, mélanger le phage avec E. coli dès le départ a réduit la masse de biofilm jusqu’à environ trois quarts et diminué le nombre de cellules vivantes à l’intérieur de plus de cent fois, selon la dose et la durée d’exposition. Lorsque l’équipe a laissé les biofilms se développer pendant un jour ou trois avant d’ajouter le phage, vECPPW9 a encore réduit l’épaisseur du film visqueux et le nombre de bactéries survivantes. Au microscope électronique à balayage, les biofilms non traités ressemblaient à des villes denses et bien organisées de cellules bacillaires intactes, tandis que les surfaces traitées au phage étaient jonchées de bactéries éclatées et de débris, et la matrice lisse était visiblement perturbée.
Nettoyer des surfaces proches de celles des élevages
Pour mieux imiter les conditions des porcheries, les chercheurs ont fait croître des biofilms d’E. coli sur des tubulures en caoutchouc et des coupons en acier inoxydable similaires à ceux utilisés dans les abreuvoirs et les conduites. Sur trois jours, les biofilms se sont épaissis de façon continue dans les témoins non traités, mais les surfaces exposées à vECPPW9 ont montré beaucoup moins d’accumulation à chaque point temporel. Lorsque les biofilms ont été autorisés à se former d’abord puis traités seulement ensuite par le phage, le virus a de nouveau diminué la biomasse par rapport aux témoins, même lorsque les communautés étaient plus mûres. Ces résultats suggèrent que vECPPW9 peut à la fois prévenir et réduire les biofilms sur les types de matériaux présents dans les systèmes d’eau et d’alimentation, améliorant potentiellement l’hygiène et réduisant la propagation de bactéries résistantes.
Ce que cela pourrait signifier pour les élevages et l’alimentation
Dans l’ensemble, l’étude présente vECPPW9 comme un chasseur viral à action rapide et au profil génétique sûr, capable de tuer des E. coli multirésistantes et d’affaiblir les biofilms qui les abritent sur les surfaces d’élevage. Bien que toutes les expériences aient été menées en conditions de laboratoire contrôlées et que des travaux supplémentaires soient nécessaires chez les animaux vivants et dans des élevages réels, les résultats indiquent des usages pratiques : ajouter des phages à l’eau de boisson ou à l’alimentation, ou les pulvériser sur les équipements et les conduites pour maintenir les bactéries nocives sous contrôle. Si de telles approches s’avèrent efficaces et sûres à grande échelle, elles pourraient aider les éleveurs à réduire leur dépendance aux antibiotiques, freiner la propagation de la résistance et, en fin de compte, rendre la production de porc plus sûre pour les animaux, les travailleurs et les consommateurs.»
Citation: Wintachai, P., Thonguppatham, R., Smith, D.R. et al. Efficacy of a novel bacteriophage in controlling Escherichia coli associated with swine farm environments and its potential for biofilm disruption. Sci Rep 16, 12937 (2026). https://doi.org/10.1038/s41598-026-42644-3
Mots-clés: thérapie par bactériophages, Escherichia coli, élevage porcin, contrôle des biofilms, résistance aux antibiotiques