Clear Sky Science · fr
Intégrer la génétique, l’âge et l’imagerie pour prédire les résultats du traitement dans la dégénérescence maculaire néovasculaire liée à l’âge : une étude de preuve de concept
Pourquoi c’est important pour la vision et le vieillissement
À mesure que l’espérance de vie augmente, un nombre croissant de personnes sont exposées au risque de dégénérescence maculaire liée à l’âge, une maladie qui peut voler la vision centrale et rendre des activités quotidiennes comme la lecture ou la conduite difficiles voire impossibles. Les médecins disposent aujourd’hui d’injections oculaires efficaces capables de ralentir ou d’arrêter une forme agressive de la maladie, mais les patients diffèrent largement dans leur réponse et dans la fréquence des traitements nécessaires. Cette étude examine si la combinaison des informations issues de nos gènes, des examens rétiniens et de l’âge peut aider les cliniciens à prévoir qui bénéficiera le plus de la thérapie et comment la maladie évoluera dans le temps, ouvrant la voie à des soins oculaires plus personnalisés.
Assembler trois indices
Les chercheurs se sont concentrés sur la dégénérescence maculaire néovasculaire, la forme « humide » causée par des nouveaux vaisseaux qui fuient sous la rétine. Les 106 participants ont tous été traités dans un même hôpital spécialisé selon un protocole standardisé de « treat-and-extend » avec des injections anti‑VEGF, des médicaments de référence pour contrôler la maladie. Pour chaque personne, l’équipe a recueilli trois types d’informations disponibles de routine dans les cliniques modernes : des images tomographiques en coupe de la rétine (scans OCT), un échantillon sanguin pour le test génétique et des données démographiques simples comme l’âge au moment de la première injection. 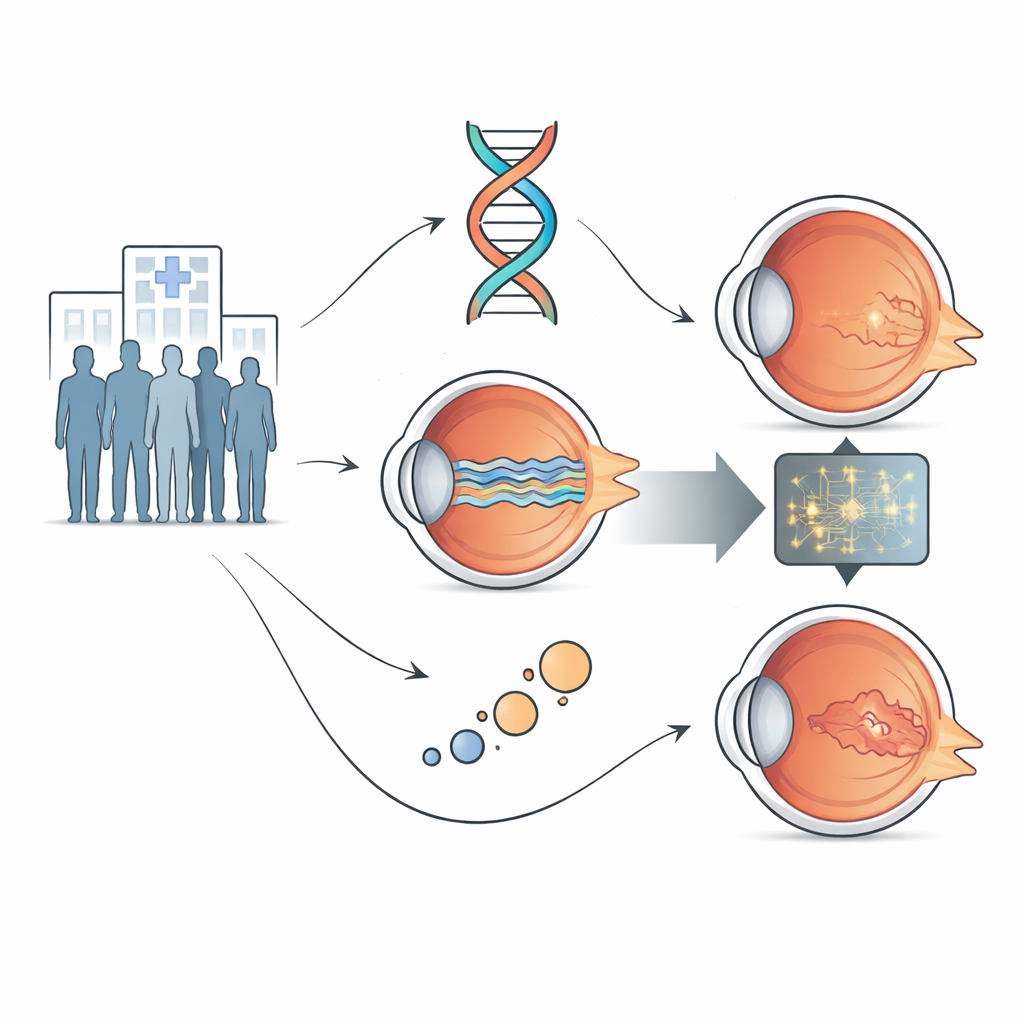
Lire la rétine avec l’intelligence artificielle
Les scans OCT peuvent révéler de petites poches de liquide et d’autres modifications structurelles de la rétine qui signalent une maladie active. Plutôt que de s’appuyer sur des évaluations humaines, l’équipe a utilisé un modèle d’apprentissage profond pour mesurer automatiquement le volume de plusieurs caractéristiques clés, notamment le liquide intra‑rétinien et sous‑rétinien ainsi que les renflements sous la couche photoréceptrice. Ces mesures ont servi d’indicateurs objectifs du degré d’atteinte ou d’activité de l’œil au début du traitement. L’objectif principal était de prédire si un œil serait « sec » — essentiellement dépourvu de liquide visible — deux ans après le début du traitement, un état qui reflète une maladie calme et qui est facile à vérifier par imagerie.
La charge génétique comme pièce supplémentaire du puzzle
L’étude a également intégré un score de risque polygénique, un nombre unique qui résume l’effet combiné de nombreux variants génétiques courants associés à la dégénérescence maculaire. Plutôt que de prédire à lui seul la réponse au traitement, ce score capture principalement la propension d’une personne à développer la maladie et l’âge probable d’apparition. Dans cette cohorte, les participants avaient tendance à présenter un risque génétique plus élevé que la population générale, et ceux avec des scores plus élevés commençaient le traitement à un âge plus jeune, ce qui suggère que la charge génétique déclenche la maladie plus tôt dans la vie même si elle ne dicte pas directement la réaction de l’œil aux injections.
Performance du modèle combiné
Pour tester si le mélange de ces indices améliorait la prévision, les chercheurs ont construit des modèles d’apprentissage automatique utilisant différentes combinaisons d’âge, d’imagerie et de données génétiques. Lorsqu’ils ont tenté de prédire une macula sèche à deux ans en n’utilisant que les caractéristiques issues des scans, la performance était correcte. En ajoutant le score de risque génétique et l’âge, la capacité du modèle à distinguer les yeux qui deviendraient secs de ceux qui ne le seraient pas s’est améliorée sensiblement, atteignant un niveau élevé de précision selon les critères statistiques habituels. 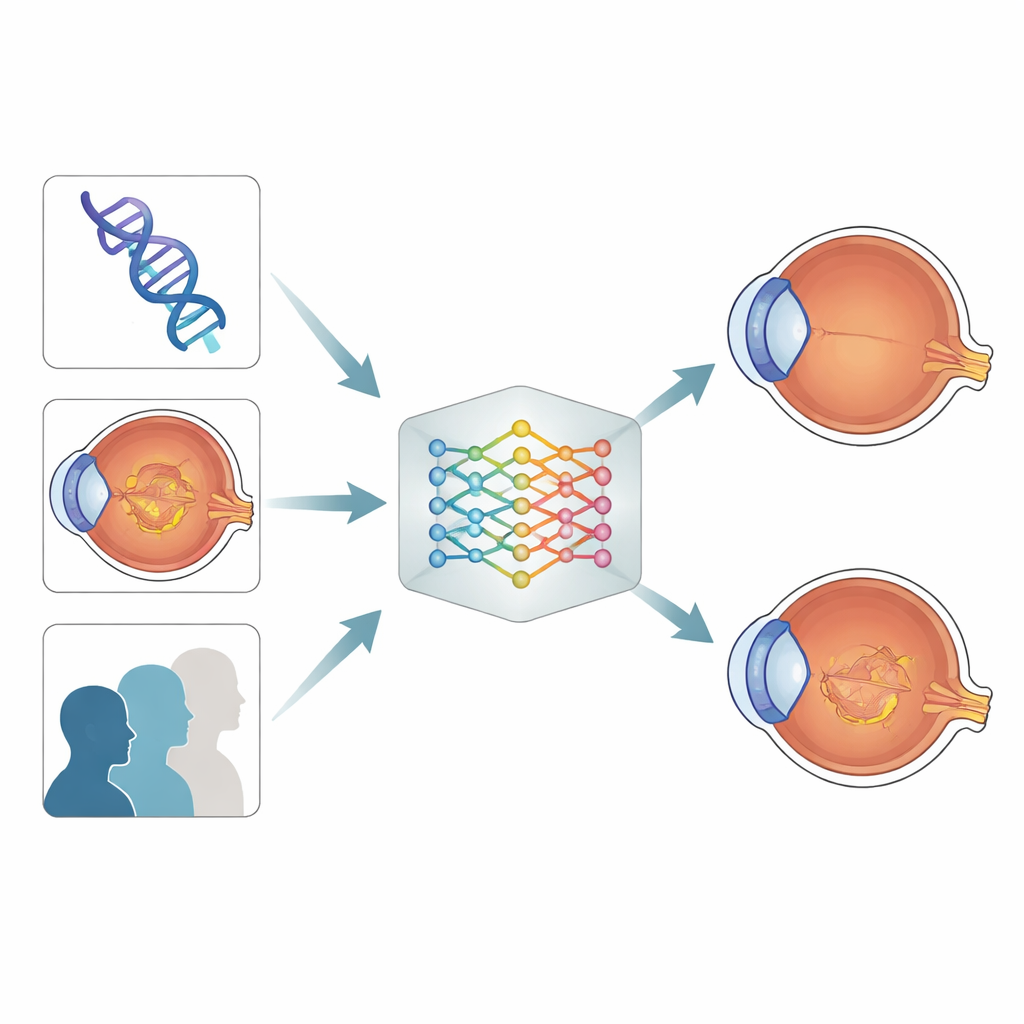
Ce que cela signifie pour les patients et l’avenir
Pour les personnes atteintes de dégénérescence maculaire ou à risque, ce travail de preuve de concept suggère qu’une approche de traitement plus individualisée pourrait se profiler. En combinant le risque héréditaire d’une personne, les détails fins de sa structure rétinienne et son âge, les cliniciens pourront peut‑être estimer les chances d’obtenir une macula calme et sans liquide et planifier le suivi en conséquence. L’étude actuelle est de petite taille et issue d’un seul centre, de sorte que ses modèles ne sont pas encore prêts pour un usage clinique courant, et ils se concentrent sur des résultats anatomiques plutôt que sur l’expérience visuelle quotidienne. Néanmoins, les résultats montrent que l’intégration de la génétique et de l’imagerie avancée dans un seul cadre d’intelligence artificielle est techniquement réalisable et biologiquement cohérente, posant les bases d’études plus larges qui pourraient apporter la médecine de précision au premier plan des soins oculaires.
Citation: Moghul, I., Pontikos, N., Sharma, A. et al. Integrating genetics, age and imaging to predict treatment outcomes in neovascular age-related macular degeneration: a proof-of-concept study. Sci Rep 16, 12489 (2026). https://doi.org/10.1038/s41598-026-41931-3
Mots-clés: dégénérescence maculaire liée à l’âge, score de risque génétique, imagerie rétinienne, intelligence artificielle, traitement oculaire personnalisé