Clear Sky Science · fr
Identification et validation de gènes pronostiques associés à la réponse intégrée au stress dans l’adénocarcinome pulmonaire et construction de modèles de risque
Pourquoi les signaux de stress dans le cancer du poumon comptent
L’adénocarcinome pulmonaire est l’une des formes de cancer du poumon les plus fréquentes et les plus mortelles, pourtant des patients présentant des tumeurs apparemment similaires peuvent avoir des évolutions très différentes. Cette étude pose une question simple mais puissante : peut-on lire les « signaux de stress » internes des cellules cancéreuses pour prédire quels patients auront de mauvais pronostics et orienter le choix des traitements ? En examinant en profondeur les gènes qui aident les cellules à faire face au stress, les chercheurs ont cherché à construire un outil pratique que les cliniciens pourraient un jour utiliser pour personnaliser la prise en charge.
Lire les appels de détresse de la cellule
Toutes les cellules, y compris les cellules cancéreuses, sont constamment confrontées au manque d’oxygène, à des molécules toxiques, à des protéines mal repliées et à des lésions de l’ADN. Pour survivre, elles activent un système d’alarme interne commun appelé la réponse intégrée au stress. Les auteurs ont rassemblé de larges jeux de données génétiques provenant de centaines de tumeurs d’adénocarcinome pulmonaire et de tissus pulmonaires non cancéreux appariés. À partir de plus de 500 gènes connus pour être liés au stress, ils ont d’abord identifié ceux qui étaient anormalement actifs ou silencieux dans les tumeurs par rapport au tissu sain. Cela a produit une liste restreinte de 34 candidats qui semblaient relier la machinerie de la réponse au stress à la biologie du cancer pulmonaire.
Réduire à cinq gènes d’alerte clés
Ensuite, l’équipe a recherché lesquels de ces candidats suivaient réellement la durée de vie des patients. En utilisant des modèles statistiques reliant l’activité génique à la survie, ils se sont concentrés sur cinq gènes — AGER, GPX3, CCNA2, KCNK3 et CHEK1. Trois d’entre eux (AGER, GPX3 et KCNK3) avaient tendance à être moins exprimés dans les tumeurs et semblaient protecteurs lorsqu’ils étaient présents, tandis que deux (CCNA2 et CHEK1) étaient surexprimés dans les tumeurs et associés à de moins bons résultats. Les chercheurs ont confirmé ces profils en utilisant des échantillons tumoraux provenant de leur propre hôpital, montrant que cette combinaison de cinq gènes n’est pas seulement une particularité des bases de données publiques mais se vérifie aussi chez des patients réels.
Transformer l’activité génique en score de risque
Avec ces cinq gènes, les auteurs ont construit un simple « score de risque » numérique qui pondère chaque gène selon la force de son lien avec la survie. La tumeur de chaque patient reçoit un score basé sur son profil d’expression génique. Lorsque les patients ont été séparés en groupes à haut risque et à faible risque selon ce score, ceux du groupe à haut risque mouraient plus rapidement et plus fréquemment. La prédiction a tenu non seulement dans le jeu de données principal, mais aussi dans deux cohortes indépendantes de patients. Pour rendre l’outil plus utilisable en clinique, l’équipe a combiné le score de risque basé sur les gènes avec les caractéristiques de stadification tumorale standard dans un nomogramme — une sorte de calculateur graphique qui estime les chances de survie à un, deux ou trois ans.
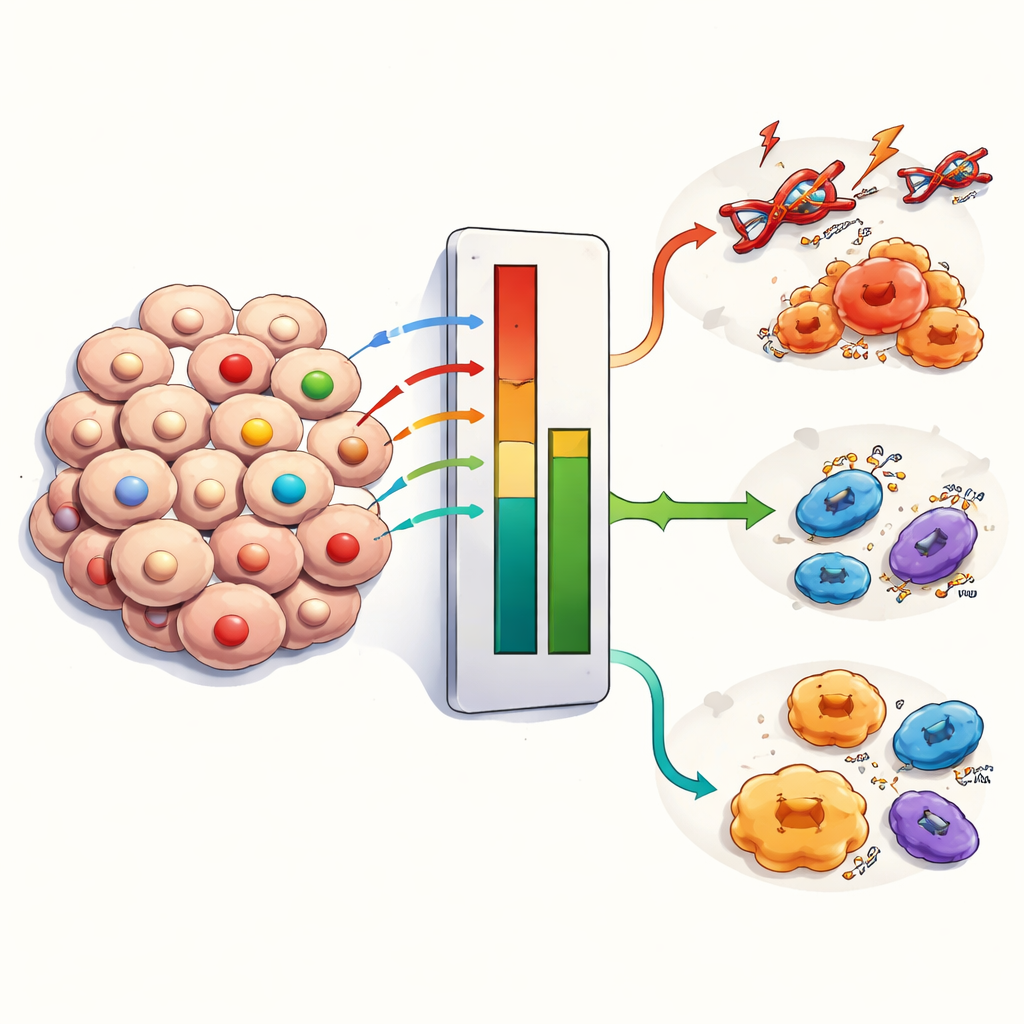
Ce que révèle le score de risque à l’intérieur de la tumeur
En creusant davantage, les chercheurs ont constaté que les tumeurs avec des scores de risque élevés étaient plus fortement mutées et présentaient des profils de présence de cellules immunitaires différents de ceux des tumeurs à faible risque. Les cancers à haut risque avaient plus de mutations au total et davantage d’indices d’« évasion immunitaire », ce qui signifie qu’ils étaient meilleurs pour échapper aux défenses de l’organisme et étaient moins susceptibles de bénéficier de certaines immunothérapies. Des types cellulaires immunitaires spécifiques, comme les lymphocytes T auxiliaires activés, les macrophages et les cellules B mémoires, montraient des liens forts avec les cinq gènes, suggérant que ces marqueurs liés au stress sont associés non seulement aux cellules cancéreuses elles-mêmes mais aussi à l’environnement immunitaire environnant. L’équipe a également utilisé des données de réponse aux médicaments pour proposer quelles chimiothérapies pourraient mieux fonctionner chez les patients à faible ou à haut risque, ouvrant la voie à des façons futures d’adapter les médicaments au profil de stress d’une tumeur.
Du stress moléculaire à des orientations pratiques
En termes simples, ce travail traduit le brouhaha moléculaire à l’intérieur des tumeurs pulmonaires en un signal concentré de cinq gènes qui aide à prédire qui est susceptible d’avoir un mauvais pronostic et pourquoi. L’étude montre que la capacité d’un cancer à gérer le stress est étroitement liée à la rapidité de sa croissance, à la fréquence des lésions de son ADN et à sa façon d’interagir avec le système immunitaire. Bien que des validations supplémentaires soient nécessaires avant que cet outil puisse guider les décisions de tous les jours, l’approche indique un avenir où un petit test génique pourrait aider les médecins à identifier les patients atteints d’adénocarcinome pulmonaire à haut risque, à adapter leurs traitements et, potentiellement, à améliorer la survie en ciblant la machinerie d’adaptation au stress de la tumeur.
Citation: Fu, J., Tao, Y. & Liu, W. Identification and validation of prognostic genes associated with integrative stress response in lung adenocarcinoma and construction of the risk models. Sci Rep 16, 11300 (2026). https://doi.org/10.1038/s41598-026-40547-x
Mots-clés: adénocarcinome pulmonaire, réponse intégrée au stress, biomarqueurs pronostiques, microenvironnement immunitaire tumoral, thérapie personnalisée du cancer