Clear Sky Science · fr
L’umami induit la sénescence des épithéliums pulmonaires via la miMOMP déclenchée par l’acide L-glutamique
Pourquoi la saveur « savoureuse » peut importer pour vos poumons
Beaucoup connaissent le glutamate monosodique (GMS) comme l’ingrédient qui confère aux aliments un goût riche et « umami ». Cette étude suggère que la consommation importante et prolongée de GMS ou d’autres régimes riches en glutamate pourrait, discrètement, affecter la santé pulmonaire. Chez la souris et dans des cellules pulmonaires, les chercheurs ont retracé comment un excès de glutamate alimentaire peut pousser les cellules pulmonaires vers un état vieilli et épuisé, susceptible d’aggraver les maladies pulmonaires chroniques. Leur travail met en lumière un nouveau lien entre notre alimentation et le vieillissement des poumons.
De l’assiette aux problèmes respiratoires
L’équipe a commencé par donner aux souris de l’eau contenant de fortes concentrations de GMS pendant plusieurs semaines. Ils ont évalué la fonction pulmonaire des animaux à l’aide d’un système de ventilation spécialisé. Au fil du temps, les souris ont développé des poumons plus raides et une capacité réduite à se dilater et à inspirer — des signes d’altération respiratoire. À l’examen microscopique des tissus pulmonaires, on observait des zones croissantes de lésions et de cicatrisation précoce. Les analyses biochimiques pulmonaires ont montré que le GMS augmentait les niveaux de glutamate, l’acide aminé responsable de la saveur umami, et que des concentrations plus élevées de glutamate corrélaient fortement avec une fonction pulmonaire dégradée et davantage de lésions.
Des régimes riches différents, le même problème
Le GMS n’est pas la seule façon d’augmenter le glutamate dans l’organisme ; les chercheurs ont donc testé deux autres régimes connus pour élever le glutamate : un régime riche en graisses sur le long terme et un régime riche en protéines. Bien que ces régimes aient eu des effets très différents sur le poids corporel, tous deux ont entraîné davantage de lésions pulmonaires et d’accumulation de tissu fibreux chez la souris, ainsi qu’une élévation du glutamate dans les poumons. Là encore, plus le glutamate était présent, plus les dommages observés étaient importants. Ces résultats suggèrent que le glutamate lui-même, plutôt qu’une propriété spécifique du GMS, est un facteur commun reliant les régimes riches aux atteintes pulmonaires.
Comment les cellules pulmonaires vieillissent prématurément
Pour comprendre ce que faisait le glutamate à l’intérieur des poumons, l’équipe s’est concentrée sur la mince couche de cellules qui tapisse les alvéoles, essentielles aux échanges gazeux. Ils ont cherché des signes de sénescence cellulaire, un état où les cellules cessent de se diviser, sécrètent des substances inflammatoires et dégradent progressivement les tissus environnants. Chez les souris alimentées au GMS, une fraction plus importante de ces cellules épithéliales exprimait un marqueur clé de sénescence. Dans des cellules pulmonaires humaines en culture exposées au glutamate, les mêmes marqueurs augmentaient, et les cellules présentaient des colorations associées au vieillissement ainsi qu’une libération accrue de molécules inflammatoires comme l’IL-6 et l’IL-8. Lorsque les chercheurs ont traité les souris nourries au GMS avec une combinaison de médicaments ciblant les cellules sénescentes, la fonction pulmonaire s’est améliorée et les lésions tissulaires ont diminué, même si les niveaux de glutamate restaient élevés. Cela indique que l’accumulation de cellules âgées était une cause majeure de la défaillance pulmonaire.
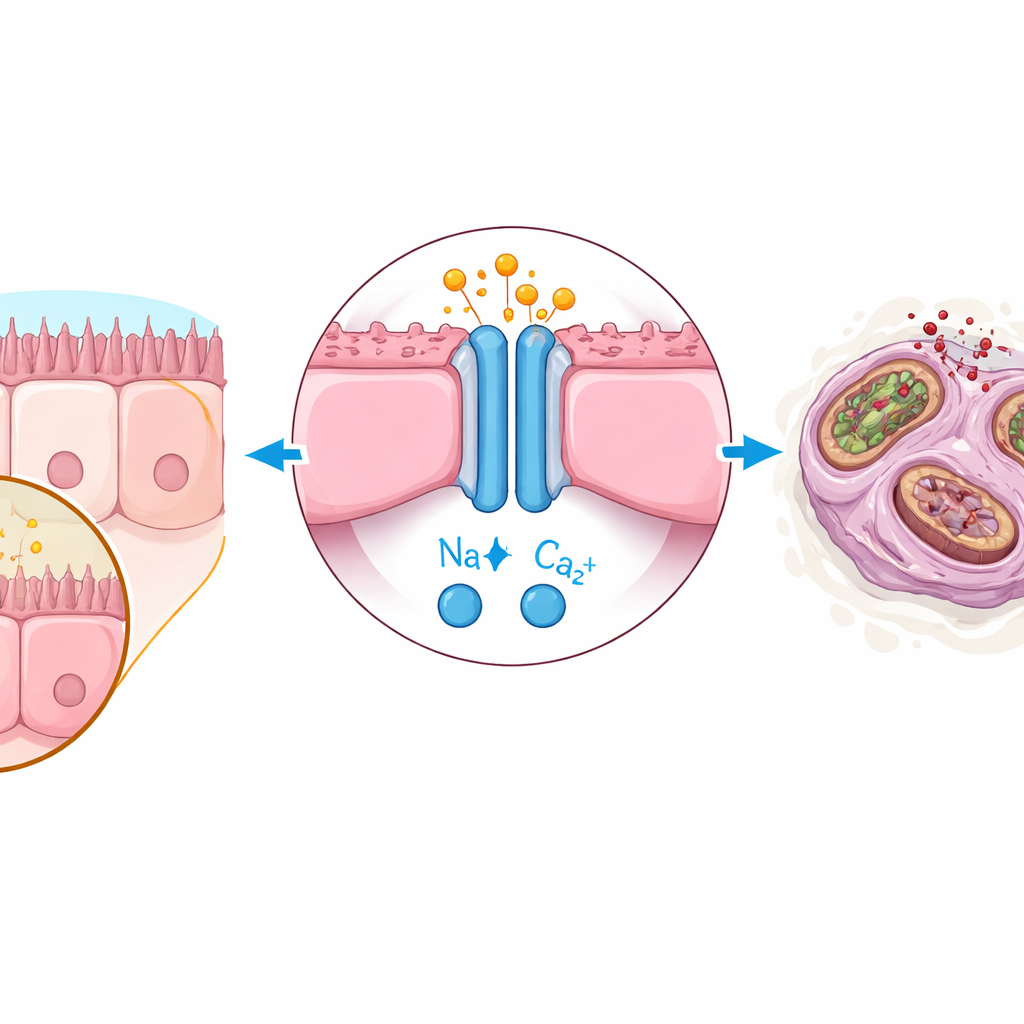
Une réaction en chaîne cachée à l’intérieur des cellules pulmonaires
En creusant plus avant, l’étude a mis au jour la cascade interne qui relie le glutamate à la sénescence. Les cellules pulmonaires portent un récepteur appelé NMDAR, surtout connu dans les cellules cérébrales où il répond au glutamate. Dans les poumons, un excès de glutamate suractive ce récepteur, ce qui perturbe ensuite les mitochondries, les centrales énergétiques de la cellule. Plutôt qu’une rupture totale, les mitochondries subissent une fuite limitée de contenu, un processus appelé perméabilisation partielle de la membrane externe mitochondriale (miMOMP). Cette lésion subtile suffit à activer une enzyme habituellement liée à la mort cellulaire, la caspase-3, à des niveaux faibles qui ne tuent pas la cellule mais l’incitent à entrer en sénescence. Bloquer le NMDAR avec des médicaments comme la mémantine, ou inhiber les caspases, a réduit le stress mitochondrial, atténué les marqueurs de sénescence et protégé le tissu pulmonaire chez la souris.
Lorsque la maladie pulmonaire fibrosante rencontre un régime riche
L’équipe a ensuite examiné ce qui se produit si un régime riche en glutamate est superposé à une lésion pulmonaire préexistante. Ils ont utilisé la bléomycine, un médicament qui provoque chez la souris une fibrose pulmonaire ressemblant à la fibrose pulmonaire chez l’homme. Comme prévu, la bléomycine seule causait des lésions, une accumulation de collagène et davantage de cellules épithéliales sénescentes. Mais lorsqu’elle était combinée au GMS, à un régime riche en graisses ou à un régime riche en protéines, les dommages et la fibrose étaient nettement aggravés, et les niveaux de glutamate pulmonaires augmentaient encore. Ces constatations suggèrent que les régimes riches en glutamate peuvent non seulement endommager des poumons sains, mais aussi accélérer l’évolution d’une maladie pulmonaire fibrosante déjà établie.
Ce que cela signifie au quotidien
Pour un public non spécialiste, le message n’est pas qu’une portion occasionnelle d’un plat savoureux endommagera les poumons, mais que l’exposition lourde et prolongée au glutamate — qu’il provienne du GMS ou de régimes riches en graisses ou en protéines — peut contribuer au vieillissement et à la cicatrisation des poumons. Le travail identifie le glutamate alimentaire comme un facteur de risque potentiellement modifiable pour les maladies pulmonaires chroniques et met en lumière une voie spécifique — l’axe NMDAR–miMOMP–sénescence — que des traitements futurs pourraient cibler. Bien que des études supplémentaires chez l’humain et à des niveaux d’apport plus typiques soient nécessaires, cette étude ouvre la voie à considérer la santé pulmonaire non seulement en termes de qualité de l’air et de tabagisme, mais aussi en termes de choix alimentaires quotidiens qui façonnent le vieillissement des organes qui nous permettent de respirer.
Citation: Zhang, J., Zhao, Y., Yang, B. et al. Umami induces pulmonary epithelial senescence via L-glutamic acid-triggered minority MOMP. npj Sci Food 10, 125 (2026). https://doi.org/10.1038/s41538-026-00783-x
Mots-clés: glutamate monosodique, vieillissement pulmonaire, sénescence cellulaire, alimentation et maladies pulmonaires, fibrose pulmonaire