Clear Sky Science · fr
L’infection expérimentale par Sodalis élimine un symbiote ancien des insectes
Partenariats cachés à l’intérieur de minuscules ravageurs des grains
Les grains stockés dans des silos ou des garde‑manger sont souvent assiégés par des coléoptères trop petits pour être remarqués. À l’intérieur de ces insectes vivent des partenaires encore plus minuscules—des bactéries qui fournissent en silence des nutriments manquants et aident les coléoptères à survivre dans des conditions sèches et rudes. Cette étude jette un coup d’œil sur ce monde caché et montre ce qui arrive lorsque des scientifiques introduisent délibérément une nouvelle bactérie dans un coléoptère déjà dépendant d’un microbe ancien et bénéfique. Le résultat est une prise de contrôle microbienne rapide qui souligne la fragilité des alliances de longue date entre animaux et bactéries.
Un long mariage entre coléoptères et microbes utiles
De nombreux insectes dépendent de bactéries vivant à l’intérieur de leurs cellules pour synthétiser des vitamines et des acides aminés qu’ils ne peuvent pas obtenir de leurs régimes alimentaires limités. Chez le tribolion des grains, un ravageur courant des céréales stockées, un partenaire bactérien de longue date appelé Shikimatogenerans réside dans des organes spécialisés connus sous le nom de bactériomes. Ce symbionte produit un précurseur chimique que le coléoptère convertit en tyrosine, un acide aminé crucial pour le durcissement et la pigmentation de sa carapace protectrice. Après des millions d’années de coopération étroite, ces symbiontes anciens réduisent typiquement la taille de leur génome et perdent en souplesse, devenant étroitement liés à leurs hôtes—et potentiellement vulnérables aux perturbations.
Introduction d’un nouvel acteur bactérien
Pour explorer comment un microbe nouveau pourrait déloger un ancien, les chercheurs ont injecté des femelles coléoptères avec une bactérie cultivée en laboratoire, Sodalis praecaptivus, apparentée aux symbiontes trouvés chez d’autres insectes. Ils ont suivi les bactéries à l’aide d’un marqueur fluorescent et de mesures d’ADN. En une semaine, Sodalis s’était répandu dans tout le corps du coléoptère, y compris le liquide analogue au sang, les tissus adipeux, le système nerveux et les organes reproducteurs. Surtout, elle a pénétré les œufs en développement et a été transmise efficacement des mères à leur descendance, génération après génération, sans aucune aide des pères. Cette transmission verticale rapide et fiable imite une étape clé de l’évolution naturelle des symbioses bénéfiques. 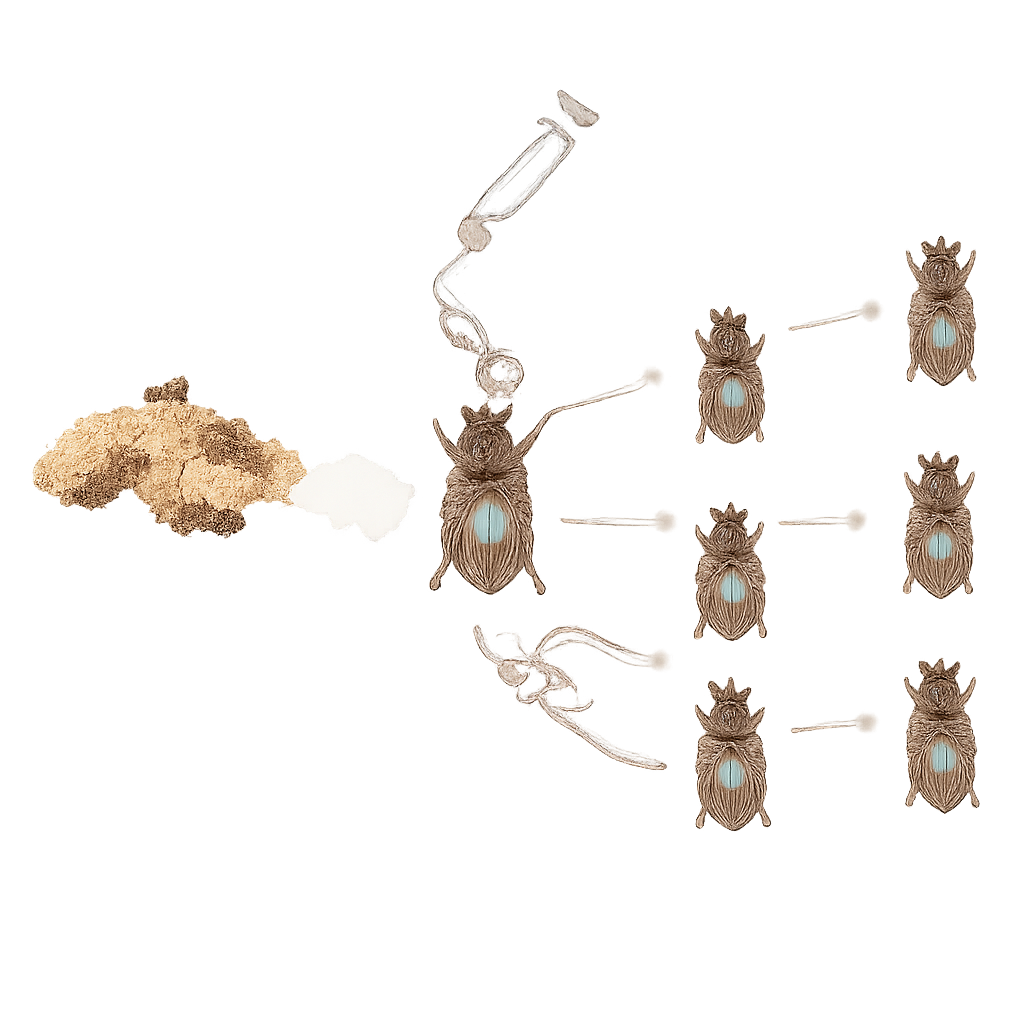
Coûts pour le coléoptère et lutte silencieuse à l’intérieur
Malgré cette colonisation réussie, le nouveau partenariat a eu un coût élevé pour les coléoptères. Les adultes infectés sont morts beaucoup plus tôt et ont produit bien moins de larves que les témoins non infectés. Les jeunes adultes portant Sodalis présentaient des carapaces plus pâles et moins pigmentées, signe que les réserves de tyrosine étaient tendues, bien que l’épaisseur de la carapace elle‑même n’ait pas changé. À l’intérieur, l’imagerie et des scans tridimensionnels ont révélé que Sodalis avait envahi les bactériomes, partageant l’espace avec Shikimatogenerans. Là où les deux bactéries coexistaient, les cellules du symbionte natif sont devenues agrandies et de forme étrange, suggérant stress ou dommages, bien que leur nombre global soit resté similaire au départ.
Quand le partenaire ancien disparaît
En seulement trois générations de coléoptères, cette coexistence précaire a basculé vers un déplacement pur et simple. À la troisième génération, chaque coléoptère porteur de Sodalis avait complètement perdu son symbionte originel et souvent ne présentait plus de bactériomes visibles, tandis que les coléoptères témoins conservaient des organes symbiotiques normaux. Les analyses d’expression génique des tissus de bactériome ont montré que le système immunitaire du coléoptère réagissait fortement à Sodalis, activant des défenses antimicrobiennes et des protéines régulatrices. En revanche, Shikimatogenerans modifiait à peine son activité, cohérent avec son génome épuré et peu flexible. Des changements subtils dans le métabolisme du coléoptère et du symbionte laissaient entendre que l’envahisseur rivalisait pour des nutriments clés, y compris ceux nécessaires à la synthèse de la tyrosine, minant encore davantage le partenaire natif. 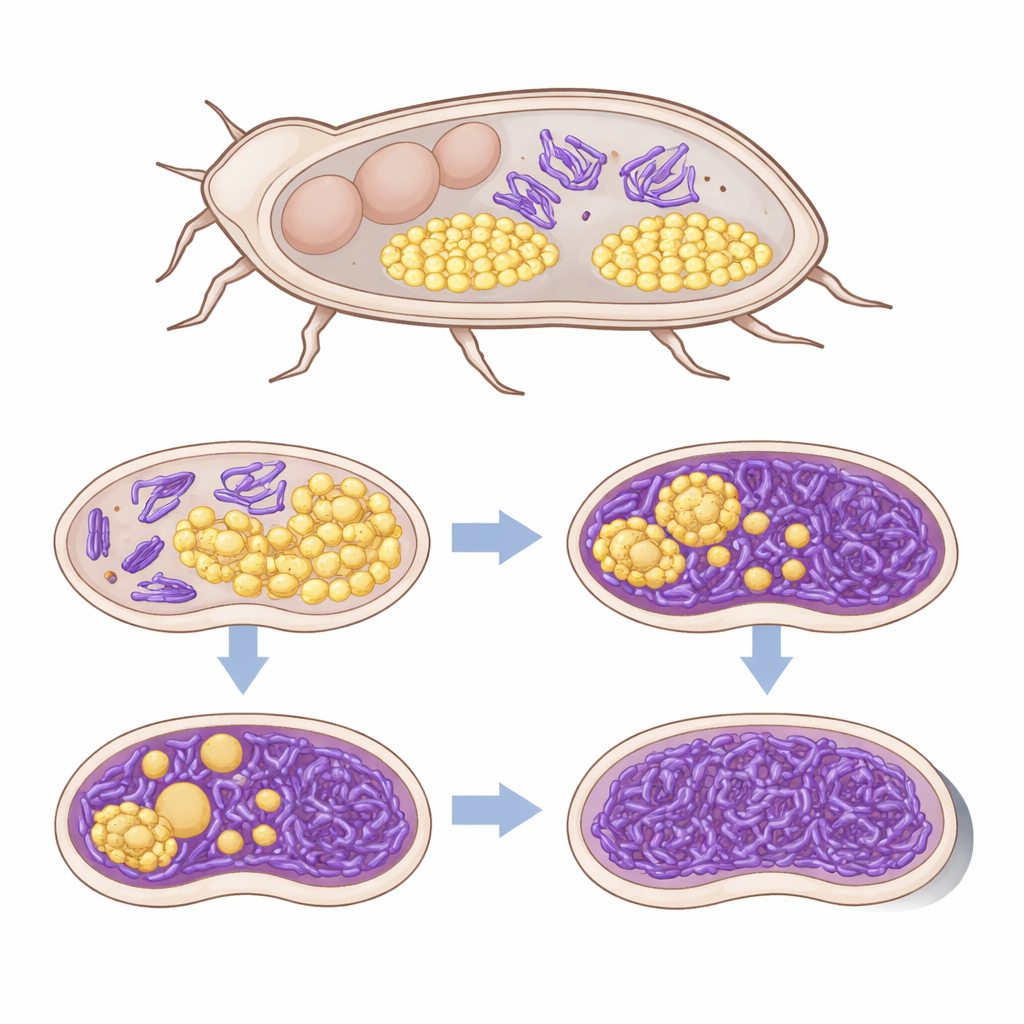
Ce que cela nous apprend sur l’évolution des alliances microbiennes
En recréant expérimentalement un stade précoce du remplacement de symbionte, ce travail montre qu’une bactérie arrivée récemment peut éliminer rapidement un partenaire bénéfique de longue date, et ce en quelques générations seulement. Dans ce cas, Sodalis satisfait déjà trois des quatre conditions considérées nécessaires pour un remplacement complet : elle s’établit à l’intérieur de l’hôte, est transmise de manière fiable de la mère à la descendance, et provoque la perte du symbionte ancestral. Ce qu’elle ne fait pas encore, c’est aider le coléoptère—au contraire, elle le nuit. Cependant, parce que Sodalis est génétiquement malléable et étroitement liée à la reproduction de l’hôte, la pression évolutive pourrait à terme favoriser des variantes qui libèrent des nutriments utiles ou atténuent leurs effets nocifs, transformant une infection destructrice en un nouveau mutualisme. L’étude offre ainsi un modèle puissant et contrôlable pour observer, en temps réel, comment les partenariats animal–microbe peuvent s’effondrer et potentiellement être reconstruit avec de nouveaux partenaires.
Citation: Krüsemer, R., Carvalho, A.S.P., Keller, J. et al. Experimental Sodalis infection eliminates ancient insect symbiont. Nat Commun 17, 3153 (2026). https://doi.org/10.1038/s41467-026-71143-2
Mots-clés: symbiose des insectes, remplacement d’endosymbionte, charançon des grains, interactions hôte‑microbe, bactéries Sodalis