Clear Sky Science · fr
Gain ou perte de domaine dans une chitinase fongique permettant une spécialisation vers l’antagonisme ou la suppression de l’immunité
Comment des champignons amicaux aident les plantes à combattre les germes et à rester calmes
Les plantes partagent leurs racines avec des communautés souterraines entières de microbes, certains utiles et d’autres nocifs. Cette étude explore comment un champignon bénéfique qui vit au niveau des racines ajuste une seule catégorie d’enzyme de sorte qu’une version fonctionne comme une arme contre des champignons dangereux, tandis qu’une version très proche désarme discrètement le système d’alerte de la plante. Comprendre cet équilibre moléculaire pourrait inspirer de meilleures façons de protéger les cultures sans recours important aux produits chimiques.
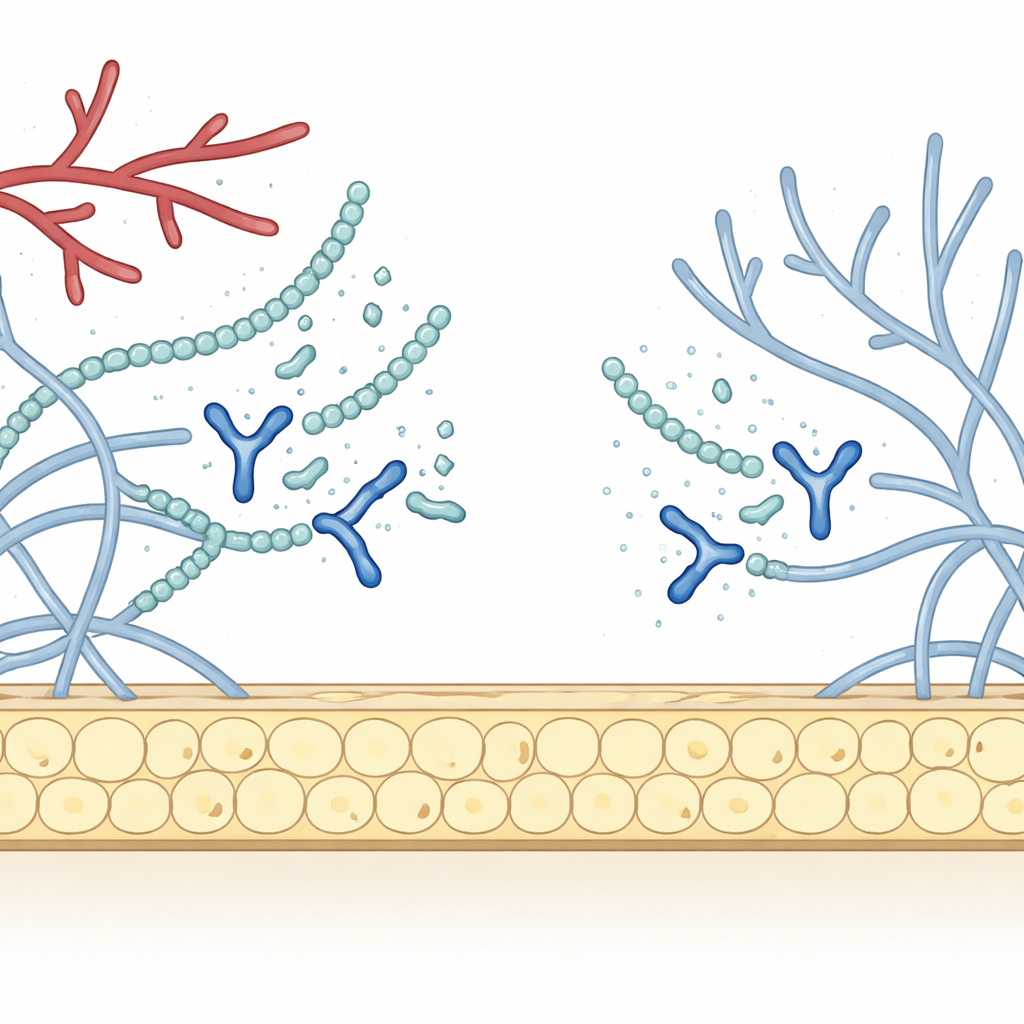
Deux fonctions pour un même type d’enzyme
Les chercheurs se sont intéressés à un champignon racinaire bénéfique appelé Serendipita indica, reconnu pour stimuler la croissance des plantes et protéger les racines contre les maladies. Comme beaucoup de microbes, il produit des chitinases — des enzymes qui coupent la chitine, un matériau résistant constituant les parois cellulaires fongiques ainsi que des fragments que les plantes utilisent comme signaux de danger. L’énigme était de savoir pourquoi certaines de ces chitinases semblent agir en mode attaque contre des champignons rivaux, alors que d’autres paraissent aider le champignon à se faufiler devant l’immunité de la plante. L’équipe s’est concentrée sur une famille de chitinases conservée et a examiné comment de petits éléments structuraux additionnels, ou domaines, pouvaient orienter chaque enzyme vers un rôle écologique différent.
Une poignée amovible transforme une enzyme en bouclier antifongique
Une enzyme, nommée SiCHIT, porte une attache supplémentaire à son extrémité C‑terminale connue sous le nom de domaine CBM5. Cet ajout agit comme un tampon d’adhérence qui aide l’enzyme à se fixer sur la chitine cristalline et rigide des parois fongiques. Lorsque les scientifiques ont retiré le CBM5, l’enzyme pouvait encore couper la chitine en éprouvette, mais elle a perdu sa capacité à se lier fermement à la chitine solide et aux parois cellulaires d’un champignon pathogène, Bipolaris sorokiniana. Sans ce domaine, SiCHIT n’a plus ralenti la germination des spores du pathogène ni protégé les racines d’orge et d’Arabidopsis contre la maladie. Le greffage du même module CBM5 sur une chitinase apparentée a rétabli une forte activité antifongique et la protection des plantes, montrant que ce petit domaine est une pièce modulaire pouvant transformer une enzyme de base en un outil défensif ciblé.
Une version allégée calme le système d’alarme de la plante
Juste à côté de SiCHIT dans le génome du champignon se trouve son homologue SiCHIT2, qui partage une grande partie du même noyau catalytique mais qui, naturellement, ne possède pas la poignée CBM5. Contrairement à SiCHIT, SiCHIT2 n’est pas activée pendant les confrontations avec d’autres champignons. À l’inverse, elle est fortement exprimée lorsque le champignon colonise les racines de plusieurs espèces hôtes. Des expériences sur racines de plantes ont montré que SiCHIT2 excelle à couper de petits fragments solubles de chitine qui déclenchent normalement un déferlement d’espèces réactives de l’oxygène — un « flash » rapide de défense de la plante. Lorsque les fragments de chitine ont été prétraités avec des versions de l’enzyme dépourvues de CBM5, la poussée défensive était fortement réduite et Serendipita colonisait mieux les racines. La présence du CBM5, en revanche, orientait l’enzyme vers l’attaque des parois solides et l’éloignait du nettoyage rapide de ces fragments activateurs d’immunité.
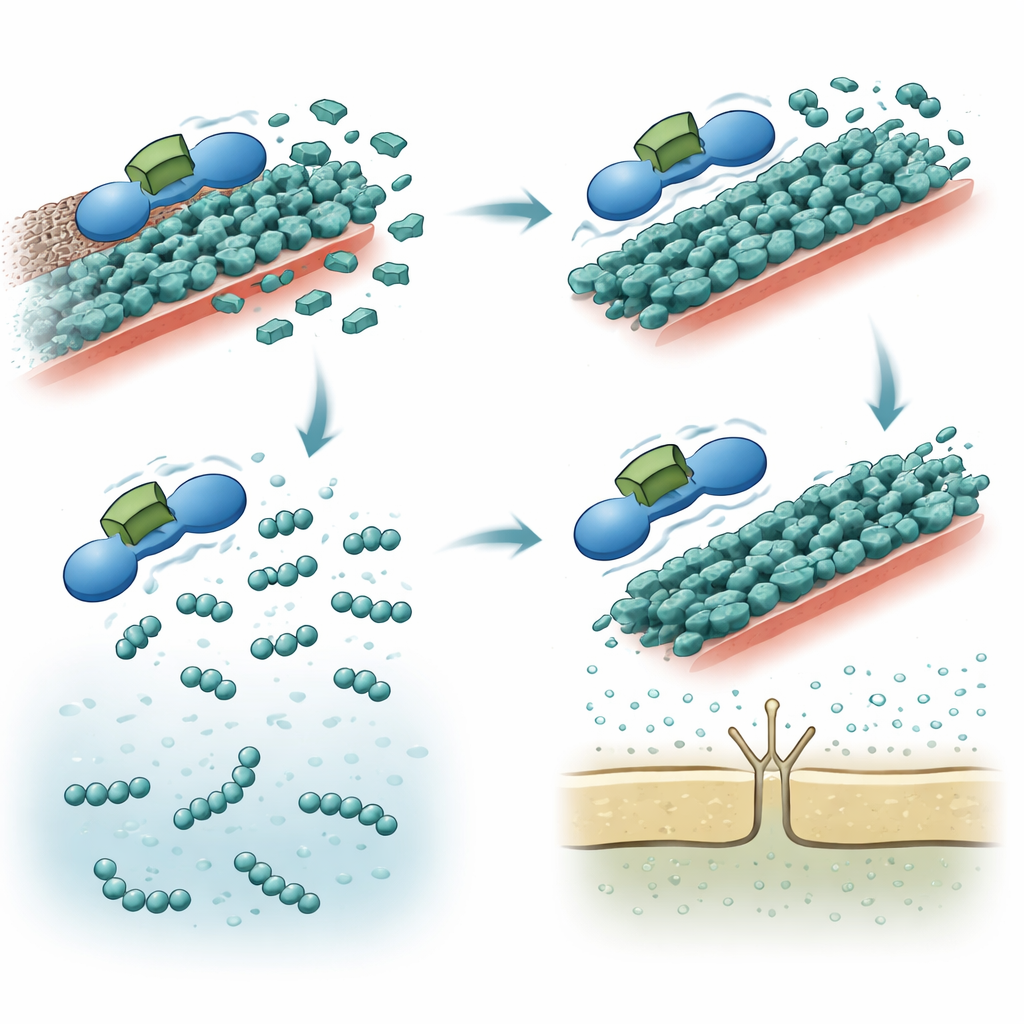
Évolution par ajout et perte de modules
Pour inscrire ces résultats dans un contexte évolutif plus large, l’équipe a examiné des chitinases apparentées à travers de nombreux champignons. Ils ont constaté que des enzymes combinant le noyau catalytique avec le CBM5 sont courantes dans certains groupes fongiques et apparaissent souvent dans des clusters de gènes dupliqués. Certains duplicata ont conservé le domaine CBM5, tandis que d’autres, comme SiCHIT2, l’ont perdu. Parallèlement, les régulations « marche–arrêt » de ces gènes ont divergé, de sorte qu’une copie est induite lors de confrontations microbiennes dans le sol, tandis qu’une autre est activée à l’intérieur des racines des plantes. Ce schéma soutient un scénario où la duplication génique, suivie d’un gain ou d’une perte de domaines et d’un remaniement de l’expression, a permis de réaffecter une enzyme antimicrobienne ancestrale à la suppression de l’immunité dans un mode de vie mutualiste.
Ce que cela signifie pour la santé des plantes
En termes concrets, ce travail montre comment un champignon bénéfique peut porter deux versions d’essentiellement le même outil, chacune réglée pour une tâche différente. Avec son ajout CBM5, une chitinase devient un ciseau de précision qui attaque les parois des champignons concurrents et protège les racines des infections. Dépourvue de cette prise supplémentaire, l’enzyme sœur change de rôle et déchiquette rapidement les miettes de chitine qui, sinon, déclencheraient l’alarme de la plante, permettant au champignon de s’installer paisiblement. En révélant comment de simples changements dans les « attaches » protéiques et le timing d’expression génique peuvent rediriger la fonction d’une enzyme, l’étude met en lumière une stratégie élégante que les champignons racinaires amicaux utilisent pour concilier défense contre les ennemis et harmonie avec leurs hôtes végétaux.
Citation: Eichfeld, R., Endeshaw, A.B., Hellmann, M.J. et al. Domain gain or loss in a fungal chitinase enables specialization towards antagonism or immune suppression. Nat Commun 17, 3115 (2026). https://doi.org/10.1038/s41467-026-71064-0
Mots-clés: microbiome racinaire, endophyte fongique, immunité des plantes, chitinase, protection des cultures