Clear Sky Science · fr
Production d’hydrogène solaire par dissociation de l’eau de mer à pression ambiante
Transformer l’eau de mer et la lumière du soleil en carburant propre
La plupart de l’eau sur Terre est salée, et pourtant presque toutes les technologies qui scindent l’eau pour produire de l’hydrogène exigent de l’eau douce purifiée et des équipements complexes. Cette étude décrit un nouveau matériau solide capable d’utiliser de l’eau de mer ordinaire et la lumière solaire, à la pression atmosphérique, pour générer efficacement du gaz hydrogène. En repensant la manière dont les charges se déplacent à l’intérieur d’un photocatalyseur populaire, les chercheurs rapprochent la possibilité de « fermes solaires » côtières extensibles qui transformeraient les océans en une vaste source d’énergie renouvelable.
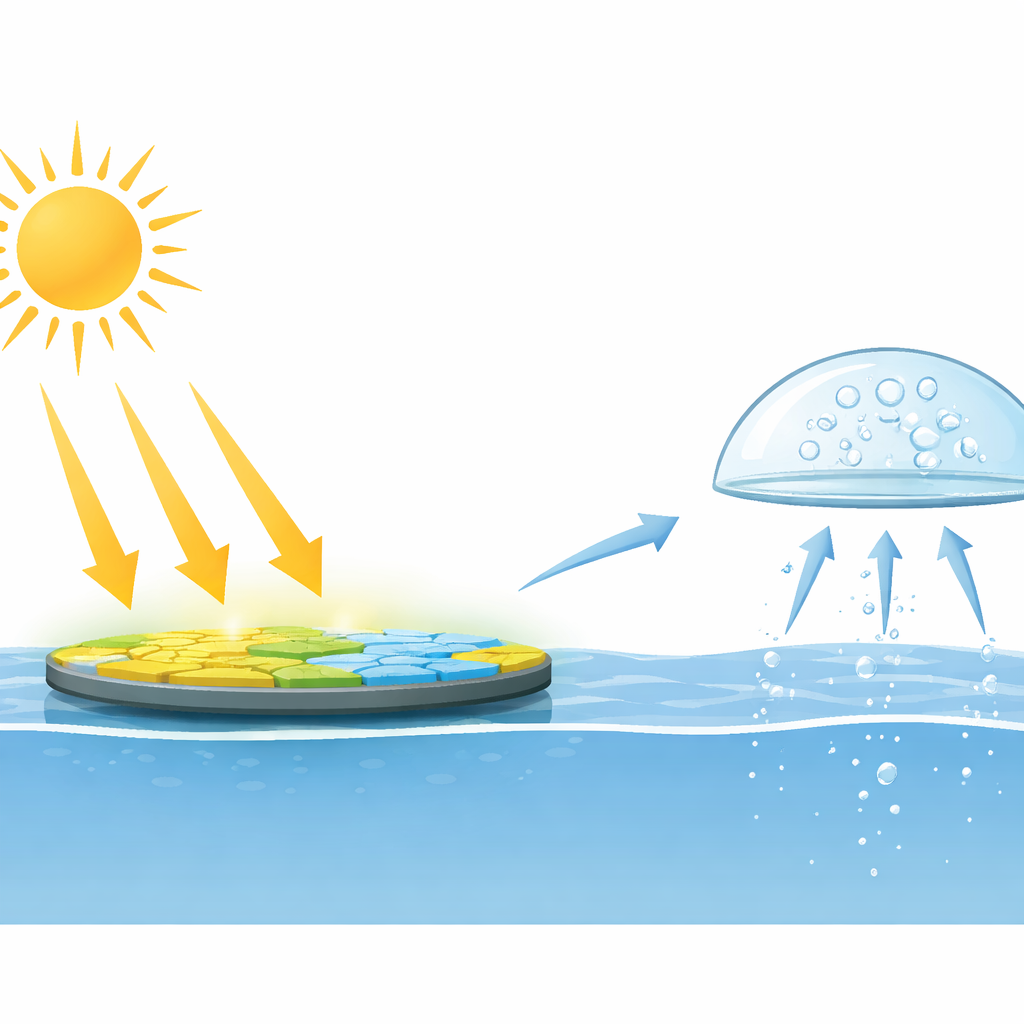
Pourquoi l’eau de mer importe pour l’énergie de demain
L’hydrogène est un carburant propre : lorsqu’il brûle, il produit de l’eau au lieu du dioxyde de carbone. Une voie prometteuse pour produire de l’hydrogène consiste à laisser un solide absorbant la lumière scinder l’eau en hydrogène et oxygène. Cependant, la plupart des systèmes actuels exigent une eau soigneusement purifiée et fonctionnent souvent sous vide partiel pour empêcher la réaction de retourner en arrière. Cette combinaison est coûteuse et difficile à déployer à l’échelle nécessaire pour une production énergétique significative. Comme environ 96,5 % de l’eau de la planète se trouve dans les océans, une technologie pratique doit fonctionner directement avec l’eau de mer, en extérieur, à la pression atmosphérique normale.
Construire un meilleur catalyseur photoactif
L’équipe s’est concentrée sur le nitrure de carbone polymérique, un matériau sans métal et relativement peu coûteux, connu pour favoriser la production d’hydrogène sous illumination. Son principal défaut est que, lorsqu’il absorbe la lumière, les électrons et les trous s’attirent fortement et ont tendance à se recombiner avant de pouvoir accomplir une chimie utile. Pour remédier à cela, les chercheurs ont greffé des unités « pyrène » fortement riches en électrons sur des feuillets ultrafins de nitrure de carbone en utilisant de petits linkers aromatiques appelés ponts π. Cela a créé un cadre donneur–pont–accepteur dans lequel les électrons migrent naturellement des donneurs pyrène vers le réseau de nitrure de carbone, établissant une poussée interne de charges à travers le matériau.
Comment le nouveau matériau fonctionne dans l’eau de mer
Parmi plusieurs conceptions, une version avec un linker biphényle, nommée UPy2, a donné les meilleures performances. Des mesures optiques détaillées et des expériences par lasers ultrarapides ont montré que UPy2 réduit l’énergie maintenant les paires électron–trou ensemble et prolonge de façon spectaculaire la durée de vie des charges séparées. En d’autres termes, une fois que la lumière excite le matériau, électrons et trous se séparent et restent éloignés suffisamment longtemps pour participer aux réactions chimiques. Le champ électrique interne créé par la structure donneur–pont–accepteur aide à balayer les électrons vers les régions où l’hydrogène peut se former et les trous vers des sites où ils peuvent être consommés en toute sécurité.
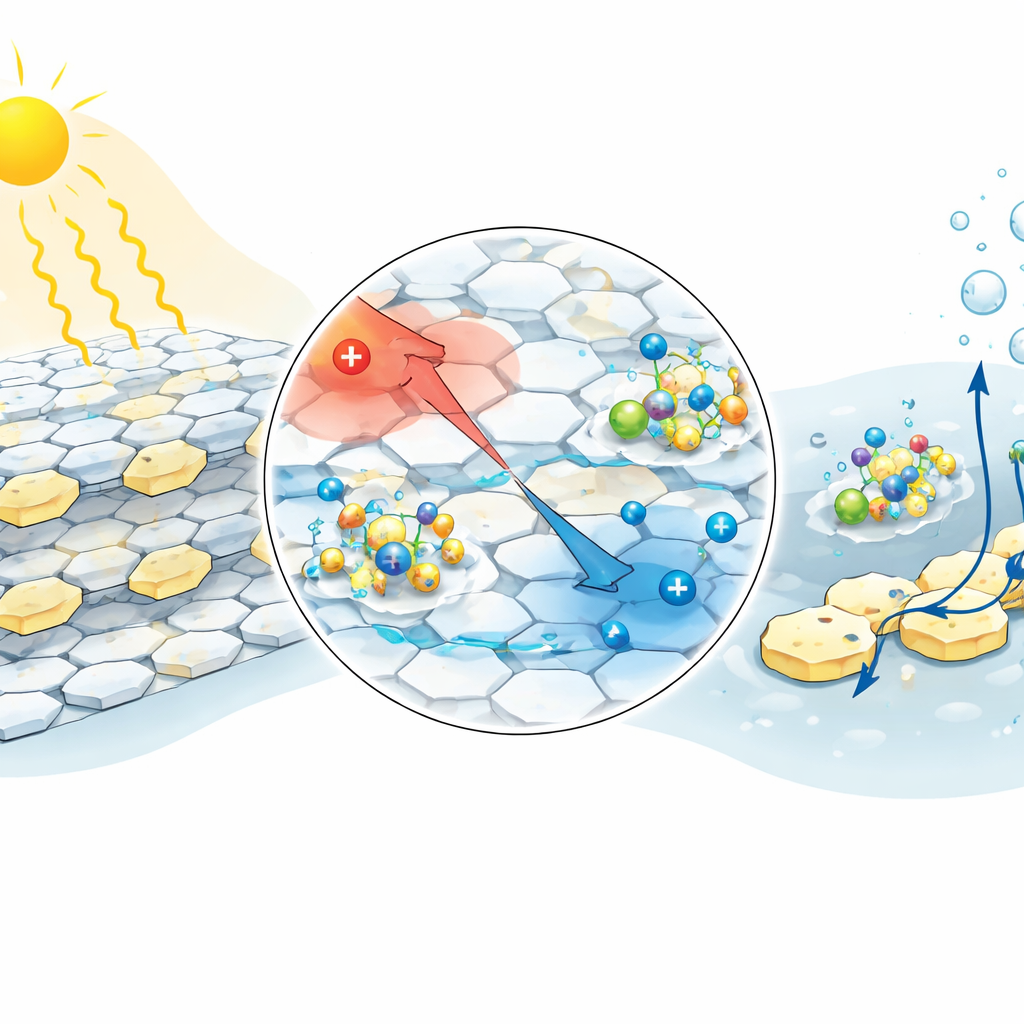
Les ions de l’eau de mer comme aides cachées
L’eau de mer réelle contient du sodium, du magnésium, du calcium et d’autres ions, ainsi que la molécule organique auxiliaire triéthanolamine utilisée ici pour éliminer les trous. Calculs et expériences suggèrent que le nitrure de carbone reconfiguré accumule des électrons supplémentaires autour de ses unités en anneau « heptazine ». Cette charge négative supplémentaire le rend particulièrement apte à attirer des complexes métal–triéthanolamine chargés positivement présents dans l’eau de mer. Une fois attachés, ces complexes éliminent rapidement les trous, ce qui réduit encore la recombinaison et permet à davantage d’électrons d’être canalisés vers la conversion des protons de l’eau en hydrogène. Même les composés de magnésium qui se forment lentement à la surface semblent aider au transfert de charge plutôt que de simplement obstruer le catalyseur.
Du réacteur de laboratoire à l’eau de mer en plein soleil
Dans des tests contrôlés avec une lumière simulée, UPy2 a alimenté la production d’hydrogène à partir d’eau de mer naturelle à des taux bien supérieurs à ceux du nitrure de carbone ordinaire, et ce en plein air sans gaz protecteur. Les chercheurs ont ensuite monté l’échelle avec un réacteur en disque peu profond de 20 centimètres de diamètre rempli d’eau de mer et placé en extérieur. Sous la lumière réelle du soleil, ce dispositif simple a produit suffisamment d’hydrogène pour être collecté, analysé et même enflammé, le tout à pression ambiante. Ce travail montre qu’en orientant soigneusement la manière dont les charges induites par la lumière se déplacent à l’intérieur d’un solide, et en exploitant les ions déjà présents dans l’eau de mer, il est possible de transformer un matériau courant et stable en une plateforme pratique pour la production d’hydrogène solaire à grande échelle à partir de la mer.
Citation: Li, K., Xiao, T., Tang, J. et al. Solar hydrogen production through ambient-pressure seawater splitting. Nat Commun 17, 2836 (2026). https://doi.org/10.1038/s41467-026-69583-x
Mots-clés: production d’hydrogène à partir d’eau de mer, carburants solaires, conception de photocatalyseur, carbure nitride, énergie verte